EAE 小鼠模型的神經發炎:mIF 與細胞激素分析
目录
我們的研究互動簡報
研究摘要:EAE 的細胞因子分析
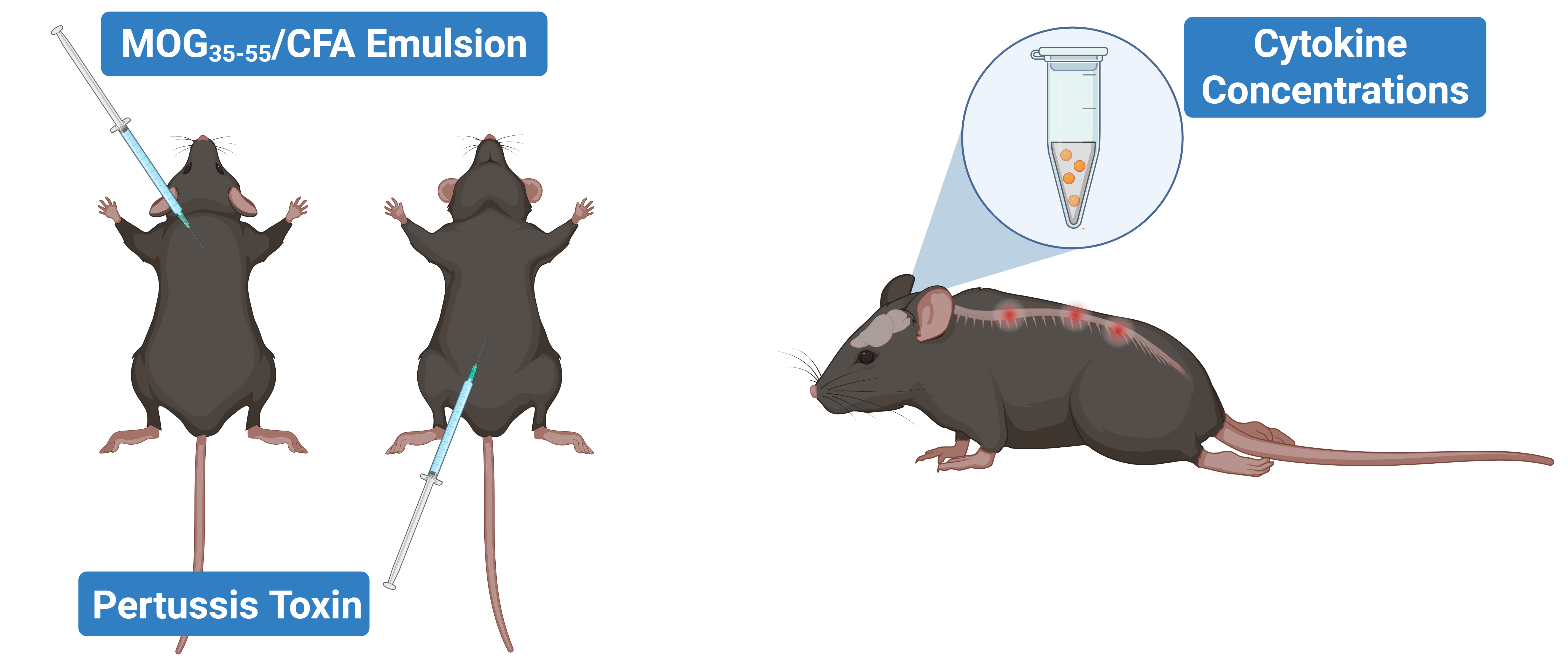
我們直接測量 EAE 中多種基質(中樞神經組織和體液)的細胞因子蛋白水平,以捕捉免疫反應的一個方面,這方面經常被推斷,但較少在蛋白水平上量化。我們使用MOG35-55與百日咳毒素在完全弗氏佐劑 (CFA) 中誘導小鼠發生 EAE,並在免疫後 21 天進行疾病評估。細胞因子水平(IL-1β、TNF-α、IFN-γ、IL-6、IL-10、IL-4、IL-2、IL-5 和趋化因子 KC/GRO)在末端血漿、CSF 和脊髓勻質物中使用超高靈敏度多重免疫分析法進行定量。
IL-2 和 TNF-α 在 CSF 中顯著升高,而 IFN-γ、IL-1β、IL-2、IL-6 和 TNF-α 則在脊髓勻質物中升高;在血漿中則未發現顯著差異。這些研究結果顯示,EAE 的發炎細胞因子上調在測定的 21 天結束點時,基本上只限於中樞神經系統。我們的觀察結果與先前的報告一致,這些報告顯示脊髓組織中的細胞因子濃度增加,但血清中的濃度沒有增加(Alassiri, 2023),而且血漿中的細胞因子也有選擇性的改變,有些細胞因子達到峰值,隨後隨時間下降(Borjini, 2016)。這種直接的多種生物基質細胞因子分析,為 EAE 較常報告的臨床和病理發現提供了補充的角度。
如需瞭解我們的體液與細胞生物標誌物解決方案,請參閱: 體液與細胞生物標記
在下面的「影像互動」中,您可以找到有關小膠質細胞-神經元互動的結果,包括 EAE 小鼠模型 和對照小鼠脊髓的高解析度多重免疫螢光組織切片 。
如何使用我們的互動式檢視器
透過左側面板或螢幕上的箭頭瀏覽「影像故事」。您可以使用滑鼠在高解析度顯微鏡影像中移動,並使用滾輪或 +/- 控制鍵放大/縮小。控制面板(右上方)可切換影像通道和分割覆蓋。為獲得最佳體驗,我們建議切換至全螢幕模式。 此互動式簡報可讓您探索模型的神經病理學和相關功能障礙的細節,就像直接從顯微鏡下觀察一樣。
細胞因子在實驗性自身免疫性腦脊髓炎 (EAE) 中扮演什麼角色?
多發性硬化症:臨床與病理特徵
多發性硬化症(Multiple sclerosis,簡稱 MS)是中樞神經系統(CNS)的一種慢性神經退化性自體免疫疾病,其特徵為少突胶质細胞的脫髓鞘和喪失。多發性硬化症通常有四個臨床病程:復發-發作性多發性硬化症 (RRMS)、原發性漸進性多發性硬化症 (PPMS)、繼發性漸進性多發性硬化症 (SPMS) 以及進行性-復發性多發性硬化症 (PRMS)。約有 85% 的患者最初症狀為 RRMS,在復發神經功能障礙之後,症狀會部分或完全緩解。症狀差異很大,可能包括步態障礙、視力障礙和認知障礙。
我們的 EAE 小鼠模型中的 T 淋巴細胞(CD3,紅色)。
EAE 小鼠模型脊髓中 T 淋巴細胞(CD3,紅色)的高倍視圖。
T 細胞在 MS 中的作用
多發性硬化症的病理特徵是自體反應性 T 淋巴細胞,尤其是 CD4+T 協同 (Th) 細胞亞群,滲入中樞神經系統。一旦被招募,Th 細胞會分泌促炎細胞因子及化學因子,促進免疫細胞招募、活化常駐的膠質細胞,並造成血腦屏障 (BBB) 破壞、脫髓鞘及軸突損失 (Heng,2022)。
在 Th 子集中,Th1 和 Th17 細胞是主要的參與者。Th1 細胞主要在 IL-12 和 IFN-γ 的影響下分化,並驅動巨噬細胞活化和細胞介導的發炎。Th17 細胞在 IL-6 和 TGF-β 等細胞因子的影響下產生,並分泌 IL-17A 和 GM-CSF。
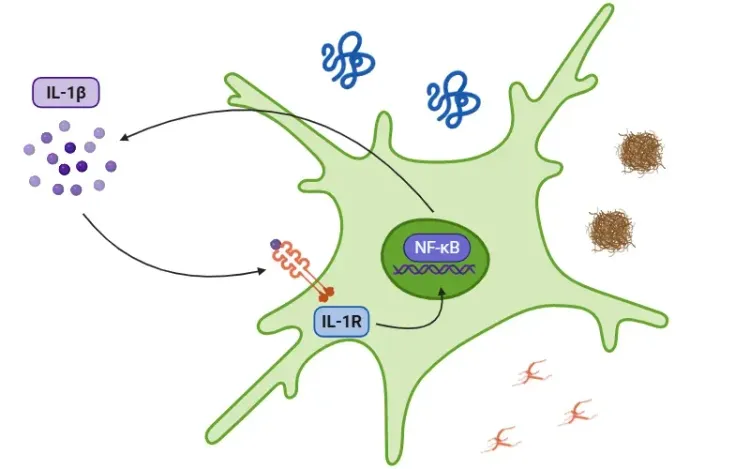
IL-17A 與多發性硬化症的發病機制有密切關聯;透過 IL-17 受體的訊號傳導可活化NF-κB,誘發額外的促發炎細胞因子產生 (包括 IL-1β),並使中性粒細胞和單核細胞持續招募至發炎部位(Heng,2022)。
請參閱我們的資源: 什麼是 NF-κB(核因子 Kappa B)?
膠質細胞與 NLRP3 發炎體
中樞神經系統駐留的膠質細胞會擴大由浸潤的 T 細胞所引發的發炎反應。星形細胞是多發性硬化症免疫病理的關鍵貢獻者,它們對 Th 細胞衍生的細胞因(cytokines)採用反應表型,擴大神經發炎並加劇組織損傷(Kunkl,2022)。反應性星形細胞會進一步損害 BBB,造成脫髓鞘和軸突損傷。巨噬細胞/小細胞也會活化並釋放發炎介質,以維持局部免疫反應並促進病變發展。
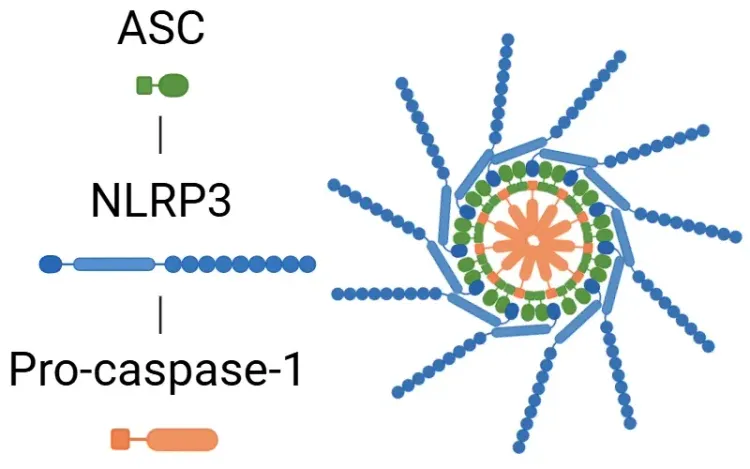
此外,NLRP3 發炎體的活化代表了 MS 重要的先天性免疫機制。NLRP3 發炎體是由 NLRP3 感應蛋白、ASC 適應體和 caspase-1 組成的多蛋白複合體。當它被啟動時,會觸發熱變性,釋放 IL-1β 和 IL-18,從而促進神經發炎和神經元損傷(Xu,2025)。與此過程相符的是,在 MS 和 EAE 模型中,IL-1β 水平都會升高(Borjini,2016;Malhotra,2020;Boraschi,2023)。
如需更多資訊,請造訪:
在我們的 EAE 小鼠模型中,顯示神經發炎的星形細胞 (GFAP,紫色)。
在我們的 EAE 小鼠模型中,巨噬細胞/小細胞(Iba-1,橘色)顯示神經炎症。
多發性硬化症中的細胞因子和趨化因子
細胞活素和化學因子是多發性硬化症免疫驅動組織損傷的核心媒介。趨化因子可調節白血球招募至中樞神經系統,進而促進發炎和脫髓鞘(Arimitsu,2025 年)。腫瘤壞死因子-α(TNF-α)是多發性硬化症的主要促發炎細胞因子,在患者和動物模型的腦脊液(CSF)中升高(Borjini,2016;Zahid,2021)。它是 MS 和 EAE 病變中最突出的細胞因子之一(Maguire, 2021)。TNF-α 會造成二次神經元和軸突損傷,不過它也可能透過不同的受體通路(例如 透過 TNFR2 與 TNFR1) 發揮依賴環境的保護效果。
除了促發炎因子之外,免疫調節細胞因子也會影響 MS 的進展。例如,IL-2 和 TGF-β 會驅使幼稚 T 細胞分化為調節性 T (Treg) 細胞,而調節性 T (Treg) 細胞會透過抑制性細胞激素釋放和其他機制維持免疫耐受;促炎性 Th17 細胞和抗炎性 Treg 細胞之間的不平衡與疾病發病機制有關(Zhang,2021)。MS 病變的最終特徵是浸潤的 T 和 B 淋巴細胞、活化的巨噬細胞/小細胞,以及驅動慢性發炎、脫髓鞘和神經軸退化的複雜細胞因子環境。
實驗性自身免疫性腦脊髓炎作為多發性硬化症的模型
實驗性自身免疫性腦脊髓炎(Experimental Autoimmune Encephalomyelitis,EAE)是多發性硬化症(MS)的黃金標準動物模型,重現了人類疾病的許多病理特徵。細胞介素驅動的脫髓鞘和神經退化是 MS 病理學的核心,也是 EAE 的主要特徵。例如,EAE 小鼠大腦中的 IL-6 增加(Leuti,2021;Marin-Prida,2022)。髓鞘少突細胞糖蛋白 (MOG)35-55 誘發的小鼠 EAE 被廣泛使用,並反映出 MS 的重要方面,包括中樞神經系統免疫細胞浸潤,以及依模型而定的復發-發作或慢性進行性病程。
然而,儘管許多 EAE 研究著重於臨床、組織病理學及/或基因表達讀數,但使用高靈敏度的多重免疫分析方法直接量化匹配組織和生物流體中細胞因子濃度的研究則相對較少。這種資料的缺乏突顯了多重生物基質細胞因子分析作為傳統 EAE 終點補充的重要性。
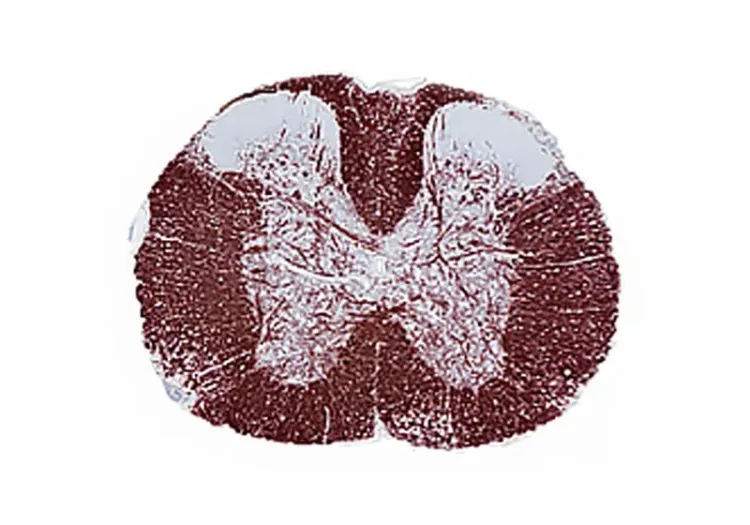
EAE 誘導會導致後肢麻痹和神經發炎,多種生物基質(包括 CSF、血液和脊髓)中的細胞因子水平均可量化。
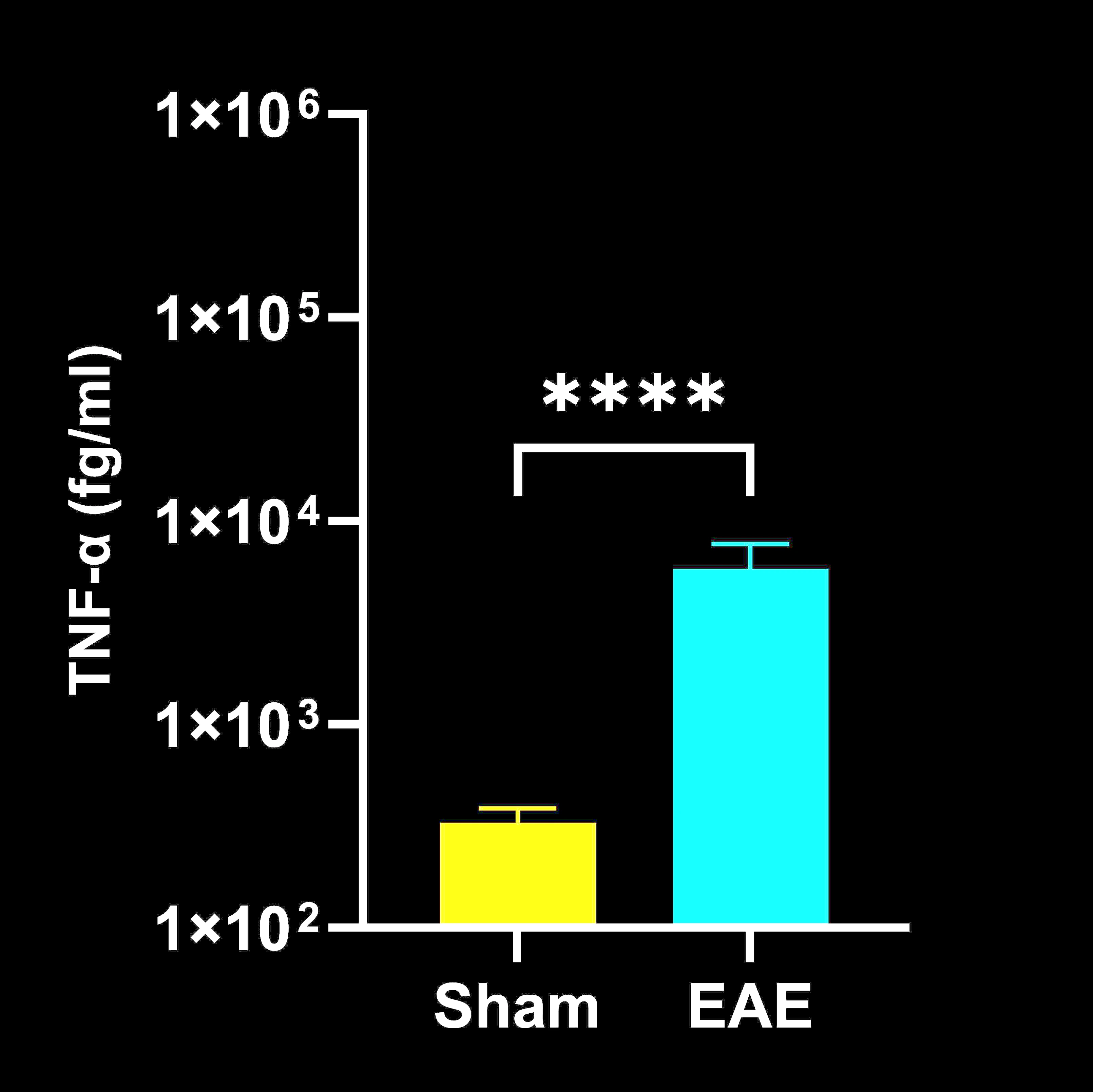
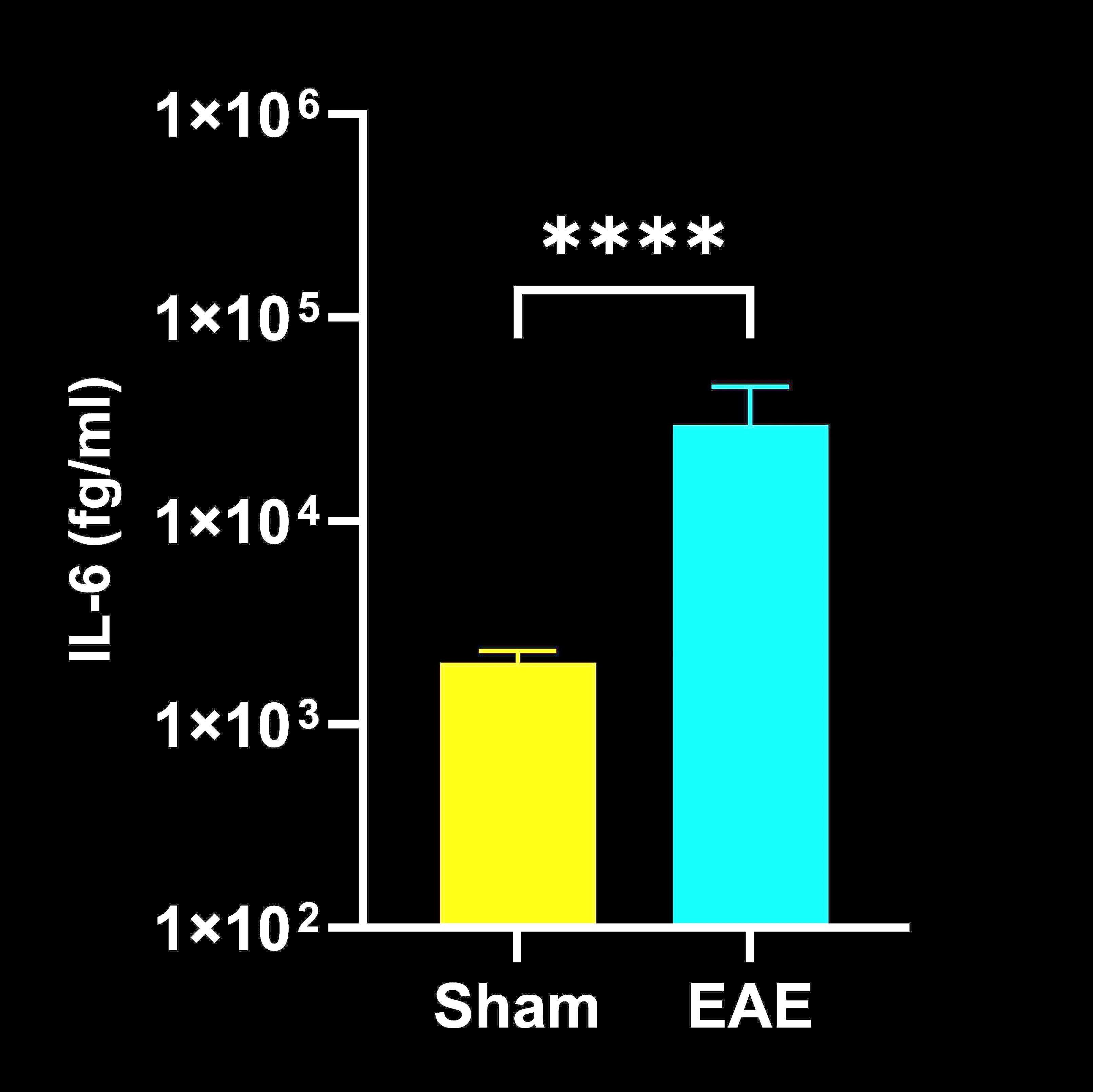
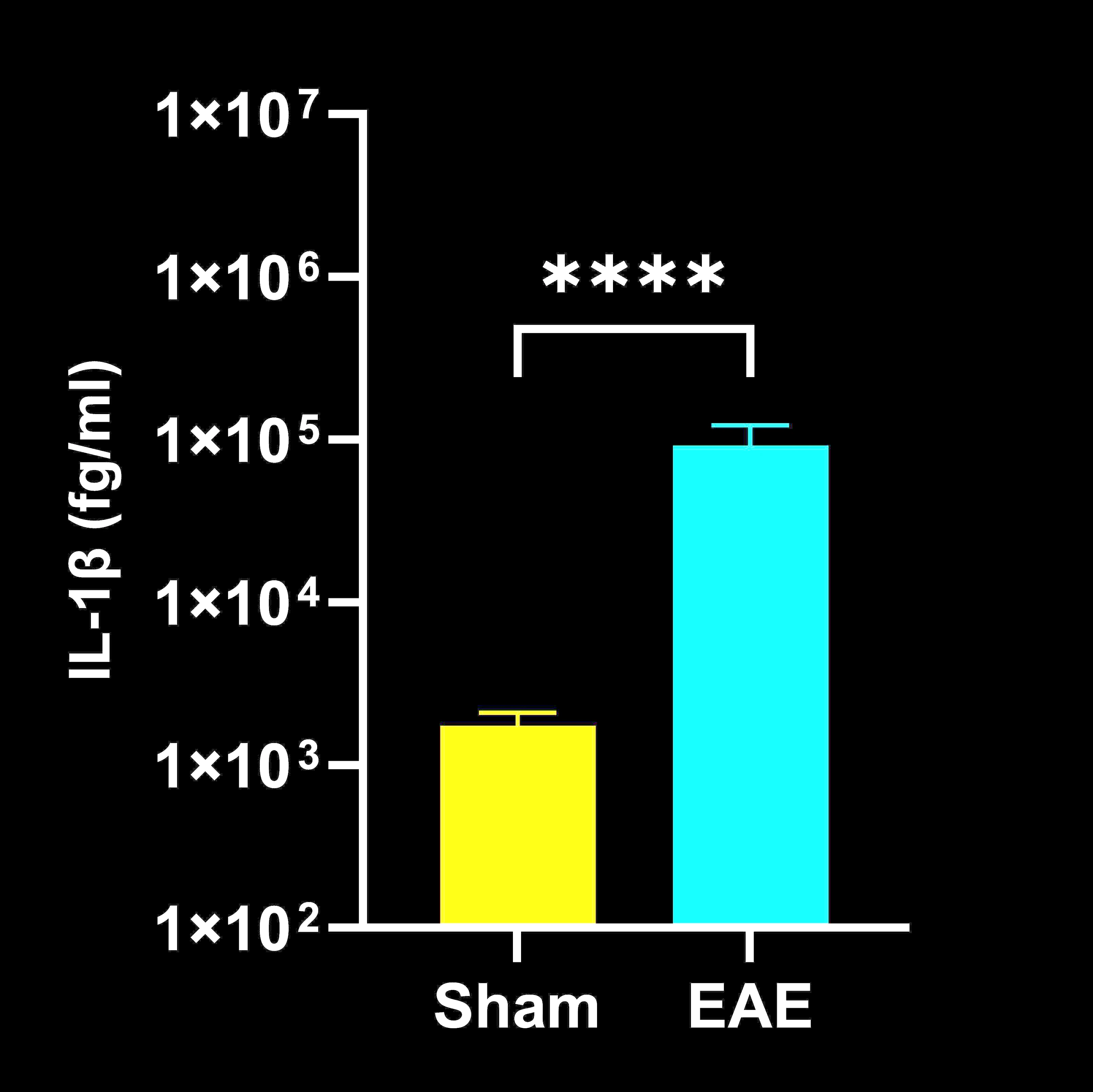
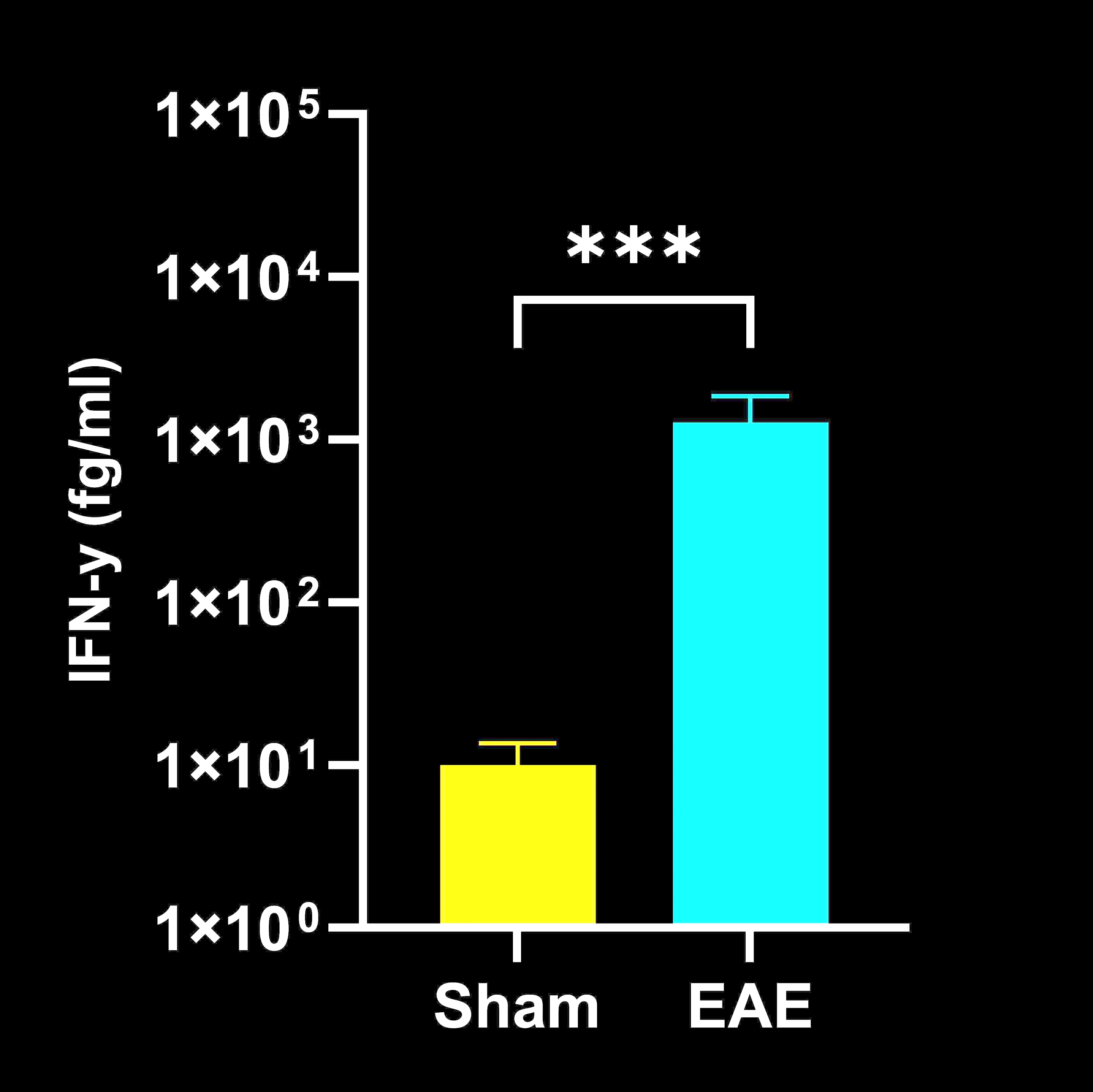
脊髓勻質物中的細胞因子濃度
EAE 與 Sham (對照) 小鼠的脊髓勻質細胞因子濃度;平均值 ± SEM,*** p<0.001; **** p<0.0001。
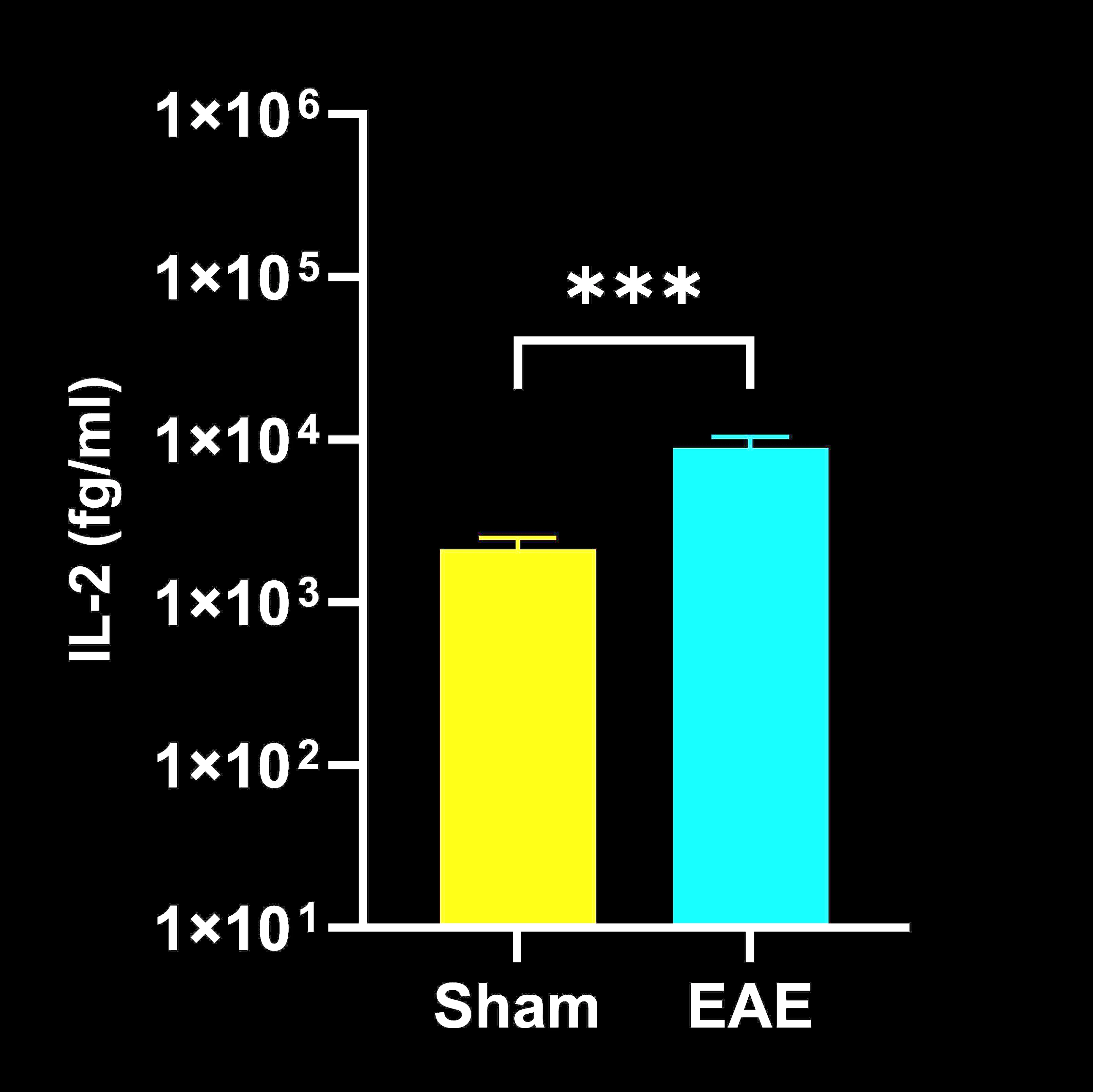
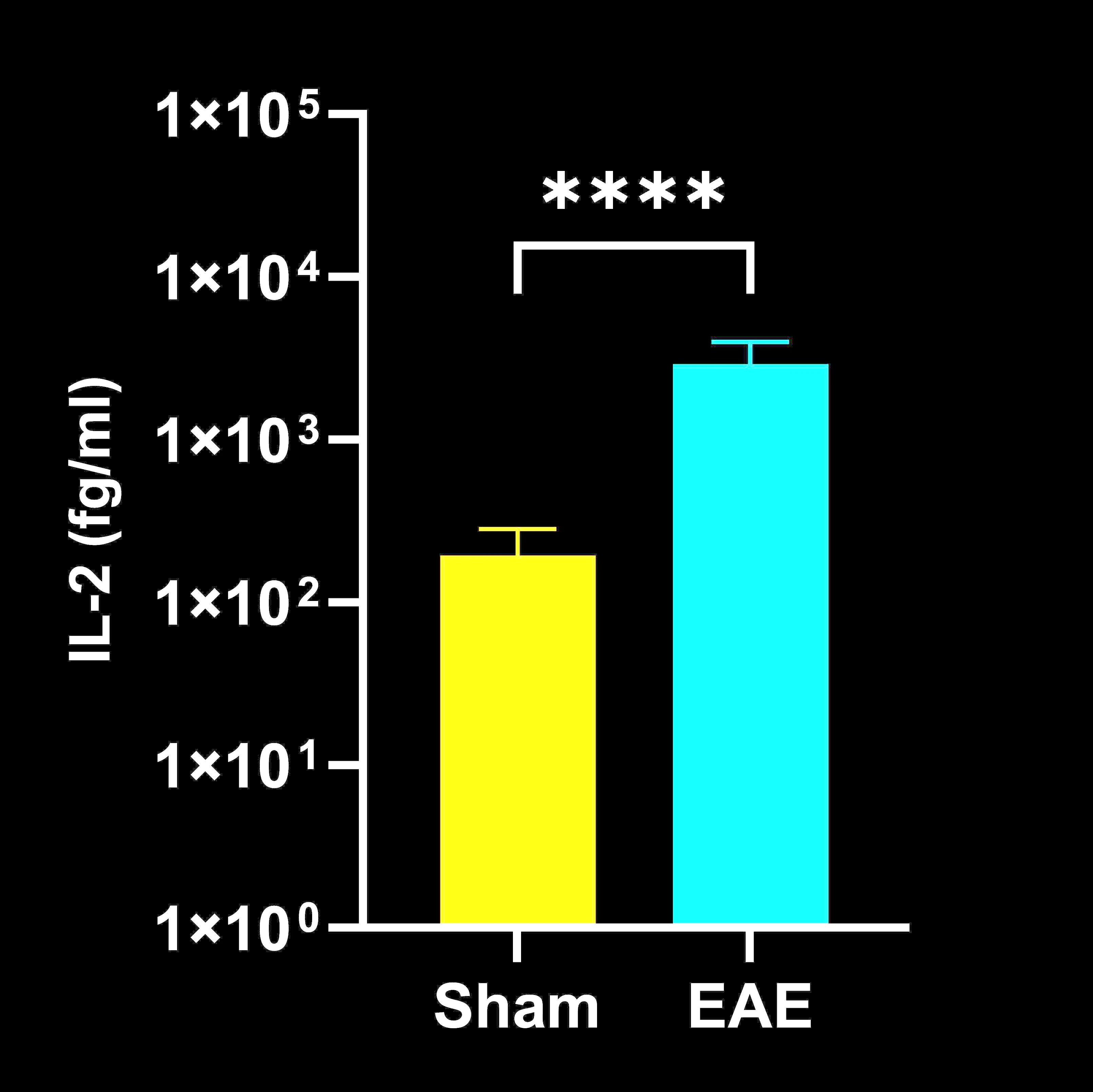
腦脊液 (CSF) 中的細胞因子濃度
EAE 與 Sham (對照) 小鼠 CSF 終期細胞因子濃度;平均值 ± SEM,*** p<0.001。
血漿中的細胞因子濃度
EAE 與 Sham (對照) 小鼠的末期血漿細胞因子濃度;平均值 ± SEM。
常見問題
進一步了解我們的神經退化性疾病模型
相關內容
關於細胞因子分析與神經發炎的最新資訊,以及在神經退化性疾病動物模型中評估治療藥物相關的最佳實踐。
什么是EAE(实验性自身免疫性脑脊髓炎)?
多发性硬化症(MS)EAE动物模型的概述,涵盖其病理生理学机制及用于临床前治疗研究的阳性对照应用。
实验性自身免疫性脑脊髓炎(EAE)和轴索损伤
本资源描述了在多发性硬化症(MS)EAE模型中测量轴突损伤和轴突变性的可用方法,包括组织标记物以及血浆和脑脊液神经丝轻链(NfL;NF-L)水平。
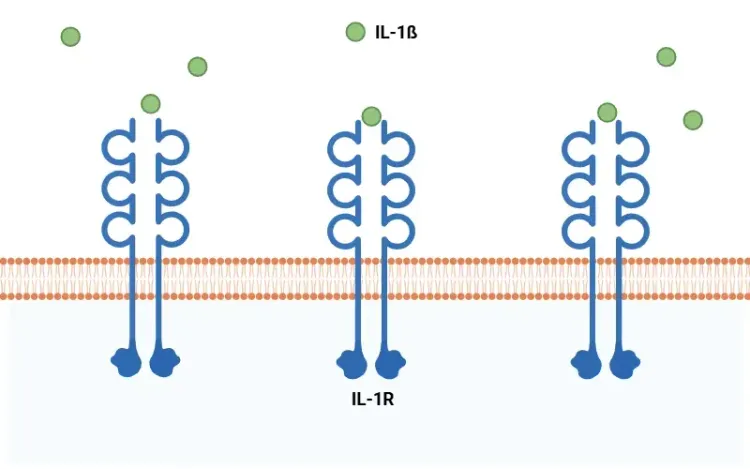
什么是IL-1β?
白细胞介素-1β(IL-1β)的概述、其在全身性及神经系统疾病中的促炎作用,以及基于IL-1β拮抗作用的治疗策略。
白细胞介素-1β(IL-1β)与神经退行性疾病
白细胞介素-1β(IL-1β)在神经退行性疾病中的作用,包括阿尔茨海默病(AD)、帕金森病(PD)和肌萎缩侧索硬化症(ALS)。
TNF-α与神经退行性疾病中的星形胶质细胞
星形胶质细胞中TNF-α信号传导的概述、其在神经退行性变中的作用以及针对该通路的治疗策略。
神经退行性疾病中的TNF-α和微胶质细胞
概述肿瘤坏死因子-α(TNF-α)在小胶质细胞中的作用及其对神经退行性病变进展的影响。
NLRP3炎症小体与神经退行性疾病
NLRP3炎症小体及其在神经退行性疾病(包括阿尔茨海默病、帕金森病和肌萎缩性脊髓侧索硬化症)中作用的概述。
什么是NLRP3?
NLRP3及NLRP3炎症小体激活的触发机制、疾病关联及治疗靶点策略综述。