EAEマウスモデルにおける神経炎症:mIFとサイトカインの解析
目次
インタラクティブな研究発表
研究概要:EAEにおけるサイトカイン・プロファイリング
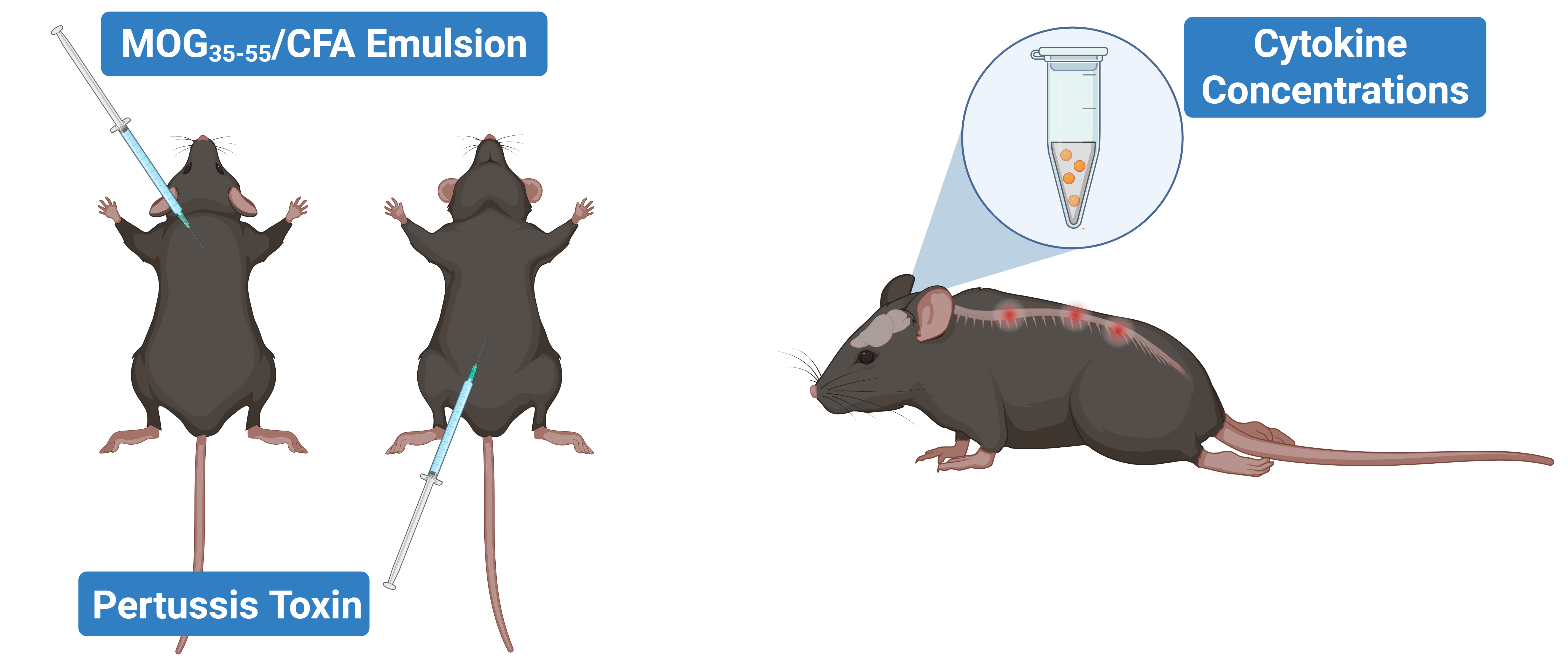
我々は、EAEにおける複数のマトリックス(中枢神経系組織と体液の両方)のサイトカインタンパク質レベルを直接測定し、推測されることは多いが、タンパク質レベルで定量化されることはあまりない免疫応答の側面をとらえた。百日咳毒素を含む完全フロイントアジュバント(CFA)中のMOG35-55を用いてマウスにEAEを誘発し、免疫後21日目に発病を評価した。サイトカインレベル(IL-1β、TNF-α、IFN-γ、IL-6、IL-10、IL-4、IL-2、IL-5、およびケモカインKC/GRO)は、終末血漿、髄液、および脊髄ホモジネート中の超高感度マルチプレックスイムノアッセイによって定量した。
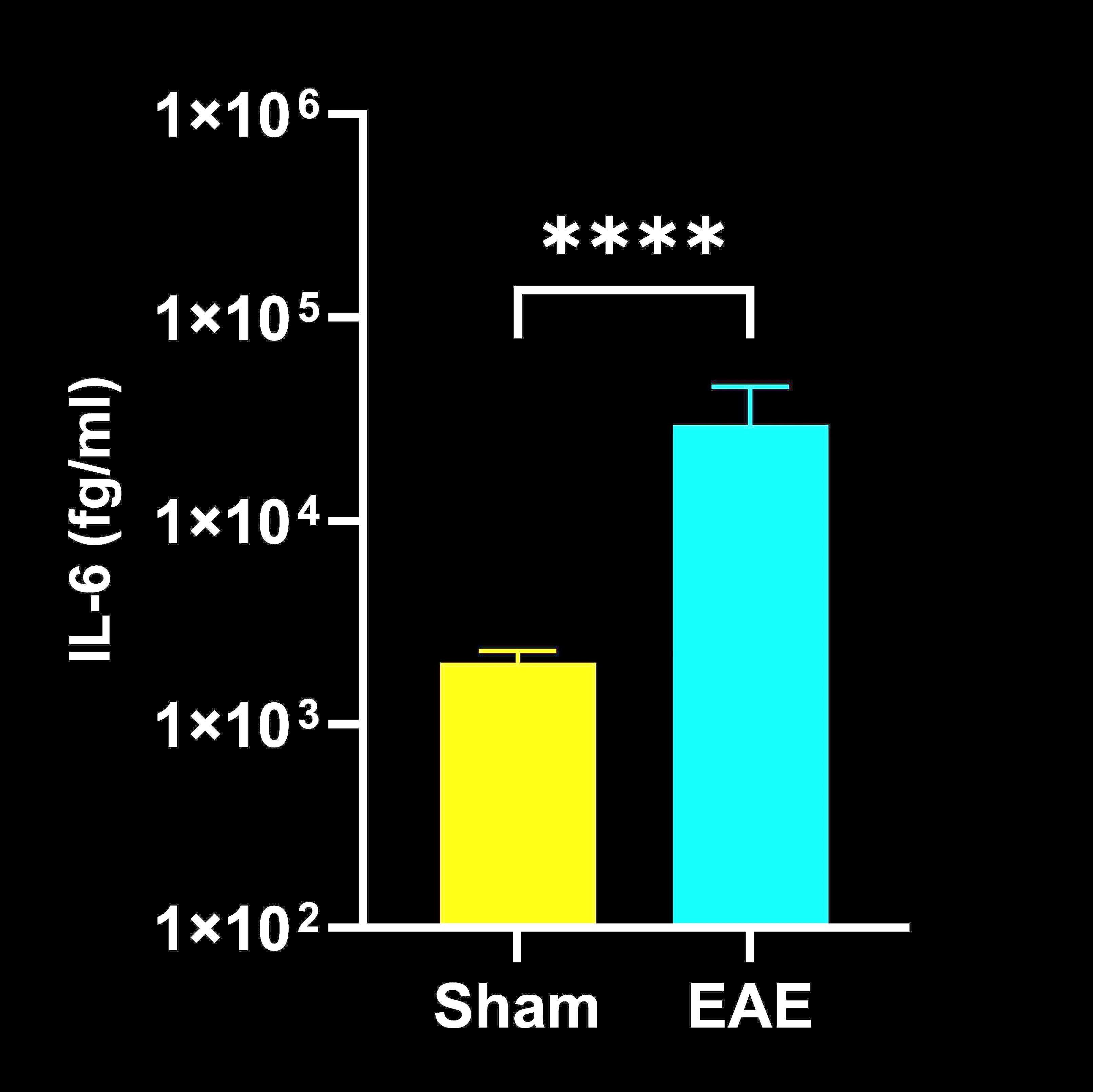
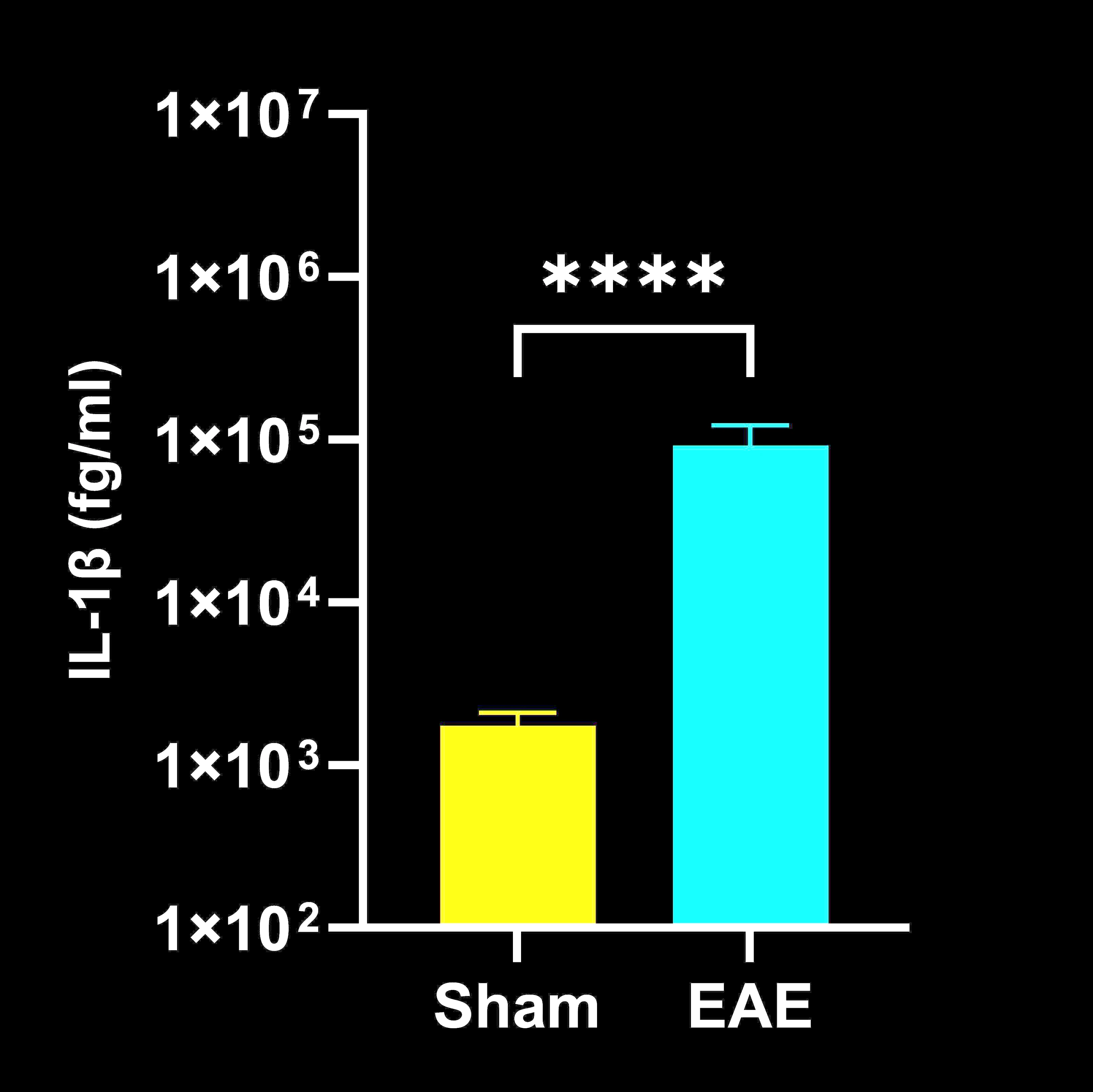
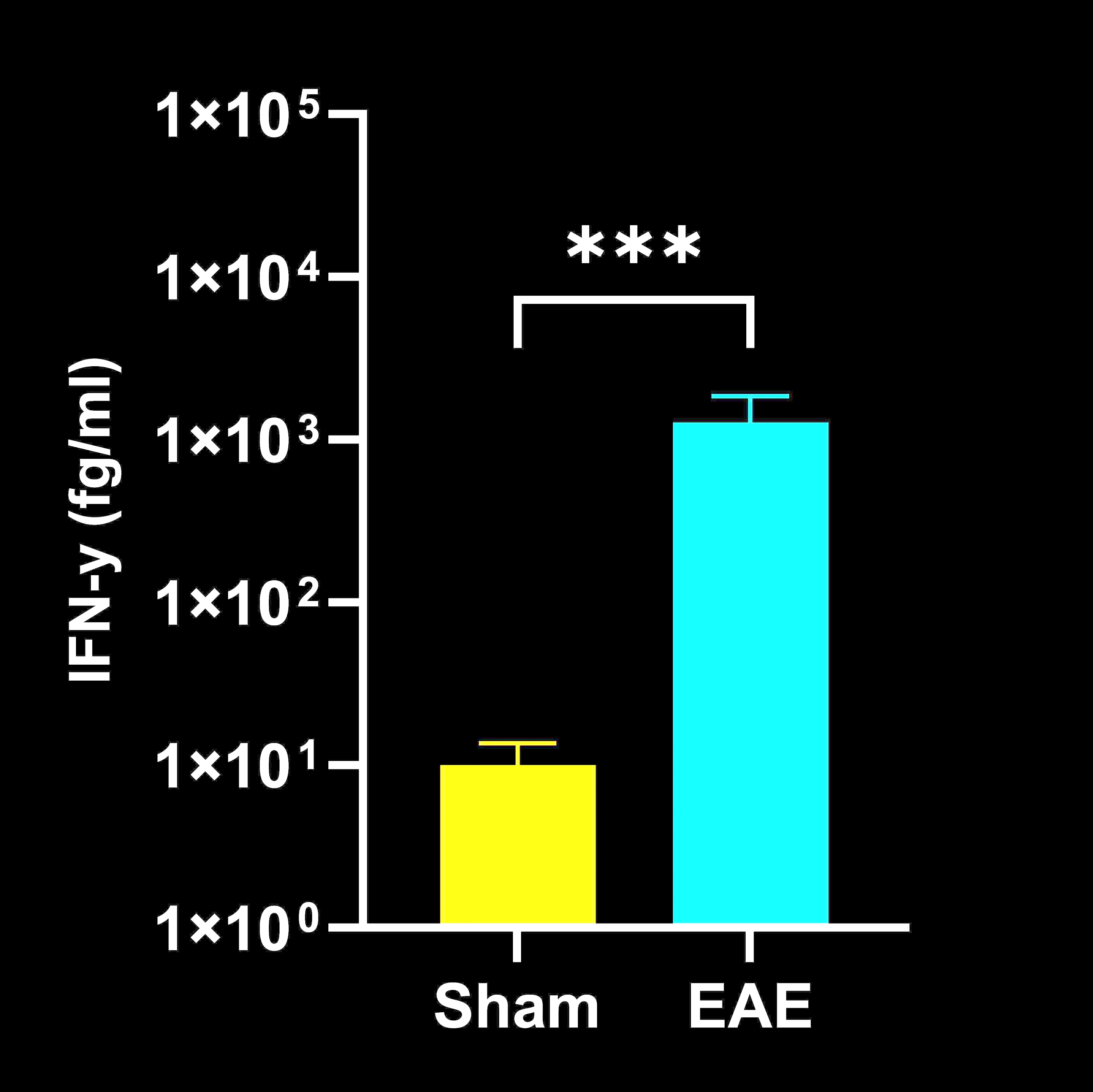
CSFではIL-2とTNF-αが有意に上昇し、脊髄ホモジネートではIFN-γ、IL-1β、IL-2、IL-6、TNF-αが上昇した。これらの所見は、EAEにおける炎症性サイトカインの発現増加は、測定された21日目のエンドポイントでは、大部分が中枢神経系に限局していることを示している。我々の観察結果は、脊髄組織ではサイトカインレベルが上昇するが血清では上昇しないこと(Alassiri, 2023)、および血漿サイトカインに選択的な変化がみられ、ピークに達したサイトカインがその後経時的に減少すること(Borjini, 2016)を示した以前の報告と一致している。この直接的で複数の生物学的マトリックスによるサイトカイン解析は、EAEにおいて一般的に報告されている臨床的・病理学的所見を補完する視点を提供する。
当社の体液・細胞バイオマーカーソリューションの概要については、こちらをご覧ください: 体液・細胞バイオマーカー
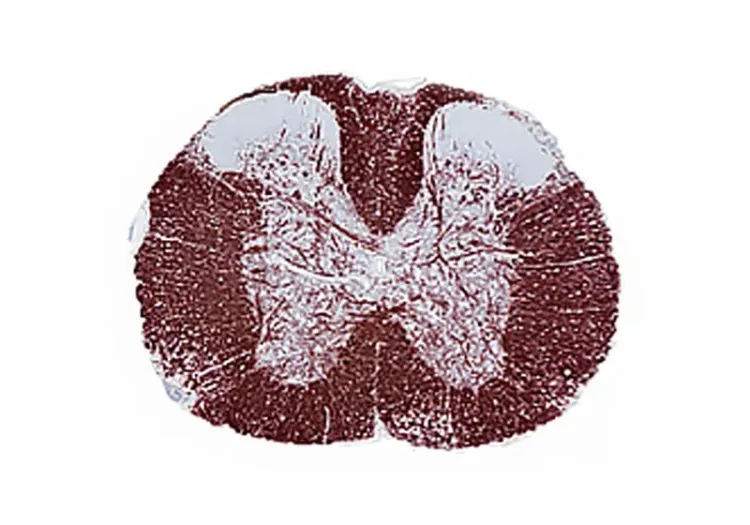
下の "Image Interactive "では、EAE モデル マウスとコントロールマウスの脊髄の高解像度Multiplex免疫蛍光組織切片を含むミクログリア-ニューロン相互作用に関する結果を見ることができる。
インタラクティブ・ビューアの使い方
左側のパネルまたは画面上の矢印で「Image Story」をナビゲートします。高解像度の顕微鏡画像をマウスでパンしたり、スクロールホイールや+/-コントロールを使ってズームイン/ズームアウトすることができます。コントロールパネル(右上)では、画像チャンネルとセグメンテーションオーバーレイを切り替えることができます。最高の体験を得るためには、フルスクリーンモードに切り替えることをお勧めします。 このインタラクティブプレゼンテーションでは、顕微鏡を直接覗き込むように、モデルの神経病理学と関連する機能障害を詳細に調べることができます。
EAEモデルマウスの血漿、髄液、脊髄ホモジネートを用いた超高感度ELISAによるサイトカイン 解析と、高解像度マルチプレックス免疫蛍光法による脊髄組織切片の画像。
クリックしてリンクをコピー
実験的自己免疫性脳脊髄炎(EAE)におけるサイトカインの役割とは?
多発性硬化症:臨床的および病理学的特徴
多発性硬化症(MS)は中枢神経系(CNS)の慢性神経変性自己免疫疾患であり、脱髄とオリゴデンドロサイトの消失を特徴とする。MSは通常、再発寛解型MS(RRMS)、一次進行型MS(PPMS)、二次進行型MS(SPMS)、進行性再発型MS(PRMS)の4つの臨床経過をたどる。患者の約85%は最初にRRMSを呈し、神経機能障害の再発に続いて部分寛解または完全寛解が起こる。症状はさまざまで、歩行障害、視覚障害、認知障害などがある。
我々のEAEモデルマウスにおけるTリンパ球(CD3、赤)。
EAEモデルマウスの脊髄におけるTリンパ球(CD3、赤)の高倍率画像。
MSにおけるT細胞の役割
MS病態の特徴は、自己反応性Tリンパ球、特にCD4+Tヘルパー(Th)細胞サブセットのCNSへの浸潤である。一旦動員されると、Th細胞は炎症性サイトカインとケモカインを分泌し、免疫細胞の動員を促進し、常在グリア細胞を活性化し、血液脳関門(BBB)の破壊、脱髄、軸索喪失の一因となる(Heng, 2022)。
Thサブセットのうち、Th1細胞とTh17細胞が大きく関与している。Th1細胞は主にIL-12とIFN-γの影響下で分化し、マクロファージの活性化と細胞媒介性の炎症を促進する。Th17細胞はIL-6やTGF-βなどのサイトカインの存在下で生じ、IL-17AやGM-CSFを分泌する。
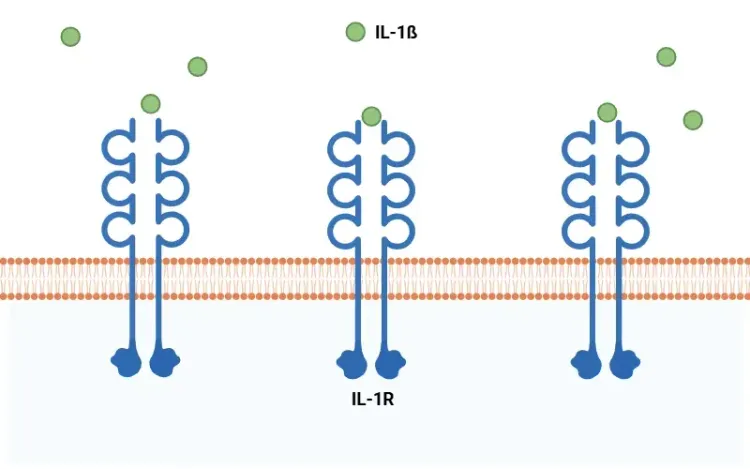
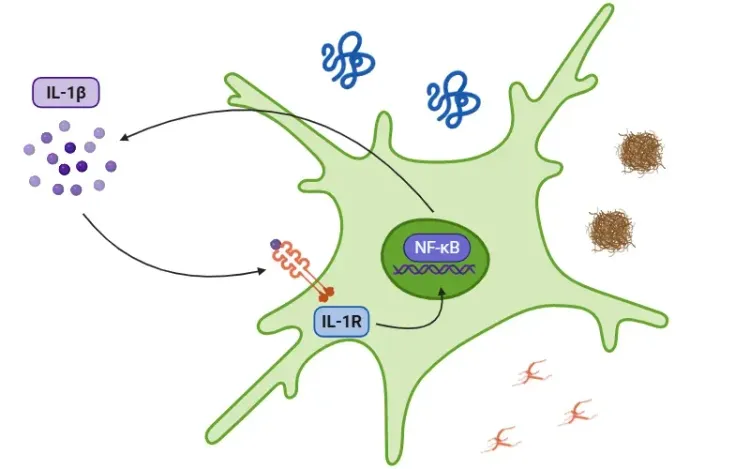
IL-17AはMSの病態と強く関連している。IL-17レセプターを介したシグナル伝達はNF-κBを活性化し、さらなる炎症性サイトカイン産生(IL-1βを含む)を誘導し、炎症部位への好中球や単球の動員を持続させる(Heng, 2022)。
リソースを参照: NF-κB(核内因子κB)とは?
グリア細胞とNLRP3インフラムソーム
中枢神経系に常在するグリア細胞は、浸潤T細胞によって引き起こされる炎症反応を増幅する。アストロサイトはMSの免疫病理学に重要な役割を果たしており、Th細胞由来のサイトカインに反応し、神経炎症を増幅させ、組織損傷を悪化させる反応性表現型をとる(Kunkl, 2022)。反応性アストロサイトはさらにBBBを悪化させ、脱髄と軸索傷害の一因となる。マクロファージ/ミクログリアも活性化され、炎症性メディエーターを放出し、局所免疫反応を維持し、病変の進展を促進する。
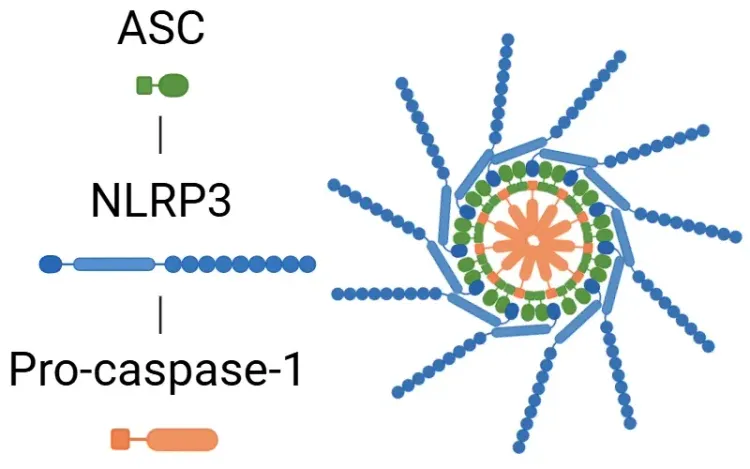
さらに、NLRP3インフラマソームの活性化は、MSにおける重要な自然免疫機構である。NLRP3インフラマソームは、NLRP3センサータンパク質、ASCアダプター、カスパーゼ-1からなる多タンパク質複合体である。活性化されると、パイロプトーシスとIL-1βとIL-18の放出を引き起こし、神経炎症と神経細胞障害を促進する(Xu, 2025)。このプロセスと一致して、IL-1βレベルはMSとEAEモデルの両方で上昇している(Borjini, 2016;Malhotra, 2020;Boraschi, 2023)。
詳細はこちらをご覧ください:
我々のEAEマウスモデルで神経炎症を示すアストロサイト(GFAP、紫)。
我々のEAEモデルマウスにおける神経炎症を示すマクロファージ/ミクログリア(Iba-1、オレンジ色)。
MSにおけるサイトカインとケモカイン
サイトカインとケモカインは、MSにおける免疫主導性の組織損傷の中心的メディエーターである。ケモカインはCNSへの白血球の動員を制御し、それによって炎症と脱髄を促進する(Arimitsu, 2025)。腫瘍壊死因子α(TNF-α)はMSにおける主要な炎症性サイトカインであり、患者の脳脊髄液(CSF)や動物モデルで上昇している(Borjini, 2016;Zahid, 2021)。TNF-αは、MS病変とEAE病変の両方で最も顕著なサイトカインの一つである(Maguire, 2021)。TNF-αは二次的な神経細胞や軸索の損傷に寄与するが、異なる受容体経路(例えば TNFR2経由とTNFR1経由)を介して、状況に依存した防御効果を発揮することもある。
炎症性因子以外にも、免疫調節性サイトカインもMSの進行に影響を及ぼす。例えば、IL-2やTGF-βは、ナイーブT細胞から制御性T(Treg)細胞への分化を促し、抑制性サイトカイン放出やその他の機序によって免疫寛容を維持する。炎症性Th17細胞と抗炎症性Treg細胞の不均衡が、疾患発症に関与している(Zhang, 2021)。MS病変は最終的に、浸潤TおよびBリンパ球、活性化マクロファージ/ミクログリア、および慢性炎症、脱髄、神経軸変性を促進する複雑なサイトカイン環境によって特徴づけられる。
MSのモデルとしての実験的自己免疫性脳脊髄炎
実験的自己免疫性脳脊髄炎(EAE)はMSの標準的な動物モデルであり、ヒトの疾患の多くの病理学的特徴を再現している。MSの病態の中心であるサイトカイン駆動性の脱髄と神経変性もまた、EAEの重要な特徴である。例えば、IL-6はEAEマウスの脳で増加している(Leuti, 2021;Marin-Prida, 2022)。ミエリンオリゴデンドロサイト糖タンパク質(MOG)35-55で誘導されたマウスのEAEは広く用いられており、中枢神経系免疫細胞の浸潤や、モデルによっては再発性あるいは慢性進行性の疾患経過など、MSの本質的な側面を反映している。
しかし、多くのEAE研究が臨床的、病理組織学的、および/または遺伝子発現の読み取りに焦点をあてている一方で、高感度マルチプレックスイムノアッセイを用いて、マッチングした組織や生体流体中のサイトカイン濃度を直接定量したものは比較的少ない。このデータの欠如は、従来のEAEエンドポイントを補完するものとして、複数の生物学的マトリックスサイトカインプロファイリングの重要性を強調している。
EAEの誘発は後肢麻痺と神経炎を引き起こし、CSF、血液、脊髄を含む複数の生体マトリックスにわたってサイトカインレベルが定量可能である。
脊髄ホモジネート中のサイトカイン濃度
脊髄ホモジネート中のサイトカイン濃度(EAEマウスとShamマウス(コントロール)の比較);平均値±SEM、*** p<0.001; **** p<0.0001.
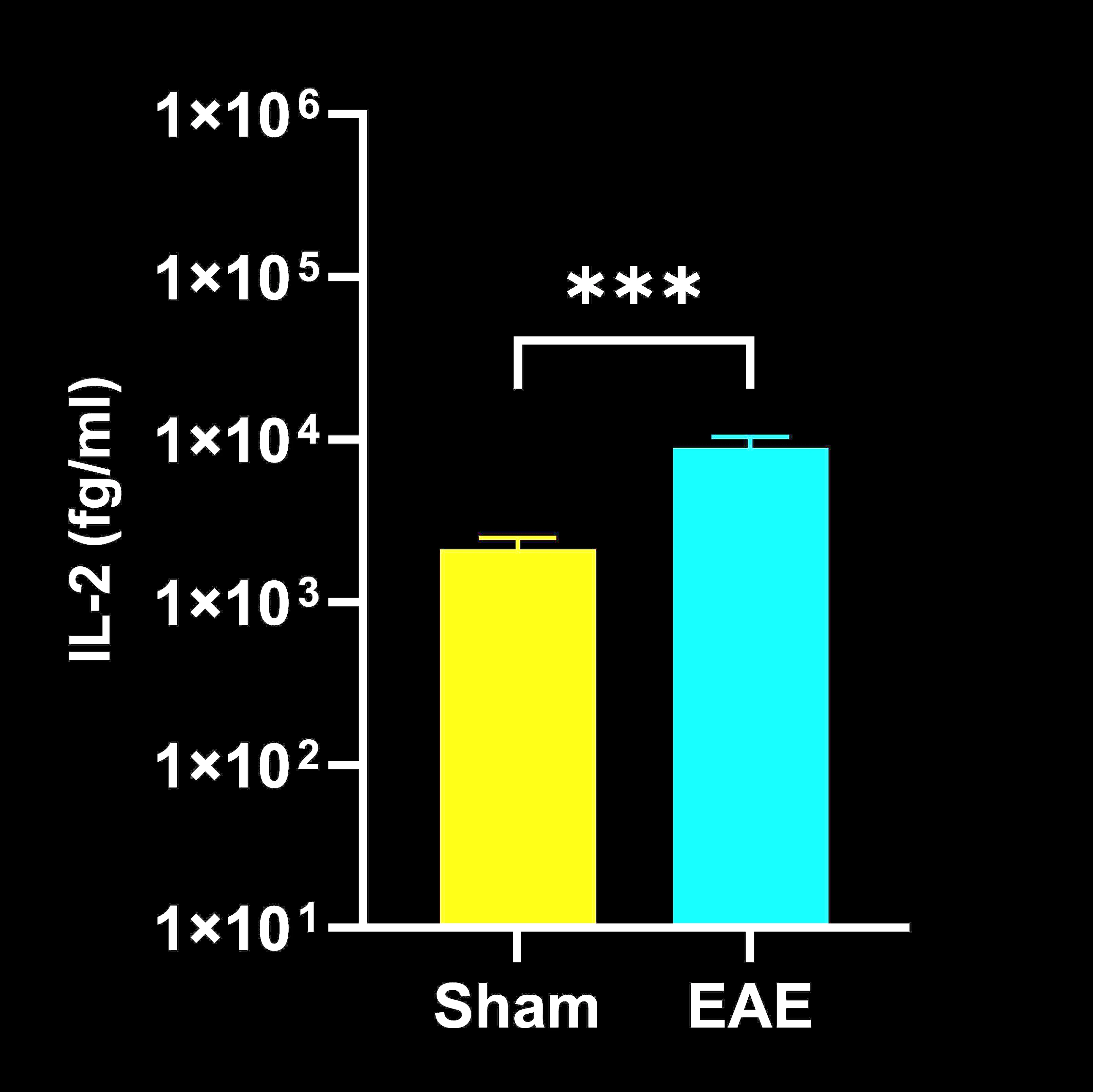
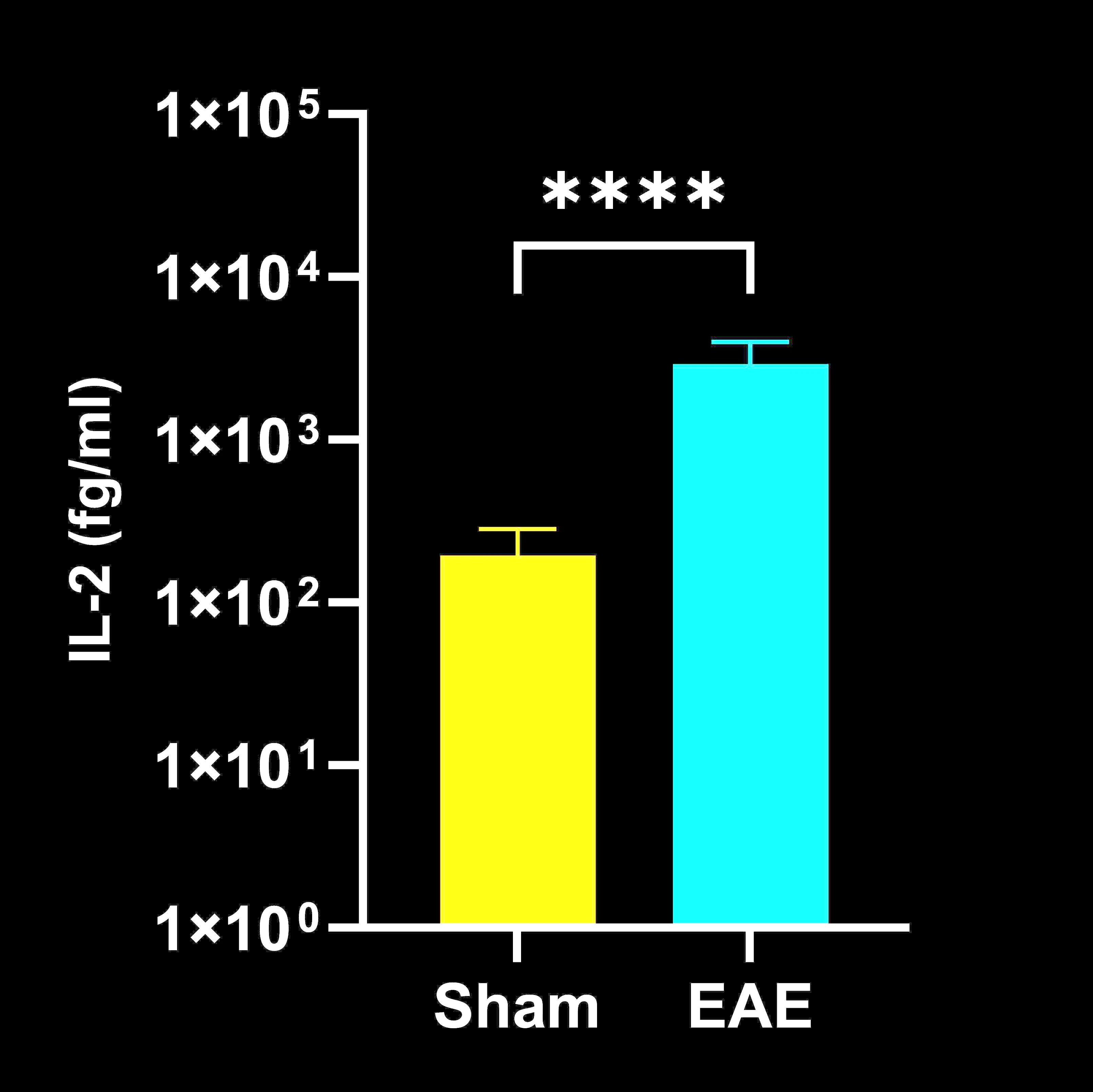
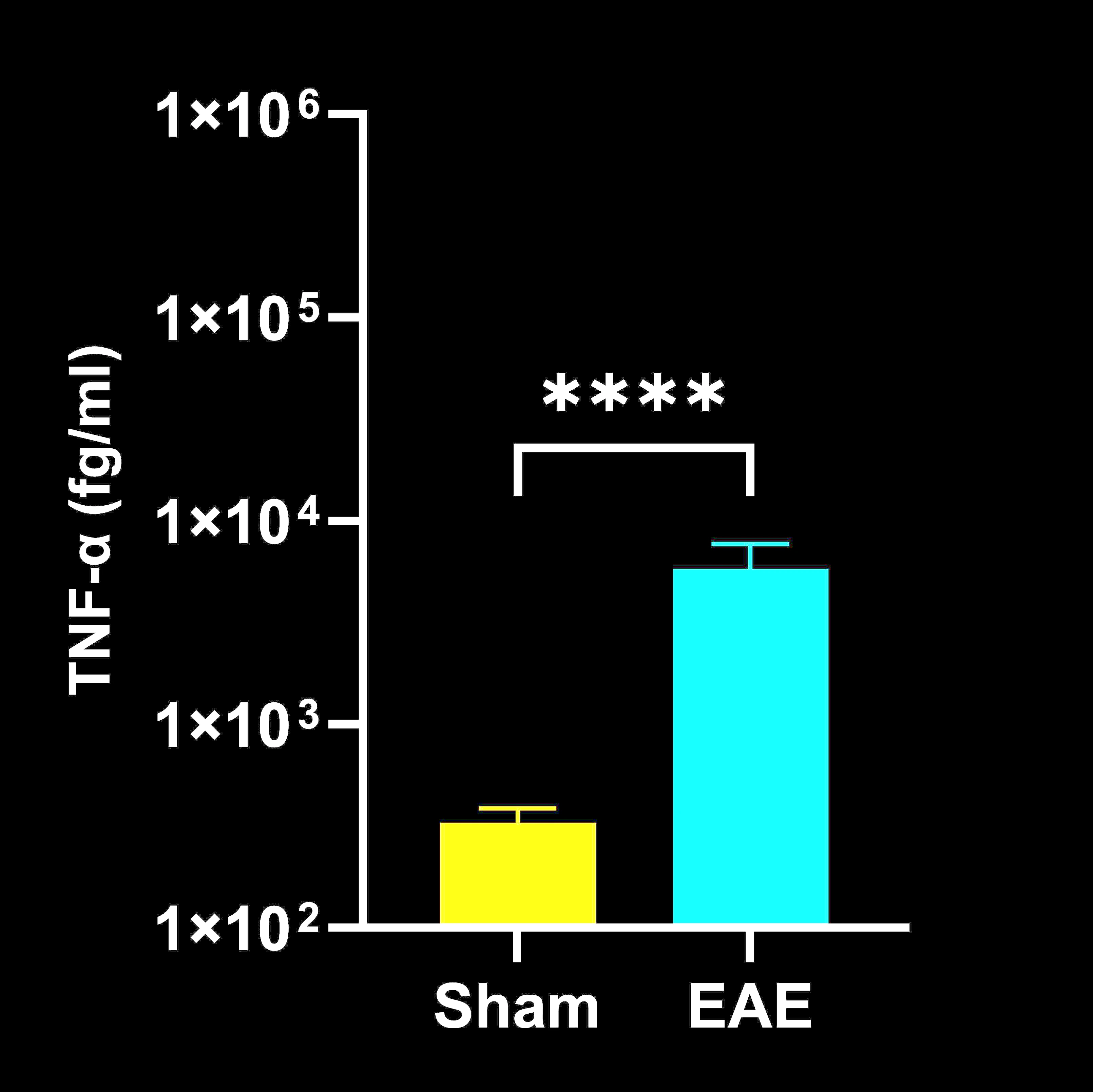
脳脊髄液(CSF)中のサイトカイン濃度
EAEマウスとSham(コントロール)マウスのCSFサイトカイン終末濃度;平均値±SEM、*** p<0.001。
血漿中のサイトカイン濃度
EAEマウスとSham(対照)マウスの終末血漿中サイトカイン濃度;平均±SEM。
よくあるご質問
当社の神経変性疾患モデルについて詳しく見る
関連コンテンツ
サイトカイン解析と神経炎症に関する最新情報、および神経変性疾患の動物モデルにおける治療薬の評価に関するベストプラクティス。
EAE(実験的自己免疫性脳脊髄炎)とは何でしょうか?
多発性硬化症(MS)のEAE動物モデルに関する概説:病態生理学および前臨床治療研究における陽性対照の利用を含みます。
実験的自己免疫性脳脊髄炎(EAE)および軸索損傷
この資料では、多発性硬化症(MS)のEAEモデルにおける軸索損傷および軸索変性の測定方法について説明しています。組織マーカーや血漿およびCSF中のニューロフィラメント軽鎖(NfL;NF-L)レベルなど、利用可能な測定方法を説明しています。
IL-1βとは何ですか?
IL-1βの概要、全身性疾患および神経疾患におけるその炎症誘発作用、ならびにIL-1β拮抗作用を基盤とした治療戦略について概説します。
インターロイキン-1ベータ(IL-1β)と神経変性疾患
アルツハイマー病(AD)、パーキンソン病(PD)、筋萎縮性側索硬化症(ALS)などの神経変性疾患におけるIL-1βの役割。
神経変性疾患におけるTNF-αとミクログリア
ミクログリアにおける腫瘍壊死因子-α(TNF-α)の機能と、神経変性進行への寄与についての概要。
神経変性疾患におけるTNF-αとアストロサイト
アストロサイトにおけるTNF-αシグナル伝達の概要、神経変性におけるその役割、およびこの経路を標的とする治療戦略について。
NLRP3とは何ですか?
NLRP3およびNLRP3炎症小体活性化トリガー、疾患関連、および治療的標的戦略の概要。
NLRP3インフラマソームと神経変性疾患
NLRP3インフラマソームの概要と、アルツハイマー病、パーキンソン病、ALSなどの神経変性疾患におけるその役割について。