Neuroinflammation dans le modèle de souris EAE : analyse du mIF et des cytokines
Table des matières
- Présentation interactive de notre étude
- Quel est le rôle des cytokines dans l'encéphalomyélite auto-immune expérimentale (EAE) ?
- Concentrations de cytokines dans les homogénats de moelle épinière
- Concentrations de cytokines dans le liquide céphalo-rachidien (LCR)
- Concentrations de cytokines dans le plasma
Présentation interactive de notre étude
Résumé de l'étude : profilage des cytokines dans l'EAE
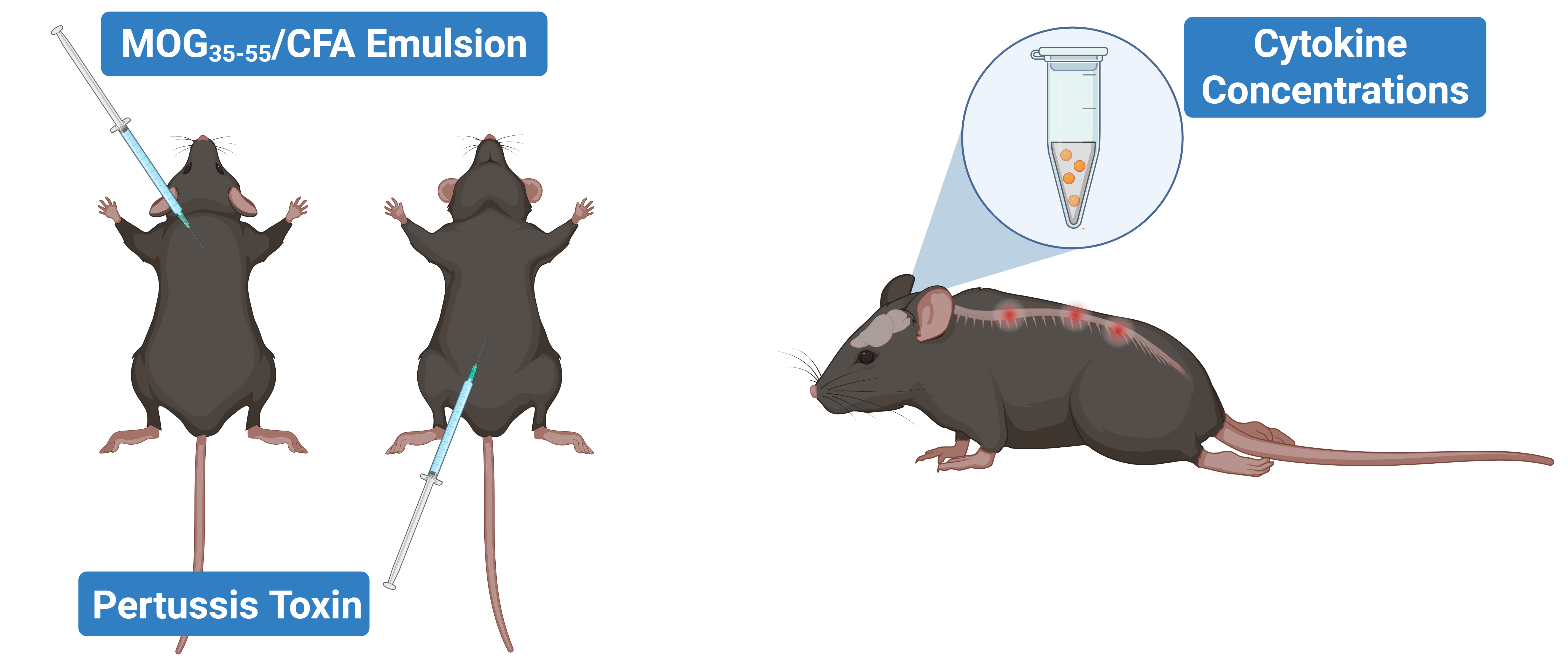
Nous avons mesuré directement les niveaux de protéines des cytokines dans plusieurs matrices (tissus et fluides du SNC) dans l'EAE afin de saisir un aspect de la réponse immunitaire qui est souvent déduit, mais moins souvent quantifié au niveau des protéines. Nous avons induit l'EAE chez des souris en utilisant du MOG35-55 dans l'adjuvant complet de Freund (CFA) avec de la toxine de coqueluche, et la maladie a été évaluée 21 jours après l'immunisation. Les niveaux de cytokines (IL-1β, TNF-α, IFN-γ, IL-6, IL-10, IL-4, IL-2, IL-5 et la chimiokine KC/GRO) ont été quantifiés par un dosage immunologique multiplex à ultra-haute sensibilité dans le plasma terminal, le LCR et les homogénats de moelle épinière.
L'IL-2 et le TNF-α étaient significativement élevés dans le LCR, tandis que l'IFN-γ, l'IL-1β, l'IL-2, l'IL-6 et le TNF-α augmentaient dans les homogénats de moelle épinière ; aucune différence significative n'a été détectée dans le plasma. Ces résultats indiquent que l'augmentation des cytokines inflammatoires dans l'EAE est largement confinée au SNC à l'issue des 21 jours mesurés. Nos observations sont cohérentes avec des rapports antérieurs démontrant une augmentation des niveaux de cytokines dans le tissu de la moelle épinière, mais pas dans le sérum(Alassiri, 2023), ainsi que des changements sélectifs dans les cytokines plasmatiques, où certains atteignent un pic et diminuent ensuite au fil du temps(Borjini, 2016). Cette analyse directe des cytokines de matrices biologiques multiples offre une perspective complémentaire aux résultats cliniques et pathologiques plus communément rapportés dans l'EAE.
Pour une vue d'ensemble de nos solutions en matière de biomarqueurs liquides et cellulaires, voir : Biomarqueurs fluides et cellulaires
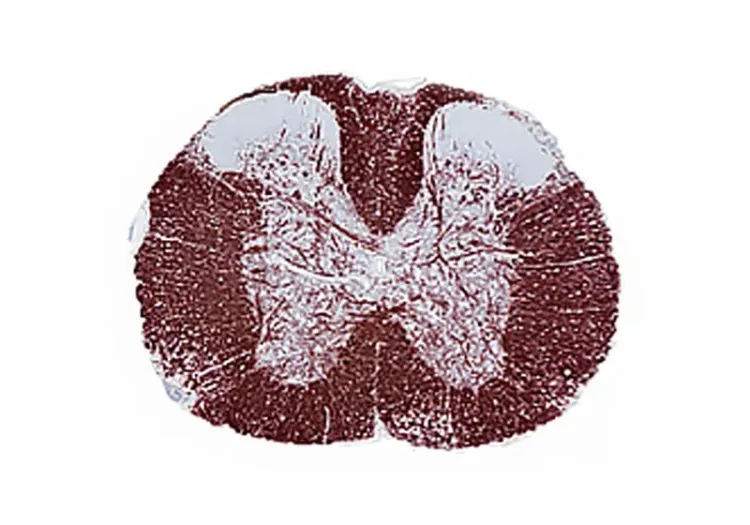
Dans l'"Image Interactive" ci-dessous, vous trouverez des résultats sur les interactions entre la microglie et les neurones, y compris des coupes de tissus par immunofluorescence multiplex à haute résolution de moelles épinières provenant du modèle de sourisEAE et de souris témoins.
Comment utiliser notre visionneuse interactive
Naviguez dans l'"histoire de l'image" à l'aide du panneau de gauche ou des flèches à l'écran. Vous pouvez effectuer un panoramique sur les images de microscopie à haute résolution à l'aide de votre souris, et faire un zoom avant/arrière à l'aide de la molette de défilement ou des commandes +/-. Le panneau de contrôle (en haut à droite) permet de basculer entre les canaux d'images et les superpositions de segmentation. Pour une expérience optimale, nous vous recommandons de passer en mode plein écran. Cette présentation interactive vous permet d'explorer en détail la neuropathologie du modèle et les déficits fonctionnels qui y sont associés, comme si vous regardiez directement au microscope.
Image interactive décrivant l'analyse des cytokines quantifiées par ELISA ultra-haute sensibilité dans le plasma terminal, le LCR et les homogénats de moelle épinière, ainsi que les coupes de tissu de moelle épinière en immunofluorescence multiplex à haute résolution du modèle de souris EAE.
Cliquez pour copier le lien
Quel est le rôle des cytokines dans l'encéphalomyélite auto-immune expérimentale (EAE) ?
La sclérose en plaques : Caractéristiques cliniques et pathologiques
La sclérose en plaques (SEP) est une maladie auto-immune neurodégénérative chronique du système nerveux central (SNC), caractérisée par une démyélinisation et une perte d'oligodendrocytes. La SEP suit généralement quatre évolutions cliniques : la SEP récurrente-rémittente (RRMS), la SEP primaire progressive (PPMS), la SEP secondaire progressive (SPMS) et la SEP progressive-rémittente (PRMS). Environ 85 % des patients présentent initialement une SEP-RR, dans laquelle les rechutes de dysfonctionnement neurologique sont suivies d'une rémission partielle ou complète. Les symptômes varient considérablement et peuvent inclure des troubles de la marche, des déficiences visuelles et des déficits cognitifs.
Lymphocytes T (CD3, rouge) dans notre modèle de souris EAE.
Vue à fort grossissement des lymphocytes T (CD3, rouge) dans la moelle épinière de notre modèle de souris EAE.
Rôle des cellules T dans la SEP
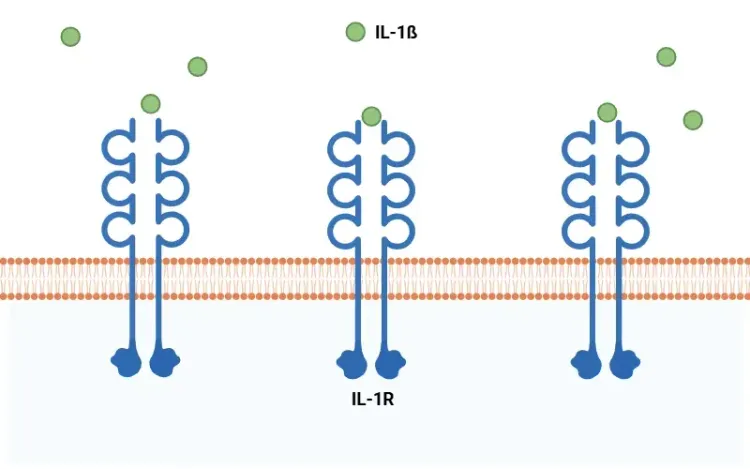
L'infiltration dans le SNC de lymphocytes T autoréactifs, en particulier de sous-ensembles de cellules T helper (Th) CD4+, est l'une des caractéristiques de la pathologie de la SEP. Une fois recrutées, les cellules Th sécrètent des cytokines et des chimiokines pro-inflammatoires qui favorisent le recrutement de cellules immunitaires, activent les cellules gliales résidentes et contribuent à la rupture de la barrière hémato-encéphalique (BHE), à la démyélinisation et à la perte axonale(Heng, 2022).
Parmi les sous-ensembles Th, les cellules Th1 et Th17 sont particulièrement impliquées. Les cellules Th1 se différencient principalement sous l'influence de l'IL-12 et de l'IFN-γ et conduisent à l'activation des macrophages et à l'inflammation à médiation cellulaire. Les cellules Th17 apparaissent en présence de cytokines telles que l'IL-6 et le TGF-β et sécrètent l'IL-17A et le GM-CSF.
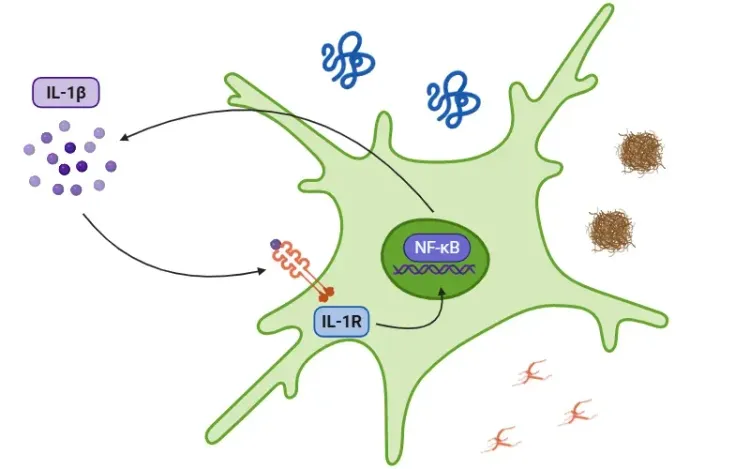
L'IL-17A est étroitement liée à la pathogenèse de la SEP ; la signalisation par le récepteur de l'IL-17 active NF-κB, induisant une production supplémentaire de cytokines pro-inflammatoires (y compris l'IL-1β) et soutenant le recrutement de neutrophiles et de monocytes dans les sites inflammatoires(Heng, 2022).
Voir notre ressource : Qu'est-ce que le NF-κB (facteur nucléaire Kappa B) ?
Cellules gliales et inflammasome NLRP3
Les cellules gliales résidant dans le SNC amplifient la réponse inflammatoire déclenchée par les cellules T infiltrantes. Les astrocytes jouent un rôle clé dans l'immunopathologie de la SEP et répondent aux cytokines dérivées des cellules Th en adoptant un phénotype réactif qui amplifie la neuroinflammation et exacerbe les lésions tissulaires(Kunkl, 2022). Les astrocytes réactifs compromettent davantage la BHE et contribuent à la démyélinisation et aux lésions axonales. Les macrophages/microglies sont également activés et libèrent des médiateurs inflammatoires qui entretiennent les réponses immunitaires locales et favorisent le développement des lésions.
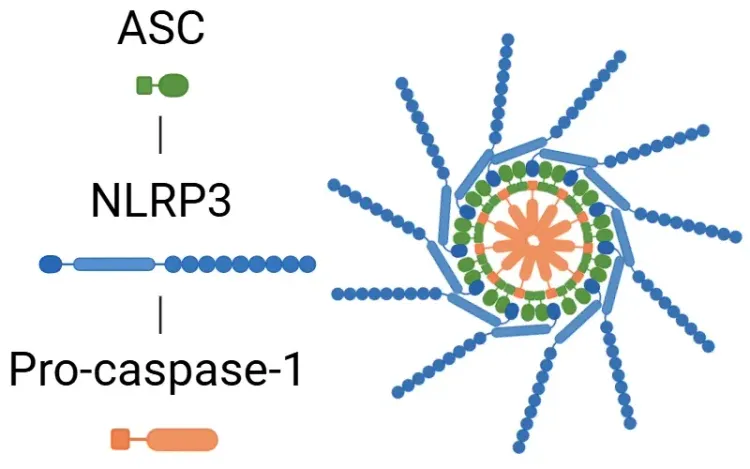
En outre, l'activation de l'inflammasome NLRP3 représente un mécanisme immunitaire inné important dans la SEP. L'inflammasome NLRP3 est un complexe multiprotéique comprenant la protéine senseur NLRP3, l'adaptateur ASC et la caspase-1. Lorsqu'il est activé, il déclenche la pyroptose et la libération d'IL-1β et d'IL-18, favorisant ainsi la neuroinflammation et les lésions neuronales(Xu, 2025). Conformément à ce processus, les niveaux d'IL-1β sont élevés à la fois dans la SEP et dans le modèle EAE(Borjini, 2016; Malhotra, 2020; Boraschi, 2023).
Pour plus d'informations, consultez le site:
Astrocytes (GFAP, violet) démontrant une neuroinflammation dans notre modèle de souris EAE.
Macrophages/microglies (Iba-1, orange) démontrant une neuroinflammation dans notre modèle de souris EAE.
Cytokines et chimiokines dans la SEP
Les cytokines et les chimiokines sont des médiateurs centraux des lésions tissulaires d'origine immunitaire dans la SEP. Les chimiokines régulent le recrutement des leucocytes dans le SNC, favorisant ainsi l'inflammation et la démyélinisation(Arimitsu, 2025). Le facteur de nécrose tumorale alpha (TNF-α) est une cytokine pro-inflammatoire majeure dans la SEP, élevée dans le liquide céphalo-rachidien (LCR) des patients et dans les modèles animaux(Borjini, 2016; Zahid, 2021). C'est l'une des cytokines les plus présentes dans les lésions de SEP et d'EAE(Maguire, 2021). Le TNF-α contribue aux lésions neuronales et axonales secondaires, bien qu'il puisse également exercer des effets protecteurs dépendants du contexte par le biais de voies réceptrices distinctes( parexemple , via TNFR2 par rapport à TNFR1).
Au-delà des facteurs pro-inflammatoires, les cytokines immunorégulatrices influencent également la progression de la SEP. Par exemple, l'IL-2 et le TGF-β entraînent la différenciation des cellules T naïves en cellules T régulatrices (Treg), qui maintiennent la tolérance immunitaire par la libération de cytokines inhibitrices et d'autres mécanismes ; un déséquilibre entre les cellules Th17 pro-inflammatoires et les cellules Treg anti-inflammatoires est impliqué dans la pathogenèse de la maladie(Zhang, 2021). Les lésions de SEP sont finalement caractérisées par des lymphocytes T et B infiltrés, des macrophages/microglies activés et un milieu cytokinique complexe qui entraîne une inflammation chronique, une démyélinisation et une dégénérescence neuroaxonale.
Pour en savoir plus sur le rôle des cytokines dans les maladies neurodégénératives, consultez nos ressources sur : IL-1β & TNF-α
L'encéphalomyélite auto-immune expérimentale comme modèle de la sclérose en plaques
L'encéphalomyélite auto-immune expérimentale (EAE) est un modèle animal de référence de la sclérose en plaques, qui récapitule de nombreuses caractéristiques pathologiques de la maladie humaine. La démyélinisation et la neurodégénérescence induites par les cytokines, qui sont au cœur de la pathologie de la SEP, sont également des caractéristiques clés de l'EAE. Par exemple, l'IL-6 augmente dans le cerveau des souris EAE(Leuti, 2021; Marin-Prida, 2022). L'EAEinduite par la glycoprotéine de l'oligodendrocyte de la myéline (MOG)35-55 chez la souris est largement utilisée et reflète des aspects essentiels de la SEP, notamment l'infiltration des cellules immunitaires du SNC et, selon le modèle, une évolution de la maladie de type récurrente-rémittente ou chronique progressive.
Cependant, alors que de nombreuses études sur l'EAE se concentrent sur les données cliniques, histopathologiques et/ou d'expression génique, peu d'entre elles ont directement quantifié les concentrations de cytokines dans des tissus et des liquides biologiques appariés à l'aide d'immunodosages multiplex très sensibles. Ce manque de données souligne l'importance du profilage des cytokines dans des matrices biologiques multiples en complément des critères d'évaluation traditionnels de l'EAE.
Voir : Qu'est-ce que l'EAE (Encéphalomyélite Auto-immune Expérimentale) & Lésions Axonales & Encéphalomyélite Auto-immune Expérimentale
L'induction de l'EAE entraîne une paralysie des membres postérieurs et une neuroinflammation, avec des niveaux de cytokines quantifiables dans de multiples matrices biologiques, y compris le LCR, le sang et la moelle épinière.
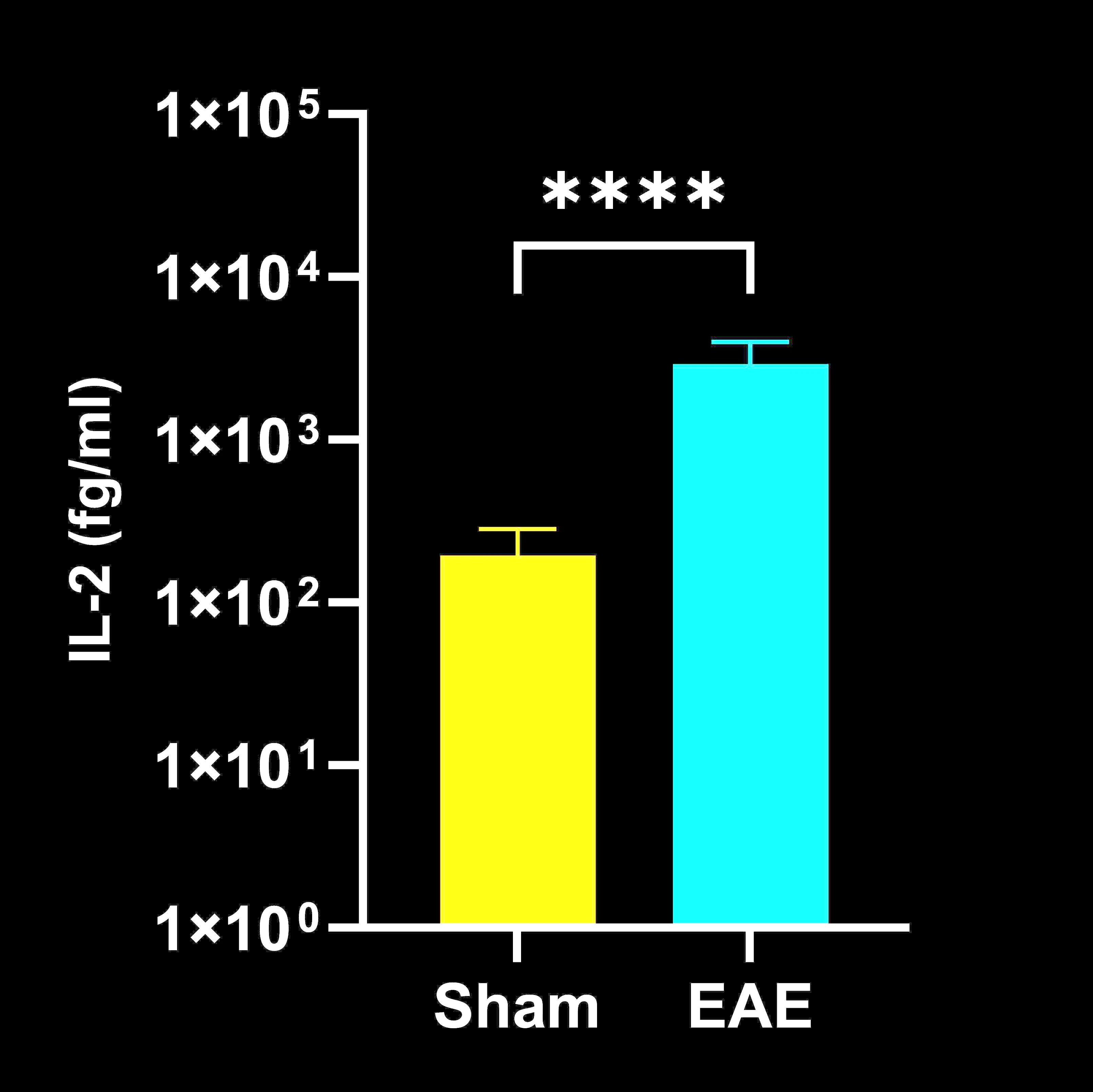
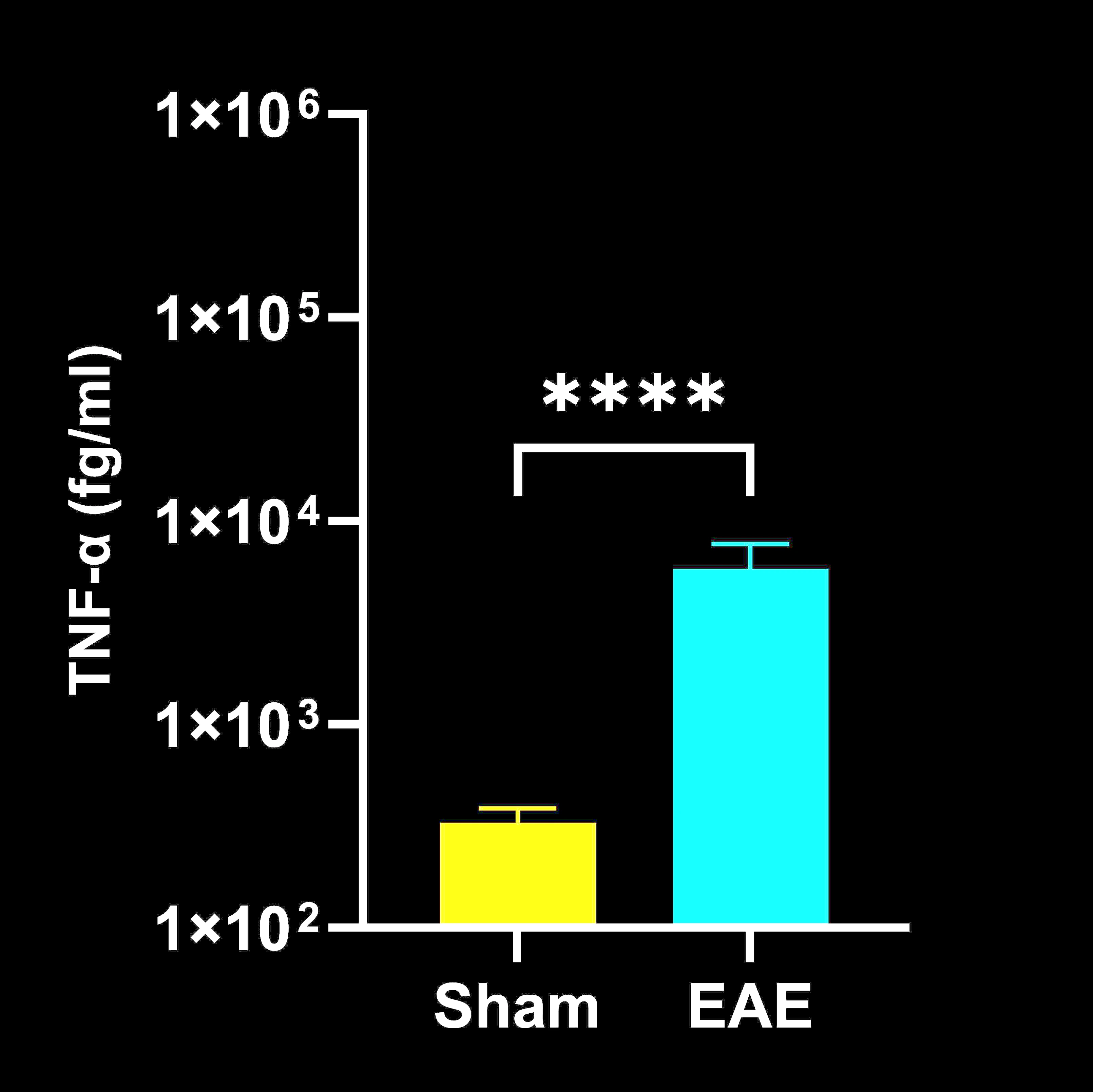
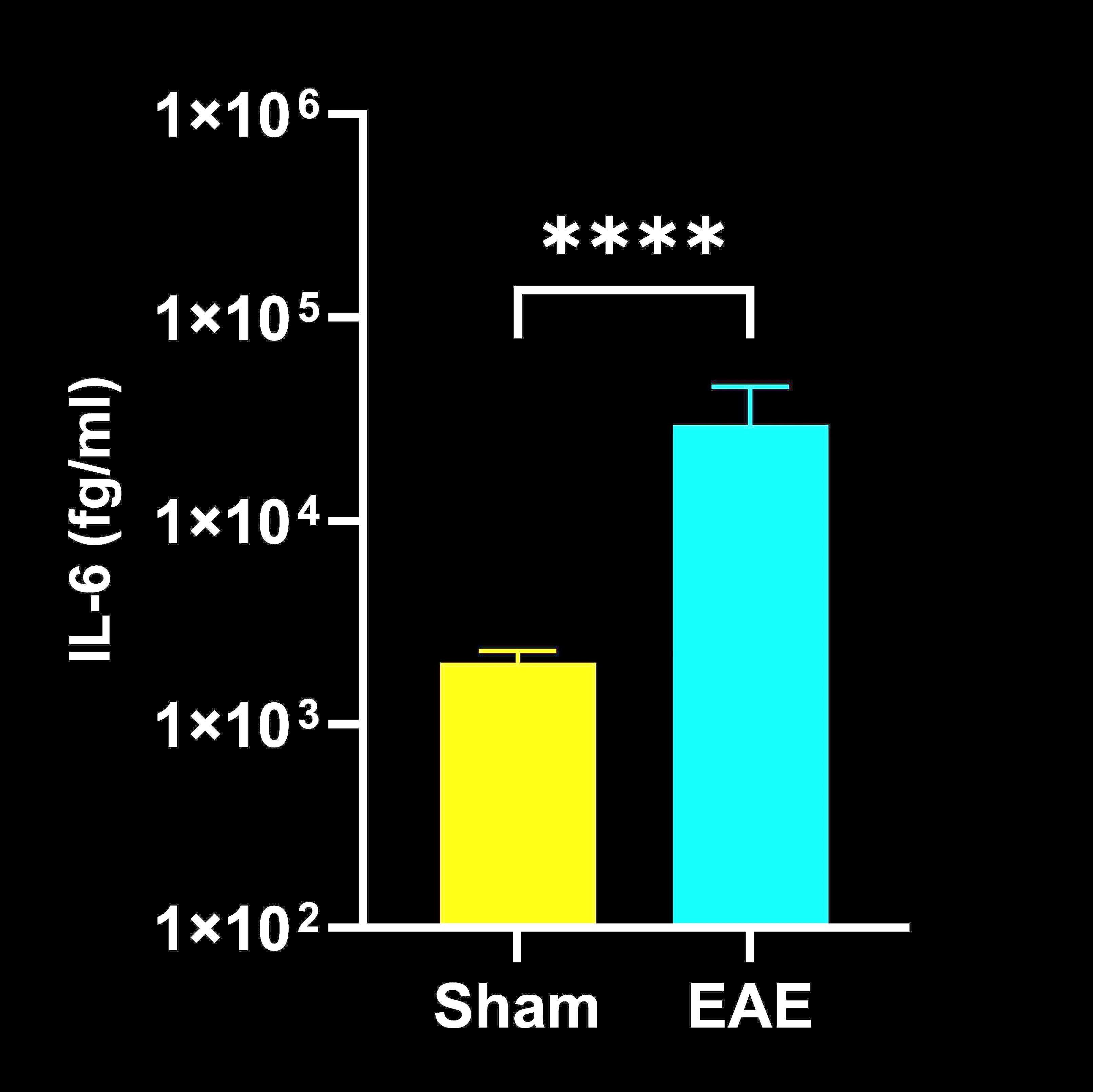
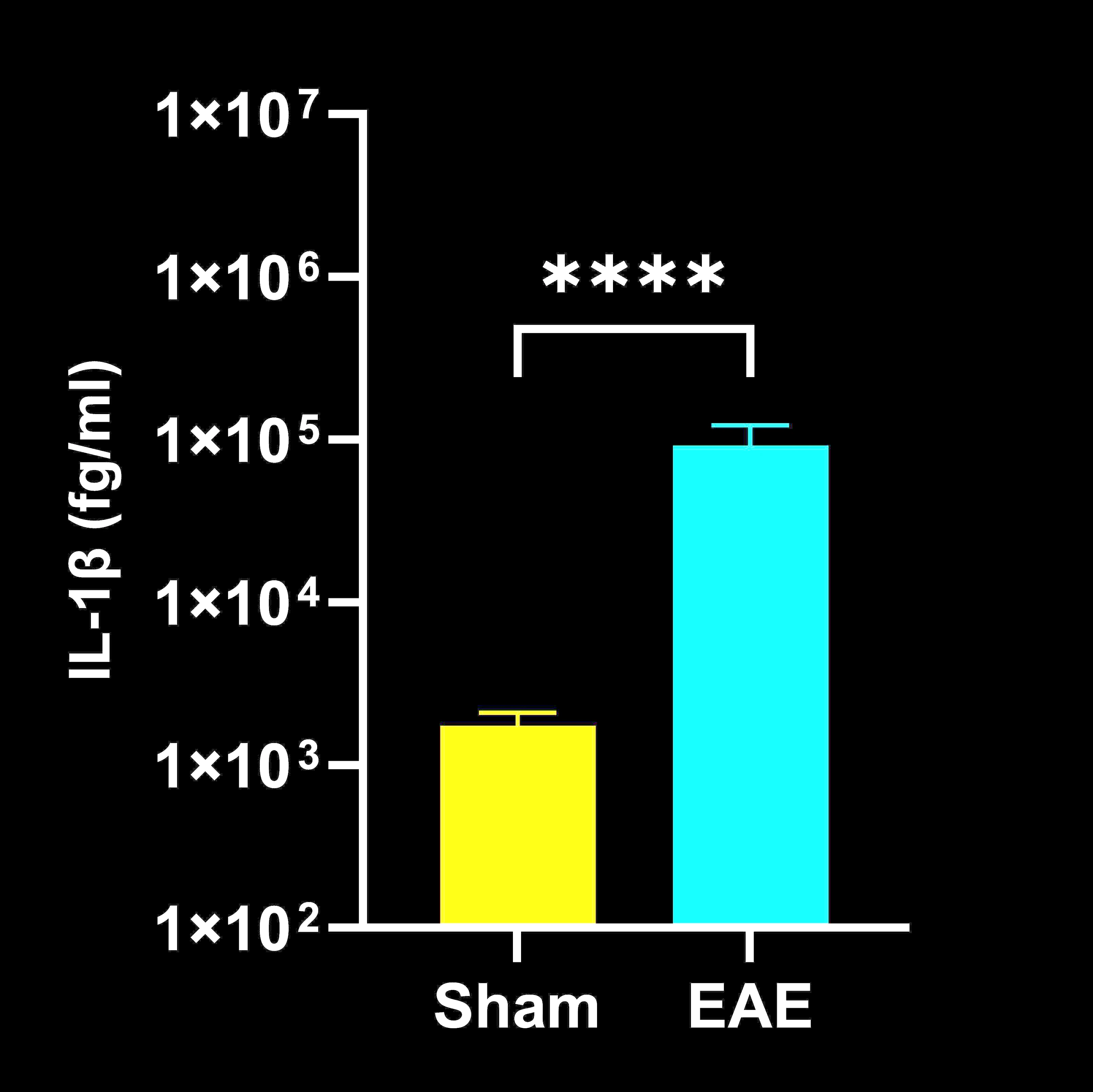
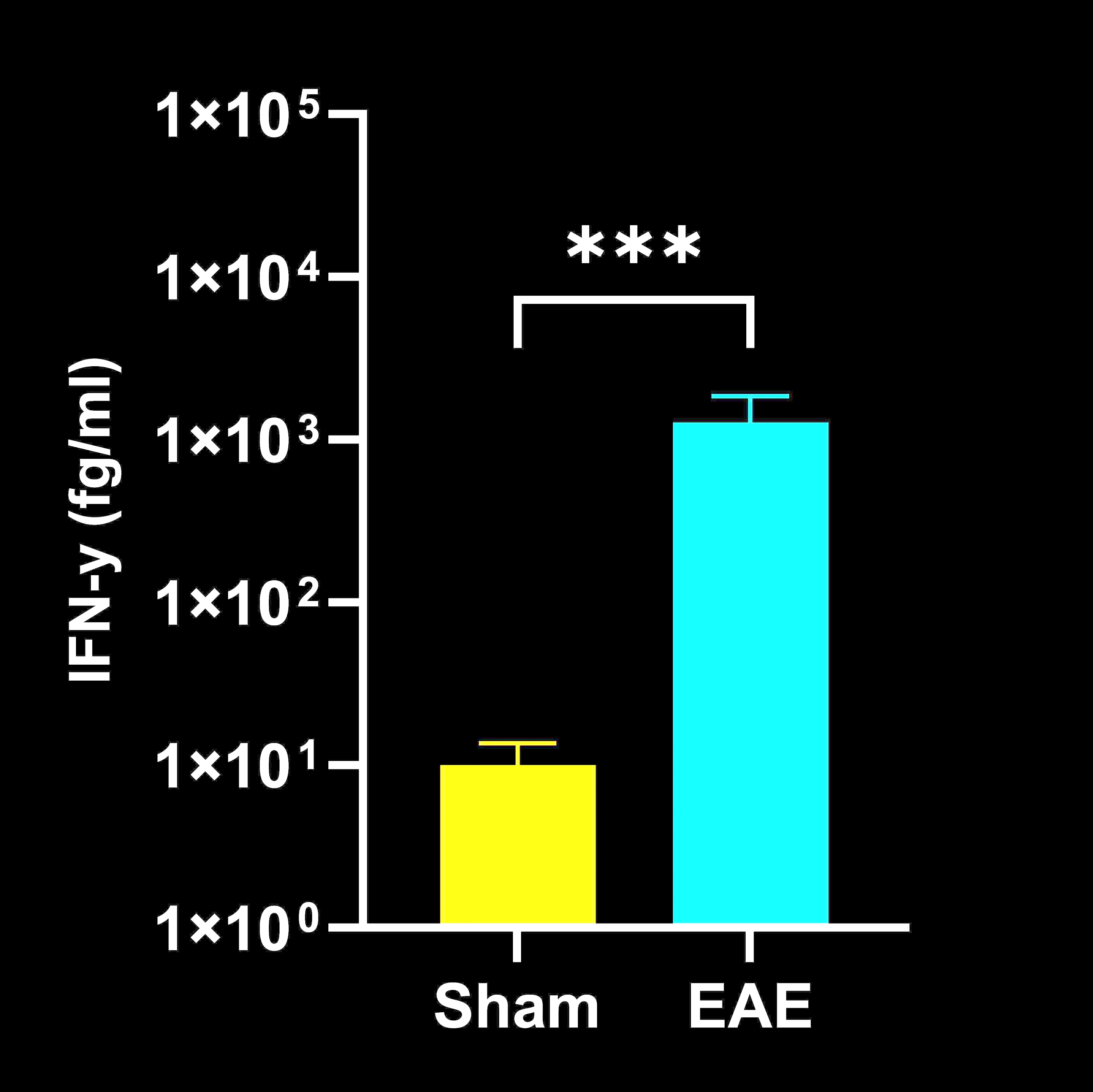
Concentrations de cytokines dans les homogénats de moelle épinière
Concentrations de cytokines dans l'homogénat de moelle épinière chez les souris EAE par rapport aux souris Sham (contrôle) ; moyenne ± SEM, *** p<0,001 ; **** p<0,0001.
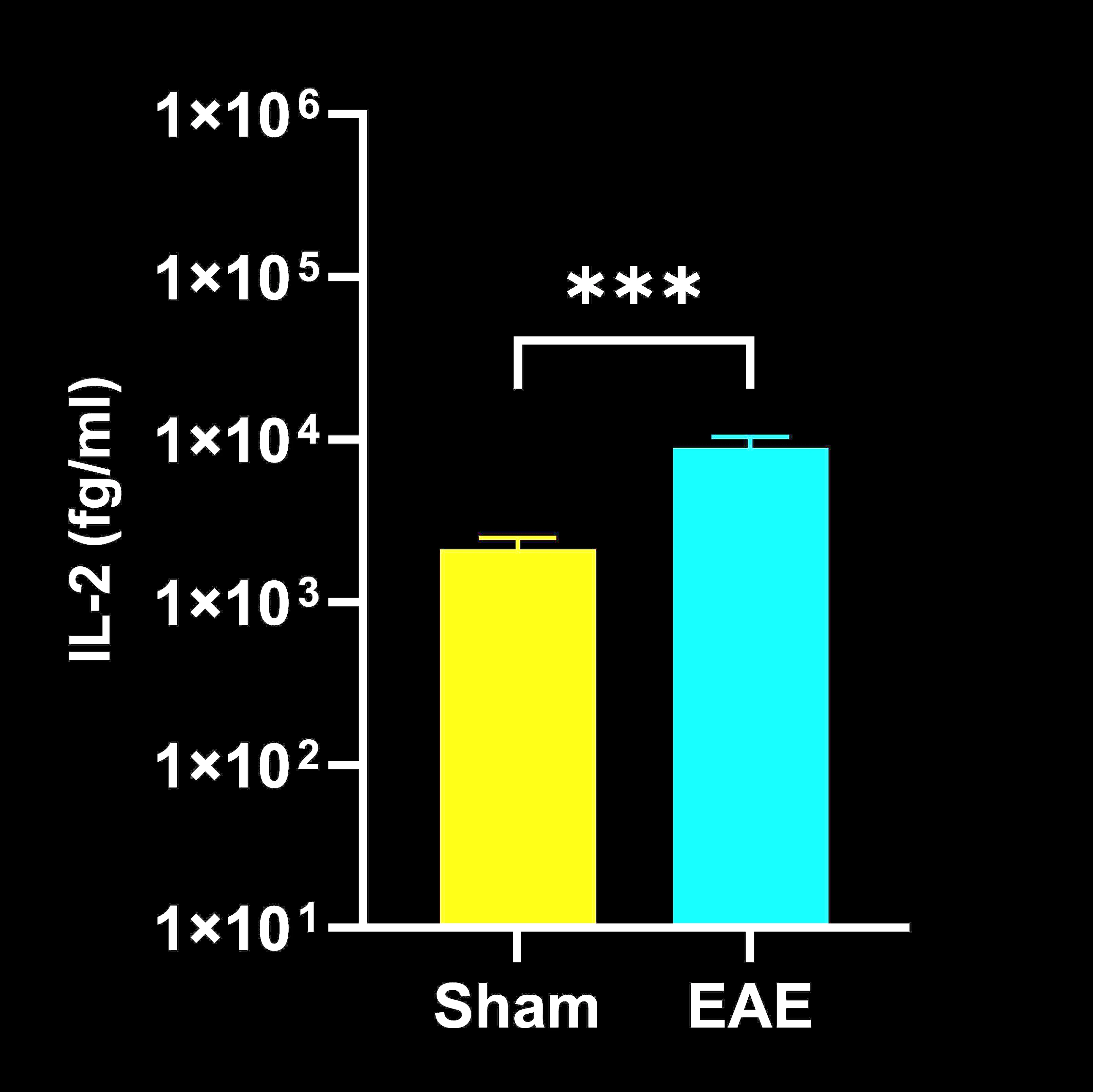
Concentrations de cytokines dans le liquide céphalo-rachidien (LCR)
Concentrations terminales de cytokines dans le LCR chez les souris EAE par rapport aux souris Sham (contrôle) ; moyenne ± SEM, *** p<0,001.
Concentrations de cytokines dans le plasma
Concentrations plasmatiques terminales de cytokines chez les souris EAE par rapport aux souris Sham (contrôle) ; moyenne ± SEM.
FAQ
Découvrez-en davantage sur nos modèles de maladies neurodégénératives
Contenu connexe
Des informations actualisées sur l'analyse des cytokines et la neuroinflammation, ainsi que les meilleures pratiques en matière d'évaluation des agents thérapeutiques dans les modèles animaux de maladies neurodégénératives.
Lésions axonales dans l'encéphalomyélite auto-immune expérimentale (EAE)
Cette ressource décrit les méthodes disponibles pour mesurer les lésions axonales et la dégénérescence des axones, y compris les marqueurs tissulaires et les niveaux de chaîne légère des neurofilaments (NfL ; NF-L) dans le plasma et le LCR, dans le modèle EAE de la sclérose en plaques (SP).
Qu'est-ce que l'EAE (encéphalomyélite auto-immune expérimentale)?
Présentation des modèles animaux EAE de la sclérose en plaques (SEP), y compris la physiopathologie et l'utilisation de contrôles positifs pour les études thérapeutiques précliniques.
Interleukine-1 bêta (IL-1β) et maladies neurodégénératives
Le rôle de l'IL-1bêta dans les maladies neurodégénératives, notamment la maladie d'Alzheimer (MA), la maladie de Parkinson (MP) et la sclérose latérale amyotrophique (SLA).
TNF-α et microglie dans les maladies neurodégénératives
Un aperçu de la fonction du facteur de nécrose tumorale alpha (TNF-α) dans la microglie et de sa contribution à la progression de la neurodégénérescence.
Inflammasome NLRP3 et maladies neurodégénératives
Un aperçu de l'inflammasome NLRP3 et de son rôle dans les maladies neurodégénératives, notamment la maladie d'Alzheimer, la maladie de Parkinson et la SLA.
Qu'est-ce que l'IL-1β?
Présentation générale de l'IL-1β, de son rôle pro-inflammatoire dans les maladies systémiques et neurologiques, et des stratégies thérapeutiques impliquant l'antagonisme de l'IL-1β.
Qu'est-ce que le NLRP3?
Présentation générale du NLRP3 et des déclencheurs de l'activation de l'inflammasome NLRP3, des associations avec des maladies et des stratégies thérapeutiques ciblées.
Le TNF-α et les astrocytes dans les maladies neurodégénératives
Présentation générale de la signalisation du TNF-α dans les astrocytes, de son rôle dans la neurodégénérescence et des stratégies thérapeutiques ciblant cette voie.