シヌクレインモデルの概要
α-シヌクレイン(α-synuclein; α-syn)は、パーキンソン病(PD)の黒質緻密部やその他の脳領域におけるレビー小体や神経突起に存在する主要な病原性タンパク質です。このパーキンソン病の動物モデルでは、M83トランスジェニックマウス[B6;C3-Tg( Prnp SNCA A53T )83Vle/J]の脳に、遺伝子組み換えヒトα--M83トランスジェニックマウス[B6;C3-Tg( Prnp SNCA A53T )83Vle/J]の脳内に、あらかじめ形成されたリコンビナントヒトα-シヌクレイン線維(PFF)を定位注入します。または、非トランスジェニックの野生型(B6-C3H)マウスの脳内に、リコンビナントマウスα-シヌクレインを注入します。
検証済みの注入部位は、前嗅覚核(AON)、線条体 +/- 上部大脳皮質、および内側前脳束(MFB)です。
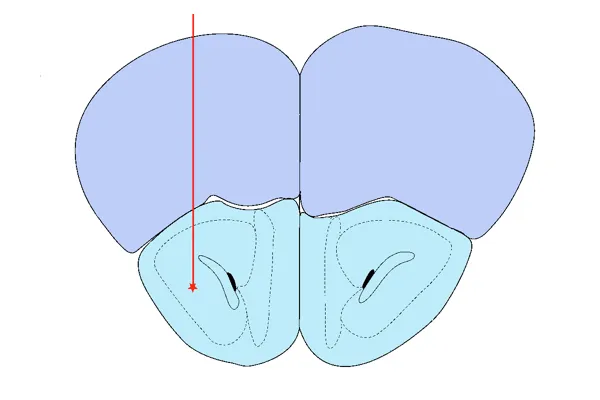
AON注射
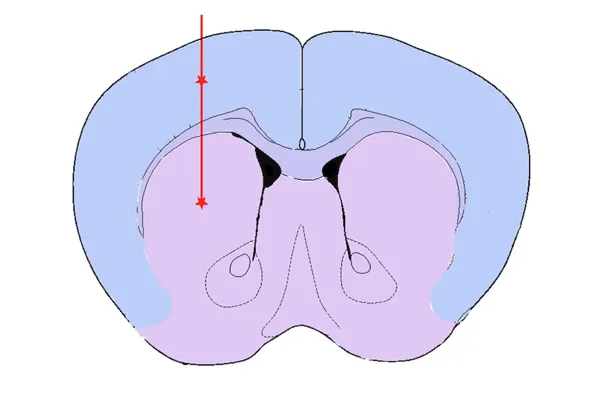
線条体およびその上部の皮質への注射
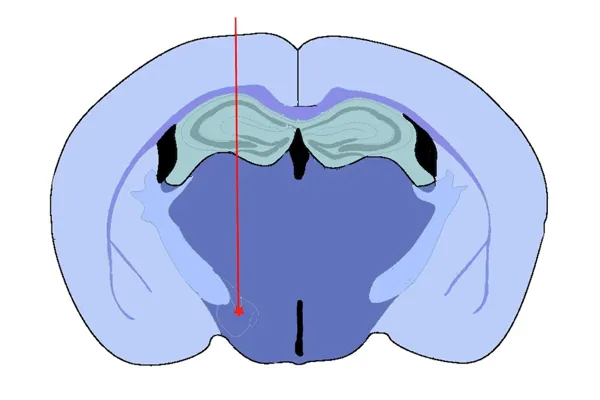
内側前脳束(MFB)注射
前嗅覚核(AON)への組換え前駆線維の定位注入後の、α-シヌクレイン病理の空間的広がりパターン。
前嗅覚核(AON) を標的とする根拠には、以下が含まれます 。
- ヒトのパーキンソン病において、α-シヌクレイン病理が最も早期に現れる部位のひとつである(Braakのステージ1)
- 辺縁系に関連する非運動症状(例えば、嗅覚低下/嗅覚喪失、睡眠障害)が広く見られ、パーキンソン病の初期症状である
- AONは、嗅球、扁桃体、嗅覚皮質への直接(1次)接続、および海馬や嗅内皮質などの高次接続を含む、同側および反対側の複数の脳領域に接続されています。これらの領域の多くは神経変性に対して非常に脆弱です。
線条体 +/- 皮質へのターゲティングの根拠には、以下が含まれます。
- これは、当初報告された注射部位です(Luk et al.,J. Exp.Med., 209: 975-986, 2011; doi: 10.1084/jem.20112457;Luk et al.,Science,338: 949-953, 2012; doi: 10.1126/science.1227157)
- 線条体のドーパミン作動性神経終末は、黒質にあるニューロンから発生します
- その上にある大脳皮質への注射は、脳内のα-シヌクレイン病理の範囲を増加させます
内側前脳束(MFB) を標的とする根拠には、以下のものがあります 。
- 黒質および腹側被蓋野に直接つながる神経線維であり、ヒトのパーキンソン病の毒素モデル(例えば、6-ヒドロキシドーパミン [6-OHDA])で標的にされることが多い
- 多くの他の脳領域からの投射の「ハブ」として機能し、それにより、遠く離れた脳領域へのα-シヌクレイン病理の広がりを促進する優れたシード位置として機能します
- このモデルでは、黒質におけるチロシン水酸化酵素陽性ドーパミン作動性ニューロンの損失と、それに伴う運動障害が起こります
このパーキンソン病の動物モデルの大きな利点は、以下を含むヒトの疾患の多くの側面を再現していることです。
- 明確な時空間パターンで再現性高く広がるα-シヌクレインが、神経細胞体および神経突起に広範なα-シヌクレイン病理を引き起こす
- 強い神経炎症(活性化ミクログリアおよび反応性アストロサイト)
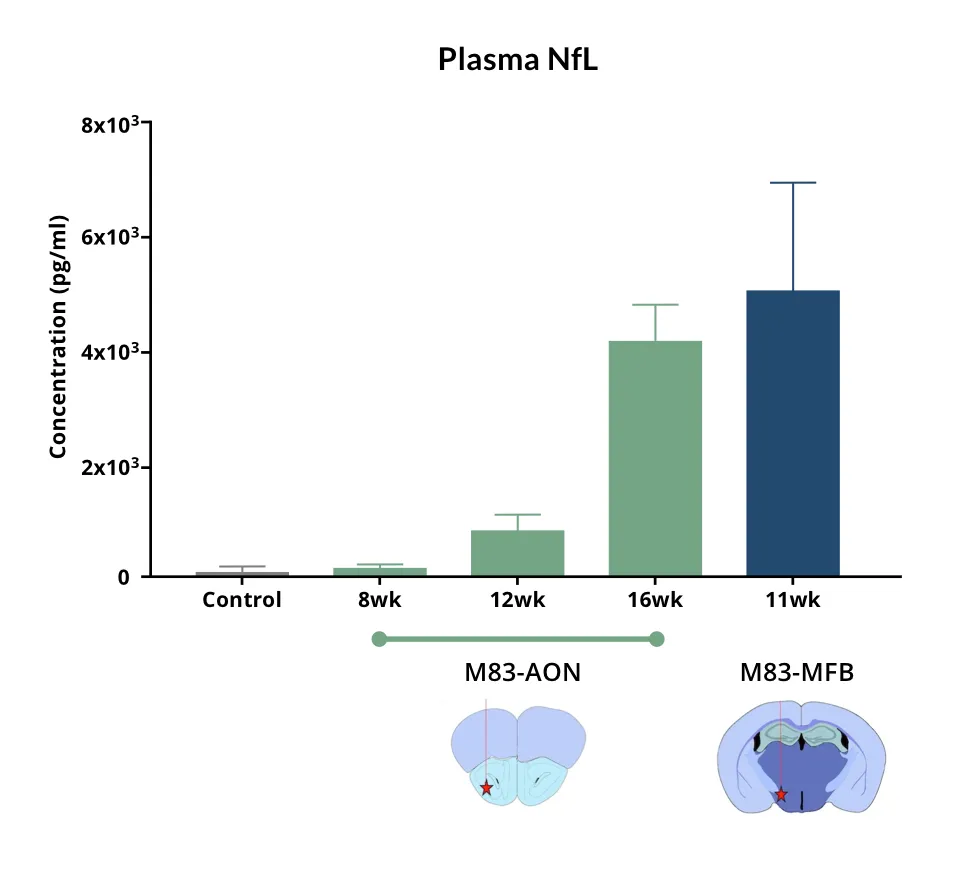
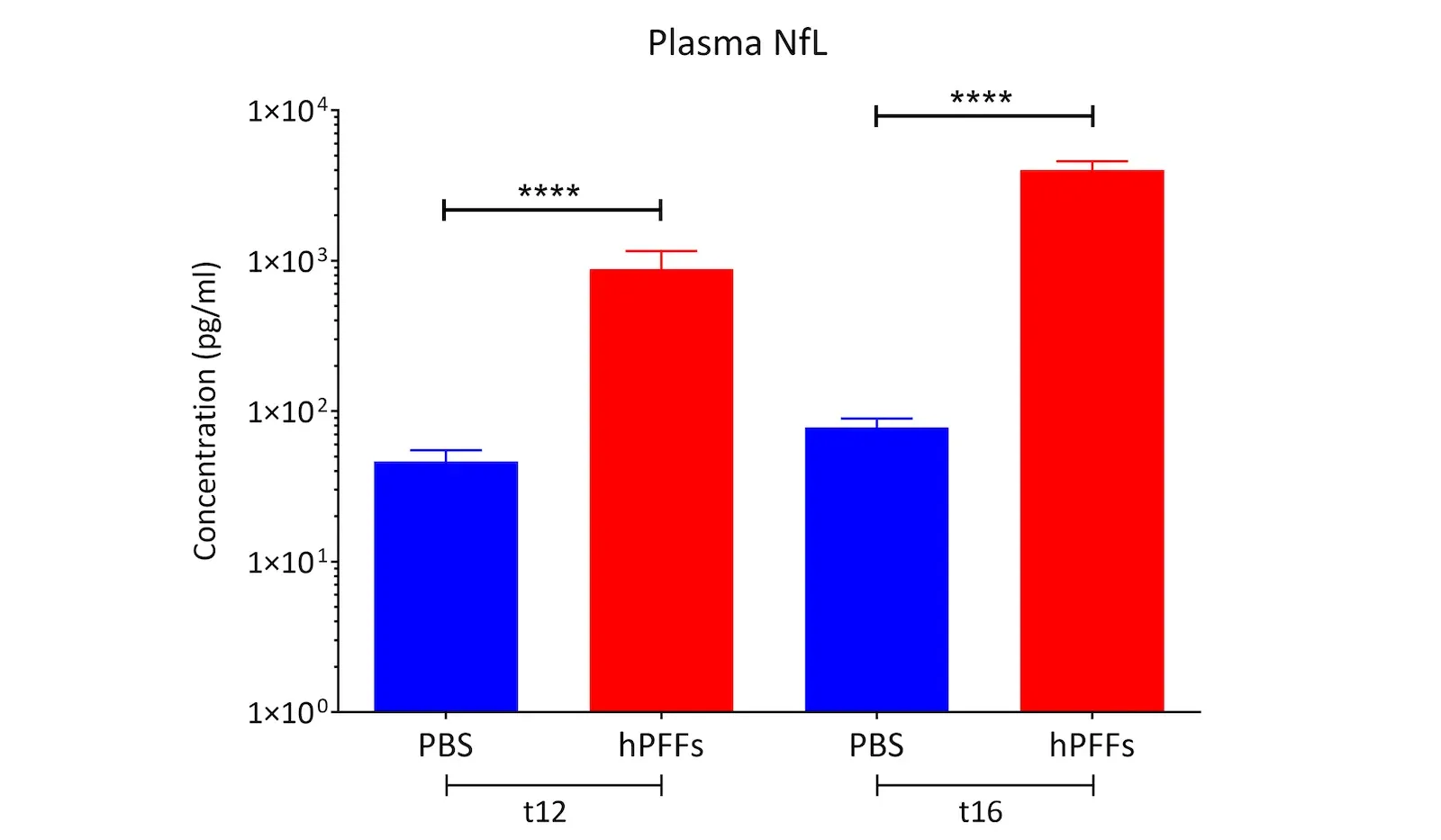
- 神経フィラメント軽鎖(NfL;NF-L)の血中および脳脊髄液中のレベル上昇を伴う神経変性
- 測定可能な行動の変化(運動機能、睡眠など)
- 治療介入による疾患修飾が可能な
シヌクレインモデルの生成
シヌクレインPFF動物モデルの一般的な作成方法は以下の通りです。
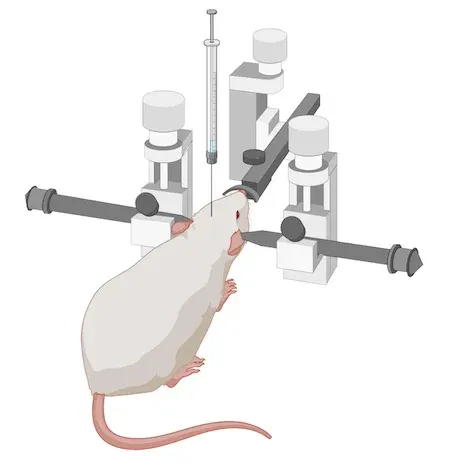
弊社は M83 トランスジェニック(tg)マウスのライセンス供与を受けています。 弊社は前臨床神経科学 CRO として、Biospective 社内にこれらのトランスジェニックα-シヌクレインマウスの繁殖コロニーを確立し、維持しています。これにより、100匹以上の規模の研究を実施することが可能です。
この齧歯類モデルでは、M83+/-マウスを繁殖させ、8~12週齢まで飼育します。あるいは、8~12週齢の野生型(B6-C3H)マウスを使用します。その後、超音波処理したヒトαシヌクレインPFFを、標的領域に定位注入します。デジタル式の定位装置と自動マイクロインジェクターを使用することで、高い精度と正確性を実現しています。
この動物モデルは、ほぼ100%の成功率でシヌクレインPFFの播種が可能であり、再現性が高いです。
当社のシヌクレインマウスモデルで検証された測定値は
- 体重
- 臨床スコア
- 行動評価
- 運動機能テスト
- 睡眠分析
- MRIによる脳萎縮(プレゼンテーション「神経変性疾患モデルマウスにおける脳萎縮分析」でさらに詳しく)
- 血漿および脳脊髄液中のニューロフィラメント軽鎖の測定(リソース「パーキンソン病モデルにおけるニューロフィラメント軽鎖」をご覧ください)
- 免疫組織化学および多重免疫蛍光法(プレゼンテーション「パーキンソン病α-シヌクレインマウスモデルにおけるミクログリアの活性化」をご覧ください)
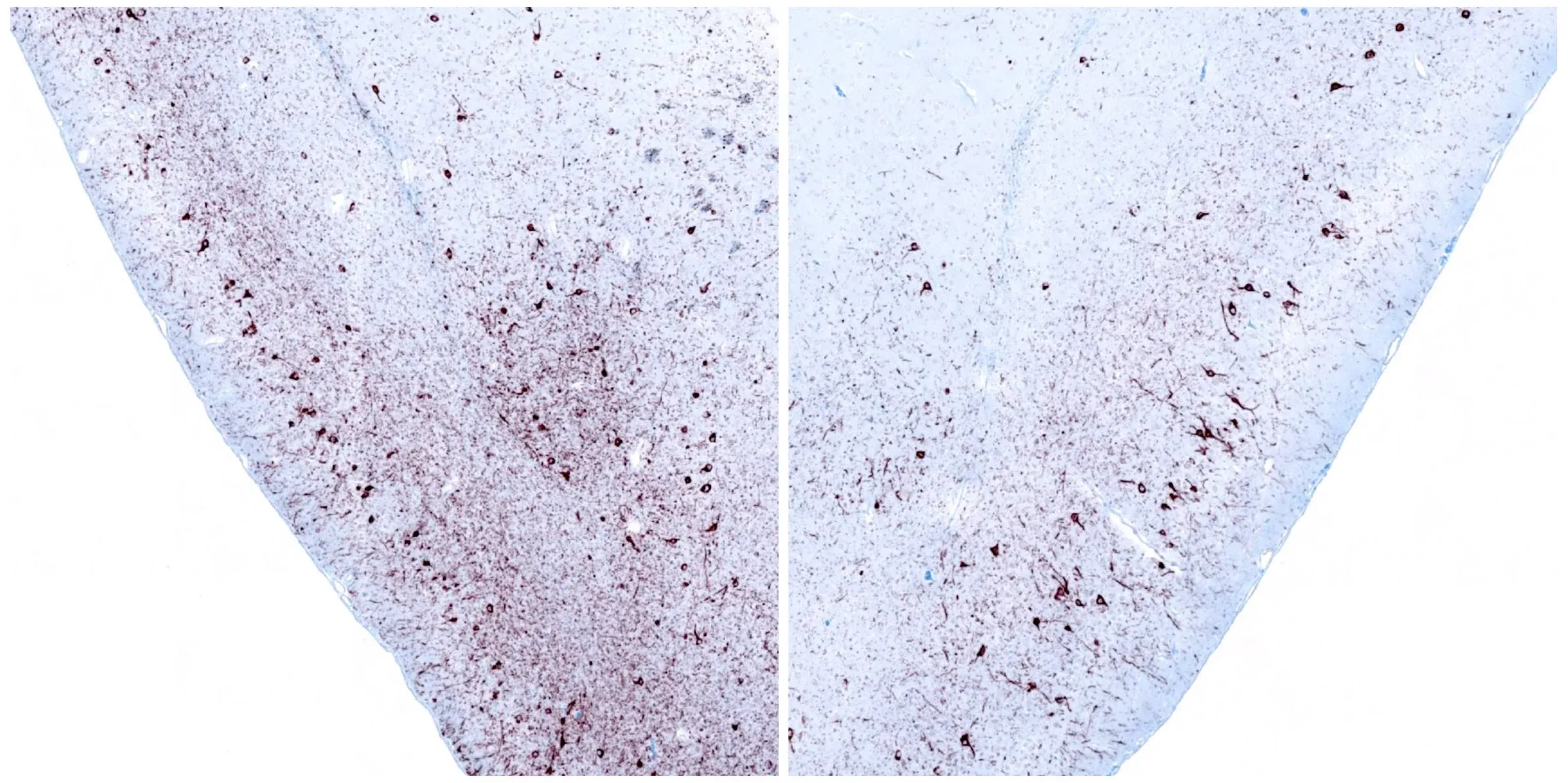
M83+/-マウスの前嗅覚核にα-シヌクレイン前駆体線維を片側的に定位注入した12週間後の同側(左)および反対側(右)の嗅球皮質のリン酸化α-シヌクレイン免疫組織化学染色。
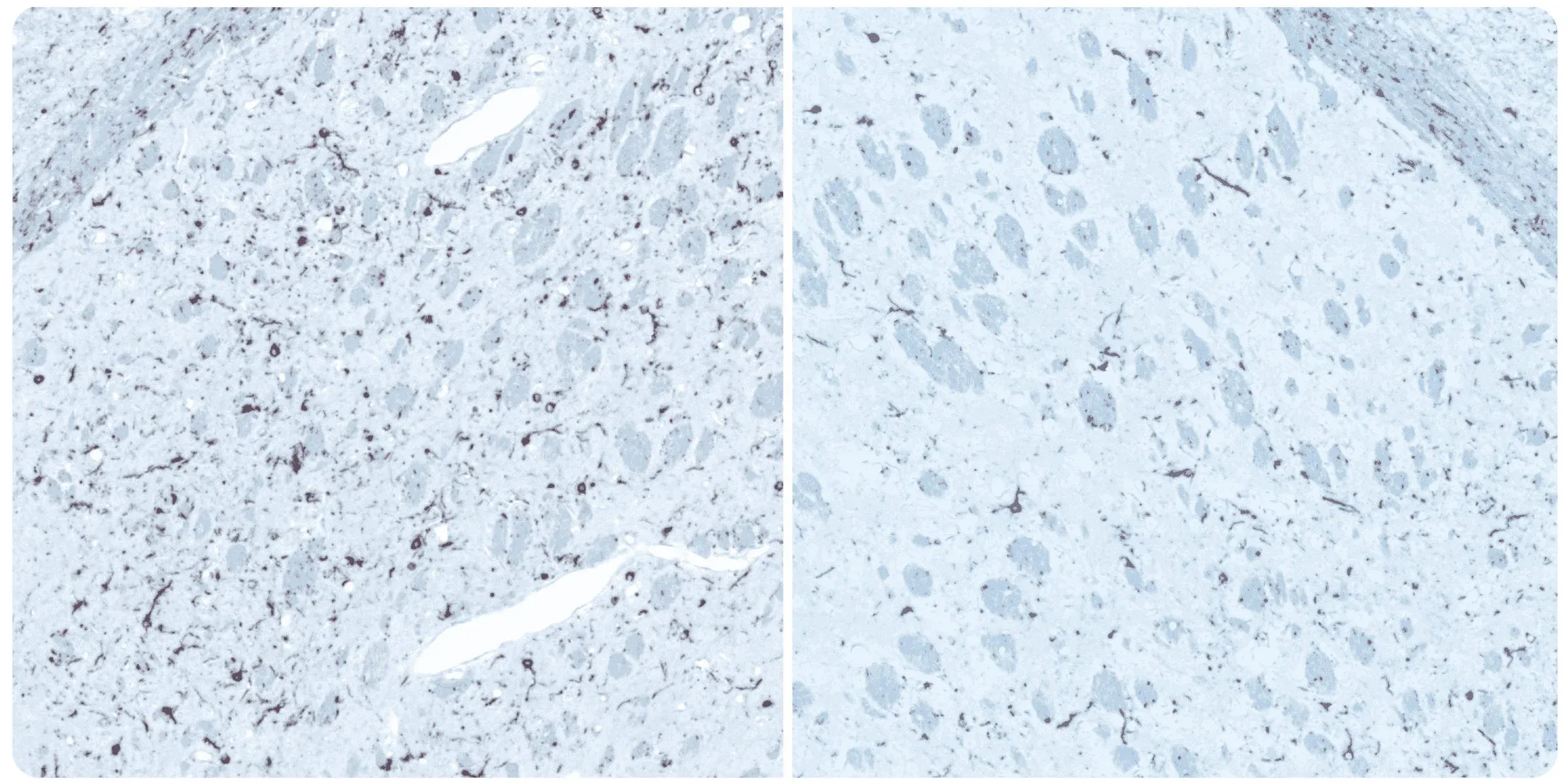
M83+/-マウスの線条体およびその上の大脳皮質に、α-シヌクレイン前駆体線維(PFF)を片側から定位注入した後の、注入後12週目の同側(左)および反対側(右)線条体のリン酸化α-シヌクレイン免疫組織化学染色。
このモデルの特性評価、検証済みの測定、前臨床神経科学 CRO サービスについて、さらに詳しく知ることができます。
パーキンソン病モデルについてさらに詳しく知る
関連コンテンツ
パーキンソン病に関する最新情報と、パーキンソン病モデル動物における治療薬の評価に関するベストプラクティス。
パーキンソン病モデルにおけるニューロフィラメント軽鎖
神経フィラメント軽鎖(NfL;NF-L)レベルが、パーキンソン病のマウスおよびラットモデルにおける血液(血漿;血清)およびCSFバイオマーカーとして使用できる方法。
パーキンソン病治療薬開発のためのAAV α-シヌクレインモデル
疾患修飾治療薬の前臨床研究に使用するマウスおよびラットモデルにおけるアデノ随伴ウイルス(AAV)によるα-シヌクレイン発現の概要。