目录
什么是额颞叶痴呆症(FTD)?
临床特征和亚型
额颞叶痴呆症(FTD)是一种常见的痴呆症,尤其影响 65 岁以下的患者。阿尔茨海默病(AD)是 早发 痴呆症最常见的病因,其次是血管性痴呆和额颞叶变性(FTLD)(Vieira, 2013)。额颞叶变性是一组临床和病理上异质性的神经退行性综合征,与额叶和颞叶的进行性变性有关。在临床上,FTD 代表了潜在的 FTLD 病理的症状表现,其特征是行为、执行功能和/或语言的进行性障碍(Root, 2021 年)。
根据发病时的主要症状,FTD 可大致分为不同的临床综合征。最常见的表现是行为变异型 FTD(bvFTD),约占病例的 60-80%。行为变异型 FTD 的特征是人格和社会行为的早期和进行性改变,包括行为抑制、冷漠、强迫或刻板行为以及洞察力丧失。随着病情的发展,患者还可能出现语言障碍、帕金森病特征或运动神经元病(MND)。
FTD 的两种主要语言变异被归类为原发性进行性失语症(PPA):
语义变异型 PPA(svPPA)的特点是逐渐丧失语义知识,包括单词理解能力受损以及对物体和面孔的识别能力减弱。患者通常表现为言语流畅但空洞,并伴有严重的失认症。
非流利/语法变异型 PPA(nfvPPA)的定义是非流利、费力的言语。临床特征可能包括口语和书面语无语法和言语瘫痪--一种扰乱词语生成的运动规划障碍(Whitwell,2019)。
尽管我们对 FTD 的临床谱系和遗传基础的了解有所进展,但目前还没有获得批准的疾病改变疗法。现有的治疗方法都是对症治疗,旨在控制行为或认知症状,而不是改变疾病的进展,这突出表明我们需要建立强大的临床前模型。
神经病理学和遗传学
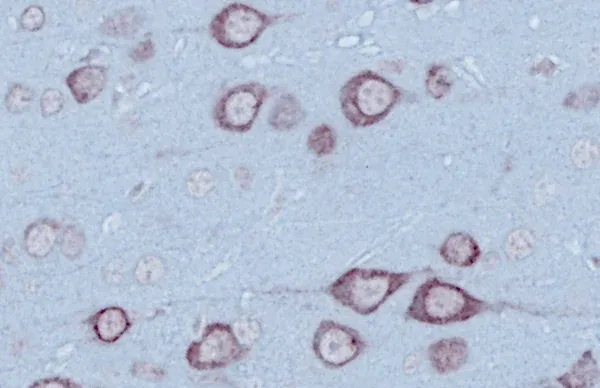
FTD在神经病理学上具有异质性,最常见的定义是三种蛋白质之一的异常聚集:微管相关蛋白tau、TAR DNA结合蛋白43(TDP-43)或肉瘤融合蛋白(FUS)。根据主要病理蛋白,FTD 又可分为 FTLD-tau、FTLD-TDP 和 FTLD-FUS。
重要的是,临床表现并不能可靠地预测潜在的分子病理学。例如,bvFTD 可能与三种主要病理形式中的任何一种有关。相比之下,svPPA与FTLD-TDP的关联最为一致,而nfvPPA则主要与FTLD-tau病理相关。
相当一部分 FTD 病例是家族性的,通常为常染色体显性遗传。最常涉及的基因包括MAPT、GRN(progranulin)和C9orf72 中的 GGGGCC 六核苷酸重复扩增。MAPT突变与 FTLD-tau 有关,而GRN和C9orf72突变则与 FTLD-TDP 病理有关。这三种突变通常都表现为bvFTD,但GRN和C9orf72携带者往往表现出更广泛的表型变异,包括语言障碍、帕金森症或肌萎缩侧索硬化症(ALS)(Whitwell, 2019)。
要了解有关 FTD 神经病理学特征的更多信息,请访问我们的资源:额颞叶痴呆的神经影像学和临床试验。
目前,人们普遍认为 FTD 和 ALS 是一种连续的神经退行性疾病,在遗传、临床和病理特征方面存在重叠。这两种疾病之间最显著的遗传联系是C9orf72重复扩增,而TARDBP、SQSTM1、UBQLN2、CHMP2B、CHCHD10和VCP 的突变频率较低,这进一步支持了共同的致病谱(Lopez-Herdoiza, 2023 年; Genin, 2024 年)。
在我们的资料中了解有关 ALS 的更多信息:ALS 药物发现模型指南》。
为什么用小鼠作为 FTD 的动物模型?
鉴于 FTD 在临床和病理上的异质性,人们开发了多种转基因和 AAV 介导的小鼠模型,以重现该疾病的关键分子和神经病理学特征。小鼠因其遗传易感性、保守的神经元回路以及适合进行详细的分子、细胞和功能研究,仍然是 FTD 研究中使用最广泛的物种。大多数FTD小鼠品系都被设计为表达与疾病相关的突变或蛋白,从而能够在基因和蛋白水平上进行与FTD发病机制相关的机理研究(Ahmed, 2017)。
FTD主要影响显著性网络,其中包括前脑岛、前扣带回皮层、腹侧纹状体、杏仁核、背内侧丘脑、下丘脑和几个脑干核团,包括下咽周围灰质、黑质和腹侧被盖区。这些相互关联的区域控制着基本的生理和行为过程,如疼痛、饥饿、口渴、自主神经调节、奖赏处理、动机和恐惧反应。重要的是,这一网络的核心结构和连通性在不同物种间高度保守,支持使用小鼠来模拟与 FTD 相关的电路功能障碍的关键方面(Roberson, 2012 年)。
受 FTD 影响的行为领域及其与小鼠模型的相关性
在 FTD 中被破坏的几个行为领域依赖于保守的神经解剖回路,因此可以使用有效的行为范式在啮齿类动物中进行部分建模(Kesner, 2011 年; Bizon, 2012 年; Roberson, 2012 年; Hamilton,2015 年; Mora,2023 年):
社交功能障碍: FTD患者社会参与度降低和移情能力丧失与内侧前额叶皮质(PFC)功能障碍有关。在背内侧前额叶皮层受累的突变小鼠中也观察到了类似的缺陷。前扣带回皮层--也与 FTD 有关--在调节啮齿类动物的移情和社会行为方面发挥着关键作用。
重复行为:在某些基因敲除小鼠模型中观察到的病理性梳理和刻板行为与 FTD 中的强迫和重复行为相似。纹状体在这两种行为中都起着核心作用。
情绪失调: FTD 患者经常表现出对负面情绪的反应迟钝,这与杏仁核萎缩有关。同样,杏仁核功能受损的小鼠也表现出恐惧条件反射受损,这支持了这些模型的转化价值。
执行障碍:计划、决策和工作记忆的进行性损伤是 FTD 的核心特征,涉及背外侧前脑皮质、前扣带回皮质、内侧前脑皮质和基底神经节的功能障碍。在 FTD 小鼠模型中,PFC-纹状体-丘脑回路的破坏同样会导致执行功能障碍。这些缺陷通常通过 T 型迷宫、Y 型迷宫和注意集转移范式等任务进行评估。
认知灵活性:FTD 患者的注意力或行为转移困难以及思维僵化与眶额皮质(OFC)、前额皮质、丘脑内侧和基底神经节有关。OFC萎缩与FTD患者和啮齿类动物模型的行为不灵活有关。逆向学习和触摸屏操作移位测试用于测量认知不灵活。
运动功能障碍: 运动症状尤其发生在FTD-ALS谱系或伴有tau突变的FTD中,涉及运动皮层(初级和辅助运动区)、基底节和脑干运动通路。在 FTD 啮齿动物模型中,运动表型与皮质和基底节变性有关。旋转运动能力、握力、步态分析和握拳常用于量化运动能力的下降。
对 FTD 小鼠模型进行全面的行为评估,包括测量重复行为、社会互动和情绪反应,为临床前评估疾病改变疗法提供了可靠的终点。
FTD 研究中小鼠模型的重要考虑因素
FTD 小鼠模型的设计主要是为了复制 bvFTD 的核心行为特征,包括社交退缩、抑制、强迫行为和刻板运动模式。这一重点既实用又与临床相关,因为bvFTD是最常见的FTD亚型,发病率约为PPA的四倍(Hogan, 2016)。
事实证明,这些临床前模型对于揭示疾病机制、绘制受影响的神经回路图以及在可访问的、表征良好的系统中确定潜在的治疗靶点非常有价值。然而,FTD 的语言优势形式建模--svPPA 和 nfvPPA--仍然是一个重大挑战。这些综合症依赖于复杂的语言和语义网络,而这些网络在啮齿类动物大脑中并没有直接的同源物,因此在小鼠中完全重现语言相关缺陷是不可行的。
因此,临床前研究适当地强调了在 FTD 中严重受损且在动物模型中可进行实验的行为维度。为了解决啮齿类动物系统的局限性,研究人员越来越多地整合基于人类的补充方法,如诱导多能干细胞(iPSC)衍生的神经元、脑器质和患者神经影像学研究,以研究语言和语义网络病理学的各个方面(Roberson, 2012; Whitwell, 2019)。
尽管存在这些限制,小鼠模型仍然是转化研究管道的重要组成部分。小鼠模型提供了对 FTD 早期细胞和电路水平机制的重要见解,并为评估体内候选疗法提供了一个强大的平台。
临床前研究中使用的 FTD 小鼠模型主要有哪些?
基于 tau 的模型(MAPT)
tau基因(MAPT)的突变是FTD的主要遗传原因,此外还有GRN和C9orf72的突变。目前已发现 40 多种与 FTD 相关的MAPT 基因突变,其中大多数是微管结合区内的错义突变。这些突变通过降低微管的稳定性产生功能缺失效应,并通过增强 tau 的聚集和过度磷酸化产生功能增益效应(Roberson, 2012 年)。
人类 tau 的突变形式(包括 P301S 和 P301L)与帕金森病-17(FTDP-17)等 tau 病有关。
在 Biospective,我们采用多种方法生成 Tau 小鼠模型:
Tau预成纤维(PFF)播种:可在体内传播病理 tau,促进对 tau 扩散和聚集的研究。在此探索该模型:Tau 纤维扩散模型。
AAV-hTau递送: 在成年 C57BL/6 小鼠的大脑中颅内注射 AAV 载体可再现人类 tau 蛋白病的主要特征,包括磷酸化 tau 聚集、行为功能障碍和体内MRI 检测到的脑萎缩。这种方法可以在相对较短的时间内生成读数。点击此处查看互动图片演示:AAV Tau 小鼠模型。
主要 Tau 小鼠模型
rTg(TauP301L)4510
该模型在前脑(包括海马和新皮层)表达人类 P301L tau 突变,转基因表达可通过多西环素调节。小鼠表现出年龄依赖性神经纤维缠结(NFT)形成,并伴有明显的前脑萎缩和神经元缺失。
行为小鼠早期表现出多动和焦虑样行为减少,4 个月左右开始出现空间记忆缺陷和进行性运动障碍,包括特征性的紧握反射(Lewis, 2000 年; Ramsden,2005 年; Pennanen, 2006 年)。
AAV-TauP301L
在该模型中,使用 AAV 载体将人类 P301L tau 送入颅内,从而在目标脑区广泛表达 tau。这种方法会导致 tau 过度磷酸化、前三角区和成熟 NFT 的形成、萎缩性神经元和神经炎症反应。
行为小鼠表现出多动、抑制、恐惧条件反射受损和记忆缺陷,反映出海马和杏仁核依赖回路的功能障碍(Cook, 2015; Silva-Llanes, 2025)。
AAV-TauP301L小鼠模型中人类tau的广泛表达(图 B、E)与在rTg4510小鼠中观察到的分布(图 C、F)密切相关。图以 知识共享署名许可协议转载自库克等人(Cook, 2015) 。
P301S Tau
这种转基因模型(如PS19 小鼠)表达人类 P301S tau 突变,其特点是早发性行为和认知障碍,在出现广泛的 NFT 病理学之前就已出现。突触功能障碍最早可在小鼠三个月大时观察到,随后在九到十二个月大时出现进行性 tau 积累、神经元缺失和脑萎缩。
行为:早期表型包括多动和焦虑样行为减少,在莫里斯水迷宫中检测到空间记忆缺陷(Takeuchi, 2011 年)。
前聚集 Tau(hTau40,ΔK280)
该模型使用可调节的前脑表达全长人 tau 的促聚集变体,该变体含有 ΔK280 突变,可增强 β 结构的形成和 tau 的聚集(Eckermann, 2007 年)。虽然没有观察到明显的神经元损失,但小鼠表现出明显的突触缺陷和长期电位降低。
行为:基因长期表达后,小鼠会出现严重的学习和记忆障碍,而运动功能则保持不变(Van der Jeugd, 2012 年)。
MAPT P301S;Int10+3;S320F 基因敲入
这种三重突变基因敲入模型表现出强大的早期 tau 病理学,病理 tau 逐渐积累,突触缺失,海马、下丘脑和杏仁核严重萎缩,并伴有星形胶质细胞增生。
行为小鼠表现出焦虑增加、重复和刻板行为、持续注意力受损、冷漠行为以及学习和行为灵活性缺陷(Morito, 2025 年)。
基于 TDP-43 的模型
TDP-43 阳性内含物是 FTD(FTD-TDP)最常见的病理基质。TDP-43 是一种核 RNA 和 DNA 结合蛋白,参与 RNA 处理和调节。TARDPB的致病突变会导致 TDP-43 从细胞核向细胞质误定位,从而导致细胞核功能丧失和细胞质毒性功能增强(Roberson, 2012 年)。
进一步了解Biospective 的 TDP-43ΔNLS (rNLS8) 小鼠模型。
关键 TDP-43 小鼠模型
TDP-43 Q331K 转基因小鼠模型
该模型在小鼠朊病毒启动子下表达人类TARDBPQ331K 突变,从而使小鼠 TDP-43 接近生理表达水平并下调内源性小鼠 TDP-43。该蛋白仍主要存在于细胞核中,不会形成典型的细胞质聚集体(Wong, 2020; Watkins, 2021)。
行为:小鼠会出现震颤、步态异常、肌肉量减少以及额叶皮层介导的认知障碍,而海马依赖性记忆则基本保持不变(Wong, 2020 年; Watkins, 2021 年)。
TDP-43 Q331K 基因敲入
在这个与生理相关的模型中,Q331K 突变被引入内源性小鼠TARDBP基因,避免了过表达的假象。该模型再现了ALS-FTD中出现的主要脑结构变化,包括额叶和内叶皮质及海马的萎缩,以及广泛的小胶质细胞激活(White, 2018; Lin, 2021)。
行为:小鼠表现出学习、注意力和记忆障碍(White, 2018; Lin, 2021)。
与年龄匹配的野生型对照组相比,体内磁共振成像(MRI)显示TDP-43Q331K/Q331K基因敲入小鼠的区域性脑容量损失(冷色)和脑室扩大(暖色),突出显示了反映人类 ALS-FTD 病理的结构变化。图以 知识共享署名许可协议转载自 Lin等人(Lin, 2021 年) 。
CamKIIa-hTDP-43NLSm 接种
该模型使用在 CAMKIIa 启动子下表达人 TDP-43 细胞质错位形式的转基因小鼠,可以研究病理 TDP-43 提取物接种后 TDP-43 的播种、聚集和传播(Porta, 2018 年)。
AAV-TDP-43模型(AAV5、AAV8、AAV9)
AAV 介导的 TDP-43 变体递送可诱导特定区域的细胞质聚集或过表达,重现皮质脊髓束变性、下丘脑萎缩、运动功能障碍、社交行为缺陷和神经肌肉病理学等特征(Jackson, 2015; Bergh, 2025; Mori, 2025)。
C9orf72 重复扩增模型
C9orf72的六核苷酸(G4C2)重复扩增是家族性FTD和ALS最常见的遗传病因。疾病病理源于毒性RNA病灶的形成、二肽重复(DPR)蛋白聚集和单倍体缺陷,这些因素共同损害了自噬和神经炎症调节(Batra, 2017; Lopez-Herdoiza, 2023)。
要进一步了解自噬在神经退行性疾病中的作用,请参阅我们的资料:自噬与神经退行性疾病。
主要 C9orf72 小鼠模型
AAV(G4C2)66 和 AAV(G4C2)102
颅内输送扩大的 G4C2 重复序列可诱导 RNA 病灶、DPR 聚集、皮质神经元缺失、胶质细胞病变和神经肌肉接头 (NMJ) 异常 。
行为小鼠表现出焦虑样行为增加、社交障碍、运动协调障碍和记忆功能障碍(Chew, 2015; Herranz-Martin, 2017)。
BAC-C9-500
该模型使用细菌人工染色体表达了 500 个人类 G4C2 重复序列,导致广泛的 DPR 聚集、TDP-43 病理学、广泛的神经元缺失和胶质细胞病变。
行为小鼠会出现焦虑样行为、运动障碍、紧握和后肢瘫痪(Liu, 2016)。
miR- C9orf72敲除
慢病毒介导的C9orf72基因敲除模拟了患者的单倍体缺陷,导致自噬缺陷、细胞质 TDP-43 积累、突触缺失和晚期神经肌肉接头异常。
行为小鼠表现出社会交往障碍和抑郁样行为(Lopez-Herdoiza, 2023 年)。
Biospective 提供业界领先的神经肌肉接头染色和神经支配与神经再生图像分析。欲了解更多信息,请访问动物模型肌肉标本的神经肌肉接头 (NMJ) 分析。
GRN(Progranulin)模型
Progranulin 是一种溶酶体蛋白,主要由小胶质细胞产生,是正常溶酶体功能所必需的(Root, 2021 年)。GRN 基因突变约占 FTD 病例的 5%,会导致 Progranulin 单倍蛋白缺乏或功能缺失。
主要 GRN 小鼠模型
GRN-/-(同基因)
原谷蛋白完全缺失会导致严重的溶酶体功能障碍、脂质沉着病、小胶质细胞病变和星形胶质细胞病变。
行为小鼠表现出强迫性梳理和社交能力下降,而依赖海马的学习和记忆直到晚期仍得以保留(Kashyap, 2023 年; Life, 2023 年)。
GRN +/-(杂合子)
部分原谷蛋白缺乏会导致相对轻微的神经病理学,但会出现可测量的突触和行为异常(Filiano, 2013; Kashyap, 2023; Life, 2023)。
行为:小鼠表现出明显的社交障碍、恐惧条件反射受损、多动和重复挖掘行为增加(Filiano, 2013; Kashyap, 2023; Life, 2023)。
人源化GRN -/-;GRNtg
该模型在小鼠原粒细胞蛋白无效背景上表达单拷贝的人类GRN基因,与杂合子表型非常相似,在晚期出现轻微的小胶质细胞病变。
行为小鼠表现出多动和重复挖掘增多(Life, 2023)。
额颞叶痴呆 (FTD) 小鼠模型全面概述:遗传学、病理学和行为表型
基于 Tau 的模型(MAPT)
小鼠模型 | 遗传学 | 病理学 | 运动功能 | 行为 |
以 AAV 为介导,在成年小鼠黑质(SNc)中过表达野生型(2N4R)人类 tau。 | SNc神经元中出现磷酸化tau包涵体;SN多巴胺能神经元大量缺失,纹状体也出现相应的神经支配;SNc中出现明显的小胶质细胞病变和星形胶质细胞病变;SNc、纹状体和中脑出现萎缩。 | 单侧注射 SNc 会导致明显的运动障碍(不对称运动功能障碍)。 | SNc靶向主要产生运动表型,短期内未观察到明显的认知障碍。 | |
PS19(P301S)tau 转基因背景;向海马和上覆皮层立体定向注射人 tau PFFs。 | 广泛的 tau 病理变化以明确的时空模式从注射部位扩散;明显的小胶质细胞病变/astrogliosis。 | 无明显运动障碍。 | 无明显认知障碍。 | |
rTg(TauP301L)4510 转基因 | 人 P301L tau 表达于前脑(海马和新皮层),可受强力霉素调节。 | 小鼠表现出年龄依赖性 NFT 形成、前脑严重萎缩和神经元严重缺失。 | 后期表现为行走能力和后肢紧握反射减弱。 | 早期的空间参照记忆障碍会随着年龄的增长而恶化;认知能力严重下降。 |
AAV-TauP301L | 通过 AAV 颅内载体递送的人类 P301L tau。 | Tau 高磷酸化、聚集、NFT、突触功能障碍、神经炎症;无明显神经元损失。 | 无明显运动障碍。 | 多动、抑制、探索减少、恐惧条件反射和记忆缺陷。 |
P301S 转基因 | 人 P301S tau 在前脑表达。 | 突触病理学、丝状 tau 病变、进行性 tau 累积、神经元缺失、脑萎缩。 | 无明显运动障碍。 | 早期多动、焦虑减少、空间记忆障碍。 |
前聚集 Tau(hTau40,ΔK280) | ΔK280突变的前脑表达可调的促聚集Tau。 | Tau聚集、磷酸化亢进、β结构形成、海马棘突触明显减少;无神经元缺失。 | 无明显运动障碍。 | 后期出现严重的学习和记忆障碍。 |
P301S;Int10+3;S320F 基因敲入 | 表达 P301S、Int10+3 和 S320F 的三重突变基因敲入。 | 进行性 tau 累积、突触丧失、严重脑萎缩、星形胶质细胞增多。 | 无明显运动障碍。 | 焦虑增加、行为重复、学习能力和行为灵活性受损。 |
基于 Tau(MAPT)突变的常用 FTD 小鼠模型概述。介绍了关键基因改变、特征性神经病理学特征(包括 Tau 聚合和神经纤维病理学)、运动功能结果和行为表型,以支持对疾病机制和治疗策略的临床前研究。
基于 TDP-43TDP-43 的模型(TARDBP)
小鼠模型 | 遗传学 | 病理学 | 运动功能 | 行为 |
双转基因(NEFH-tTA × tetO-hTDP-43-ΔNLS)可使缺乏核定位信号的人类 TDP-43 在神经元中表达;表达可受强力霉素调节。 | 细胞质 TDP-43 错定位,出现磷酸化聚集;广泛的神经变性;NMJ 神经支配;严重的小胶质细胞病变和星形胶质细胞病变;后肢肌肉萎缩。 | 诱导后迅速出现严重的运动障碍。 | 主要是运动表型,无明显认知障碍的报道。 Biospective 的 Low Dox 方案可延缓疾病进展,延长存活期,并可对疗效研究进行纵向评估。 | |
转基因 TDP-43 Q331K | 朊病毒启动子下的人类 TARDBP Q331K。 | 出现症状时没有典型的细胞质 TDP-43 聚集;蛋白质仍为核蛋白。 | 早期震颤、步态异常、后肢质量减少、肌肉功能下降。 | 工作记忆和认知灵活性缺陷;空间学习能力保持不变。 |
TDP-43 Q331K 基因敲入 | 内源性 TARDBP 的生理相关突变。 | TDP-43 表达增加,RNA 剪接改变,脑萎缩明显,脑室扩大,小胶质细胞广泛激活。 | 无明显运动障碍。 | 学习、注意力和记忆障碍。 |
AAV5-TDP-43 | AAV 介导的人类 TDP-43 向下丘脑输送。 | 剂量依赖性下丘脑萎缩、核和细胞质 TDP-43 包涵体、代谢失调。 | 运动活动和协调能力降低 | 探索行为减少,筑巢行为减少(类似冷漠行为)。 |
由 TDP-43 (TARDBP) 突变或失调驱动的广泛使用的 FTD 小鼠模型概述。该表概述了与机理和转化研究相关的主要基因修饰、标志性病理结果(如 TDP-43 错定位和聚集)、运动障碍和行为异常。
C9orf72 重复扩增模型
小鼠模型 | 遗传学 | 病理学 | 运动功能 | 行为 |
AAV(G4C2)66 | 通过 AAV 扩增人类 G4C2 66 倍重复。 | DPRs、pTDP-43 聚集、皮质神经元缺失、神经炎症。 | 运动功能降低。 | 焦虑增加、社交障碍。 |
AAV(G4C2)102 | 通过 AAV 扩增人类 G4C2 102 重复序列。 | RNA 病灶、DPR 病理、Purkinje 细胞凋亡、稀疏胞质 TDP-43 聚集。 | 随着年龄增长,协调能力下降,活动减少,步态恶化。 | 工作记忆缺陷。 |
BAC-C9-500 | 表达人类 C9orf72 的 BAC 转基因,有 500 个重复序列。 | 大脑皮层、海马、脊髓出现广泛的 DPR 聚集、pTDP-43 病变、大量神经元丢失;神经炎症。 | 步态异常、握力减弱、后肢痉挛、瘫痪。 | 焦虑增加。 |
miR-C9orf72 | 慢病毒敲除模拟单倍体缺陷。 | 自噬-溶酶体功能障碍、TDP-43 聚集、皮质突触密度降低。 | 肌肉力量减弱,后期神经肌肉接头异常。 | 早期社交障碍,抑郁样行为增加。 |
基于 C9orf72 重复扩增模型的 FTD 小鼠模型总结。列出了主要的遗传策略、重复相关的病理特征(包括 RNA 病灶的形成和二肽重复蛋白的积累)、运动表型和行为结果,以促进临床前治疗的开发。
基于 Progranulin 的模型(GRN)
小鼠模型 | 遗传学 | 病理学 | 运动功能 | 行为 |
纯合子原粒细胞蛋白无效 (GRN-/-) | 前谷蛋白完全缺失 | 溶酶体功能障碍、神经炎症、TDP-43聚集。 | 无明显运动障碍。 | 强迫性梳理、社交能力下降;海马学习能力保持不变。 |
杂合子丙种球蛋白-无效(GRN+/-)。 | 一个功能拷贝;30-50% 的野生型 progranulin。 | 神经病理变化最小。 | 无明显运动障碍。 | 社交障碍、恐惧条件反射受损、多动、重复行为增加。 |
人源化原粒细胞缺乏症(GRN-/-;GRNtg) | 在 GRN 基因缺失背景上的单拷贝人类 GRN。 | 轻度小神经胶质增生,与 GRN+/- 相似。 | 无明显运动障碍。 | 多动,重复行为增加。 |
涉及原花青素(GRN)缺乏的已建立的 FTD 小鼠模型摘要。该表详细介绍了遗传策略、相关神经病理学(包括溶酶体功能障碍和 TDP-43 病理)、运动表现变化和行为表型,为疾病发病机制和干预方法研究提供了参考。
AAV 诱导的 FTD 模型有哪些优势?
基于 AAV 的方法为神经退行性疾病(如 FTD)建模提供了快速、灵活和精确的平台(Lunev, 2022 年; Aliev, 2025 年):
快速灵活: AAV 传播避免了培育要求,缩短了实验时间,并可与现有的转基因或基因敲除品系相结合。高通量研究允许进行药物筛选。
定向表达:AAV 载体可实现特定区域和细胞类型的基因表达,这种表达可在时间上加以控制,并具有高度的可重复性。
实验精确性:在成年动物体内进行基因递送可最大限度地减少发育干扰,并可在干预前进行基线表型分析。
安全性: 重组 AAV 无致病性,可高效转导非分裂细胞,并支持长期转基因表达。
总之,AAV 诱导的 FTD 模型加速了临床前研究,为剖析疾病机制和评估治疗策略提供了一个强大的平台。
AAV 诱导的模型能够快速、精确地生成量身定制的疾病模型,支持定向基因表达、高度的实验可重复性以及神经退行性疾病转化研究的高安全性。
哪些生活中的成像技术可支持 FTD 研究?
神经影像学在增进我们对 FTD 的了解方面发挥着至关重要的作用,它为早期诊断提供了非侵入性生物标志物,并为纵向了解疾病进展提供了依据。结构磁共振成像(MRI)、 [18F]fluorodeoxyglucose positron emission tomography([18F]FDG PET)、弥散张量成像(DTI)和静息态功能磁共振成像(rs-fMRI)等技术不断揭示出萎缩、代谢低下和网络破坏的亚型特异性模式。
在 bvFTD 中,结构磁共振成像和 FDG PET 通常显示前额叶皮质和前颞叶明显萎缩和代谢减弱,而后部脑区则相对保留(Bruun, 2019 年; Peet, 2021 年)。脑容量损失可能先于临床发病,并以每年高达 3% 的速度发展,尤其是在额叶。额叶萎缩与执行功能障碍相关,而颞叶退化则与外显记忆障碍有关(Ghetti, 2015; Whitwell, 2019)。DTI 研究揭示了前纹状体和前丘脑束的白质退化,这与行为的严重程度相关。静息态 fMRI 显示显著性网络内的连接性降低,与行为和执行功能障碍相对应。随着 FTD 的发展,连通性的下降会扩展到更广泛的网络,包括额叶、基底神经节和背侧注意系统(Ferreira, 2022 年)。
FTD 小鼠模型的临床前成像再现了人类病理学的许多特征。在 rTg4510 tauopathy 小鼠中,结构性 MRI 检测到年龄依赖性的皮质和海马萎缩,而 DTI 早在 2.5 个月时就发现了早期白质紊乱,8 个月时轴突结构紊乱明显(Sahara, 2017 年)。TDP-43Q331K基因敲入模型表现出额叶、内侧、运动、眼眶和扣带回皮质以及齿状回和丘脑的萎缩。这些变化反映了早期 ALS-FTD 以及携带C9orf72、MAPT 或GRN突变的患者身上观察到的模式。这些小鼠的脑室扩大率高达 49.7%,反映了在人类遗传性 FTD 携带者身上观察到的症状前模式(Lin,2021 年)。
使用纵向[18F]FDG PET 对TDP-43A315T模型进行补充性代谢成像显示了葡萄糖代谢的特异性区域改变,这与人类 ALS-FTD 非常相似。在单侧运动皮层、躯体感觉皮层和纹状体中观察到低代谢,这可能反映了突触和线粒体功能障碍或神经元缺失。相比之下,在双侧黑质、网状核和杏仁核中检测到高代谢,这可能表明神经炎症和小胶质细胞活化。这些发现与 ALS-FTD 早期的功能生物标志物一致,尤其是约 98% 的 ALS 患者会出现局灶性、不对称的运动功能障碍(Weerasekera, 2020 年)。
在 Biospective,我们的全自动图像处理管道PIANOTM 已被用于分析 FTD 研究中的结构和弥散 MRI。该平台可实现针对特定疾病的干预目标,同时最大限度地减少所需的试验参与者数量,保持统计功率。研究表明,多模态成像--结合结构、弥散和代谢数据--为临床试验中的鉴别诊断、疾病监测和患者分层提供了强有力的工具(Whitwell, 2019)。
欲了解更多信息,请参阅我们的创新演讲:额颞叶痴呆症(FTD)与核磁共振成像脑萎缩、弥散核磁共振成像与额颞叶痴呆症(FTD)以及神经变性小鼠模型的脑萎缩分析。
常见问题
了解更多关于我们的神经退行性疾病模型
相关内容
关于额颞叶痴呆(FTD)的最新信息,以及在神经退行性疾病动物模型中评估治疗药物的最佳实践。
TDP-43——其在肌萎缩侧索硬化症与额颞叶痴呆中的作用
TDP-43概述:其生理功能、在肌萎缩侧索硬化症(ALS)及额颞叶痴呆(FTD)病理中的重要性,以及涉及TDP-43的治疗策略。
额颞叶痴呆症和临床试验中的神经影像学
核磁共振成像和正电子发射断层扫描成像生物标记物在了解额颞叶痴呆(FTD)变体方面的效用,以及它们在FTD临床试验中的终点用途。
ALS小鼠模型用于药物研发
指导如何最有效地使用肌萎缩侧索硬化症(ALS)的实验动物模型(小鼠和大鼠模型)进行临床前治疗测试。