Caractérisation d'un nouveau modèle de souris AAV-hTau pour les tauopathies présentant des caractéristiques parkinsoniennes
Biospective possède une expertise de pointe dans la fourniture de services d'histologie tau, y compris la coloration par immunofluorescence multiplexe (mIF) à l'aide de divers anticorps. Nous disposons de capacités uniques pour mesurer les caractéristiques de la pathologie tau ( par exemple, l'agrégation, la phosphorylation, la conformation, le clivage) et analyser spatialement les relations complexes avec d'autres pathologies (par exemple, les plaques Aβ) et la neuroinflammation associée, y compris les microglies activées et les astrocytes réactifs.
Table des matières
- Quels sont les services de recherche sous contrat proposés par Biospective pour la coloration et l'analyse de la protéine Tau ?
- Quel est le flux de travail de Biospective pour la coloration et l'analyse quantitative de la protéine Tau ?
- Exemple de coloration et d'analyse de la protéine Tau mIF dans un modèle murin de tauopathie 4R
Quels sont les services de recherche sous contrat proposés par Biospective pour la coloration et l'analyse de la protéine Tau ?
Coloration par immunofluorescence multiplex, segmentation, analyse morphologique et spatiale de la protéine tau dans des coupes de tissus provenant de modèles de rongeurs atteints de la maladie d'Alzheimer et d'autres tauopathies.
Biospective fournit une caractérisation de bout en bout des agrégats de tau et des réponses gliales en utilisant la coloration tissulaire par immunofluorescence multiplex avancée (mIF), l'imagerie haute résolution de la lame entière et l'analyse morphologique automatisée basée sur l'apprentissage automatique et l'apprentissage profond.
Nos capacités de coloration Tau et d'analyse d'images
Coloration de la protéine Tau et multiplexage
Nous proposons des colorations IHC/mIF utilisant une grande variété d'anticorps, notamment
Tau non phosphorylée : Tau15-25, Tau1-100, HT7
Tau phosphorylée : AT8, PHF1, CP13, pTau-217
Tau clivée : N368, Asp421
Conformation de la maladie : MC-1
Structure des fibrilles amyloïdes : pFTAA
Nous développons continuellement des protocoles pour d'autres anticorps et nous disposons d'excellentes capacités pour la mise en œuvre de marqueurs personnalisés.
Pour obtenir une image plus complète des processus pathologiques dans les coupes de tissus, nous disposons d'une grande expertise en matière de coloration à l'aide de panels IF multiplex.
Quantification et analyse des images
Nous effectuons la quantification de la densité des colorations IHC/mIF sur des lames entières et la quantification de la charge régionale dans des régions d'intérêt spécifiques.
Nous pouvons également effectuer des analyses spatiales complexes pour étudier les relations entre les protéines mal repliées, la neuroinflammation et la neurodégénérescence.
Quel est le flux de travail de Biospective pour la coloration et l'analyse quantitative de la protéine Tau ?
Protocoles bien établis pour la préparation des échantillons de cerveau, la coloration, le balayage des lames et l'analyse quantitative des images.
Notre processus de coloration et d'analyse de la protéine tau
Chez Biospective, nous avons mis en place un processus standardisé et hautement reproductible en plusieurs étapes pour la coloration et l'analyse de la protéine tau à partir de cerveaux fixés au formol :
Préparation de l'échantillon
coupe microtomique de haute précision ou cryosectionnement de cerveaux FFPE ou fixés et congelés.
Protocoles de récupération d'antigènes personnalisés, optimisés pour chaque anticorps spécifique à la protéine tau, garantissant une liaison de haute affinité et la préservation de la morphologie de la protéine tau. Les conditions de récupération sont également personnalisées pour tout anticorps supplémentaire inclus dans le panel multiplex. Nous effectuons systématiquement une récupération induite par la chaleur (HIER), une récupération enzymatique, une récupération par l'acide formique ou une combinaison de ces méthodes.
Contrôle de qualité rigoureux de la qualité et de la spécificité de la coloration ainsi que de l'intégrité des tissus.
Coloration (IHC ou IF multiplex)
Marqueurs Tau
Marqueurs du microenvironnement pathologique
Microglie(Iba-1 et autres marqueurs microgliaux)
Astrocytes (GFAP)
Neurones (NeuN ; marqueurs de sous-type neuronal, par exemple TH pour les neurones dopaminergiques)
Autres protéines mal repliées(par exemple, plaques amyloïdes-β, α-synucléine, TDP-43)
Marqueurs subcellulaires et biochimiques(par ex. lysosomes, autophagie, mitochondries, neurodégénérescence)
DAPI (noyaux)
Avantages du multiplexage
Le multiplexage permet une analyse spécifique du type de cellule du microenvironnement sur une seule lame, caractérisant avec précision le paysage cellulaire entourant les plaques individuelles.
Imagerie
Balayage fluorescent multicanal de la section entière
Analyse quantitative
Nous avons développé une analyse quantitative entièrement automatisée pour l'immunofluorescence multiplex afin de compléter l'analyse de la protéine tau, y compris la segmentation et le comptage des plaques de bêta-amyloïde, l'analyse de la morphologie des cellules gliales et l'analyse du microenvironnement.
Illustration du processus de Biospective consistant à prélever des échantillons de tissus cérébraux sur des modèles animaux, à effectuer des coupes de tissus, des colorations par immunofluorescence multiplex, à scanner des lames entières et à procéder à une analyse quantitative des images.
Lignes directrices pour le prélèvement, la préparation et l'expédition des échantillons
Nous fournissons une assistance complète pour garantir l'intégrité des échantillons et la fiabilité des données :
Collecte des échantillons : Les animaux doivent être perfusés avec du PBS froid et/ou du formol tamponné neutre à 10 %, et les cerveaux doivent être soigneusement extraits.
Préparation des échantillons : Les cerveaux doivent être brièvement fixés dans du formol neutre à 10 %
Expédition des échantillons : Les échantillons doivent être expédiés dans du PBS contenant de l'azoture de sodium.
Exemple de coloration et d'analyse de la protéine Tau mIF dans un modèle murin de tauopathie 4R
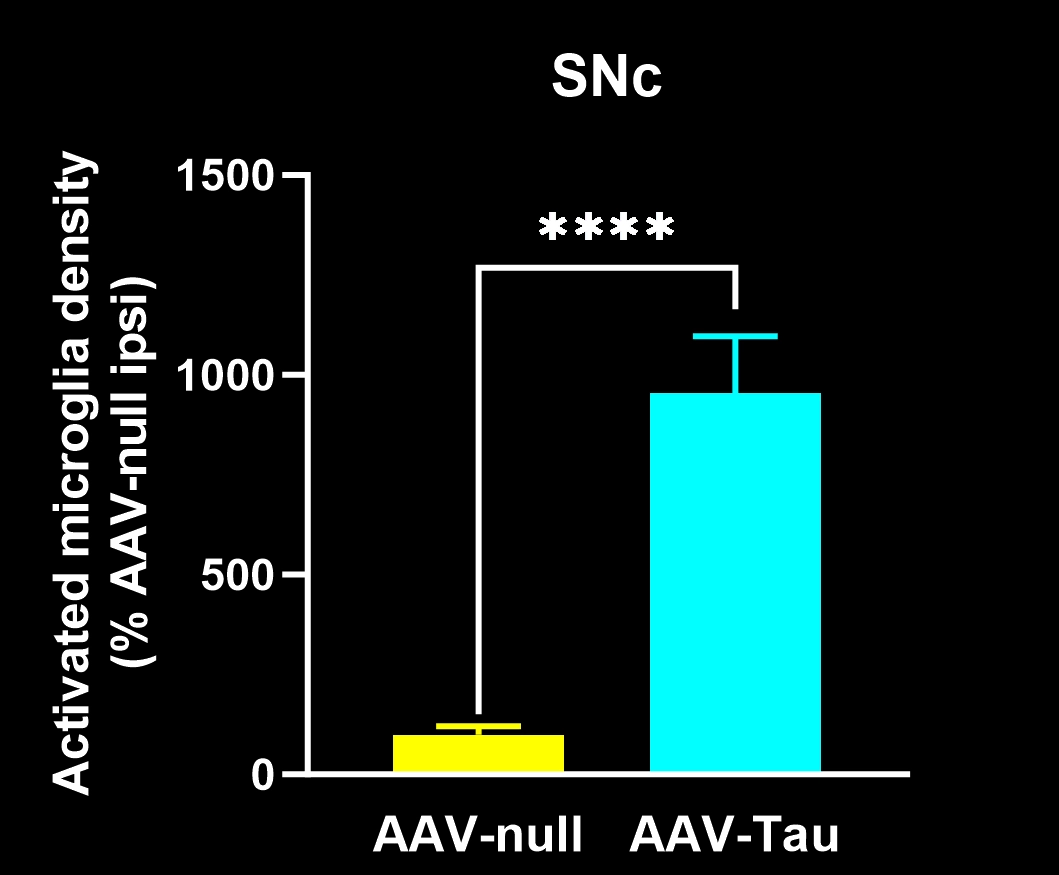
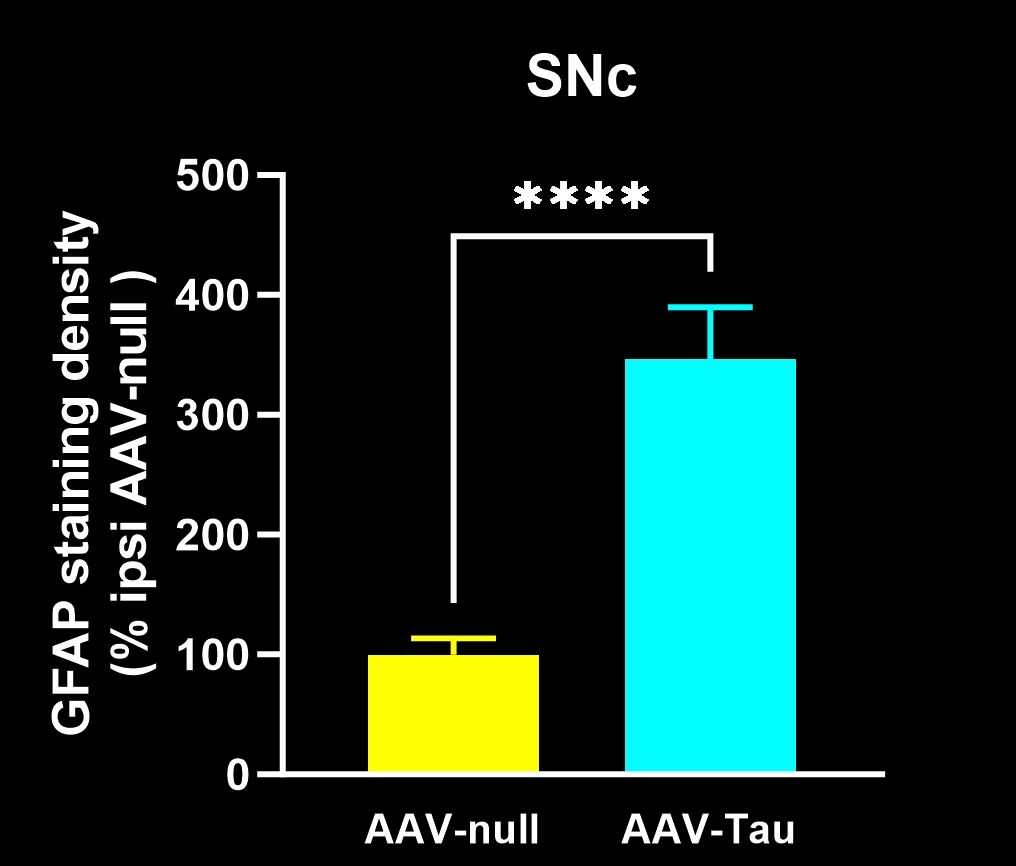
Exemple de pathologie tau, de neuroinflammation et de neurodégénérescence dans un modèle murin de PSP et de CBD.
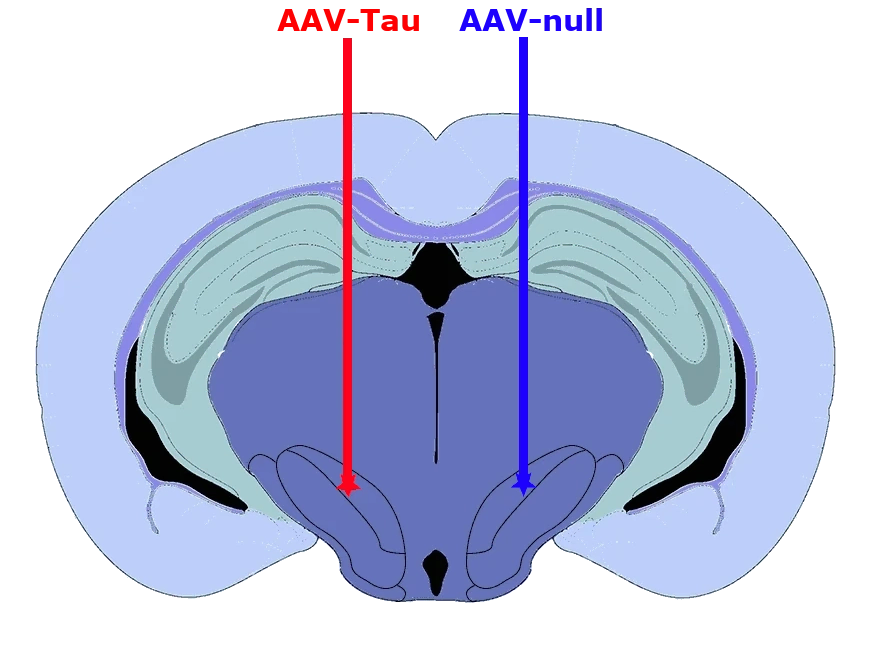
Biospective a développé un modèle unique de souris de la Tauopathie 4R, qui inclut un dysfonctionnement dopaminergique et des déficits moteurs. Nous avons largement validé ce modèle en utilisant une large gamme d'essais in vivo et ex vivo, y compris divers biomarqueurs translationnels pour servir de plateforme pour l'évaluation d'agents thérapeutiques. Nous avons tiré parti de notre portefeuille de marqueurs tau et de panels IF multiplex pour caractériser la neuropathologie chez ces souris.
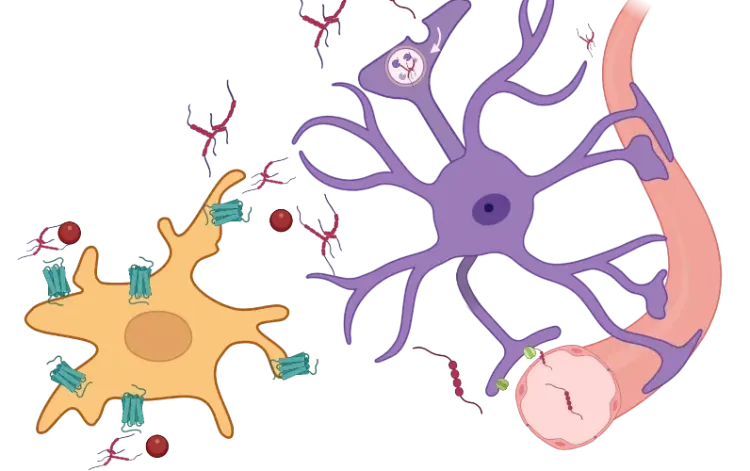
Images représentatives d'immunofluorescence multiplex de la protéine tau neuronale intracellulaire colorée par divers anticorps pour la protéine tau phosphorylée et/ou clivée dans des coupes de tissus cérébraux de souris. La microglie et les astrocytes sont également colorés dans ces images.
Dans notre caractérisation de ce modèle, nous avons trouvé :
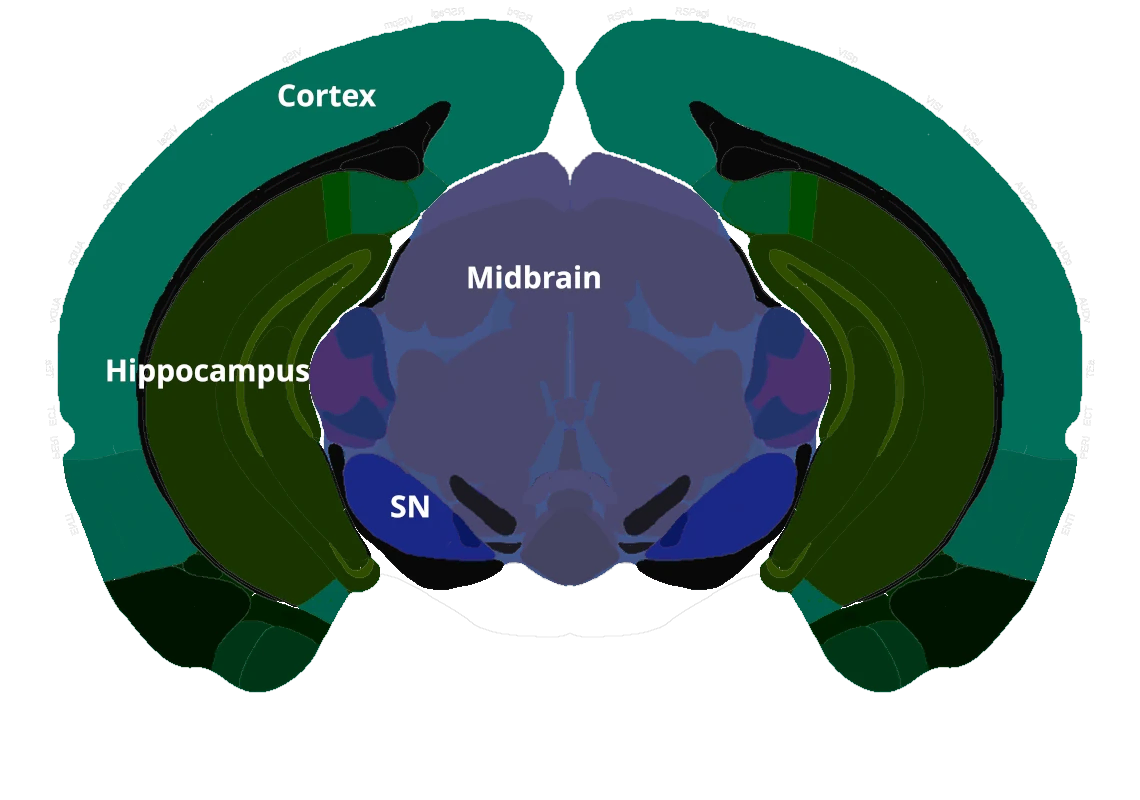
Des agrégats de tau phosphorylés dans la substantia nigra et le mésencéphale.
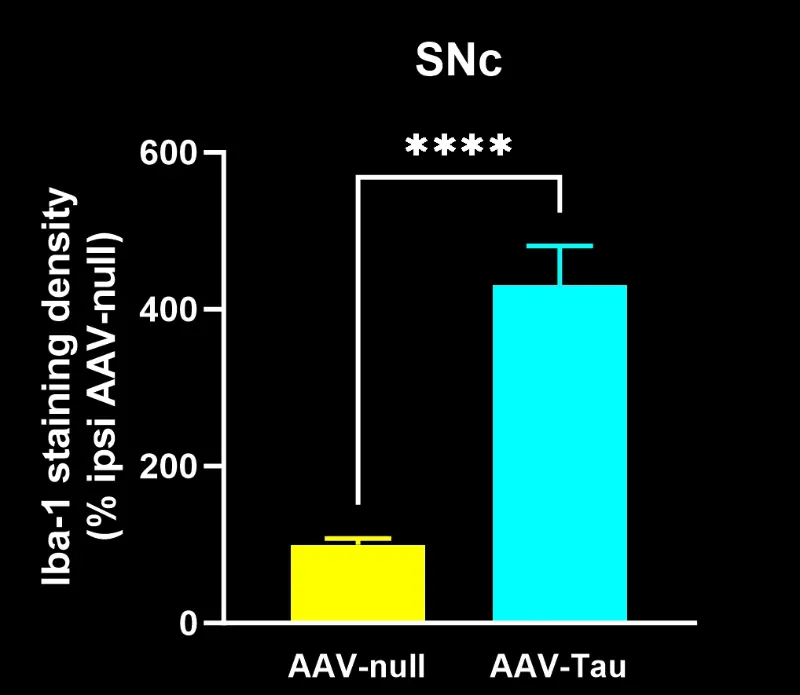
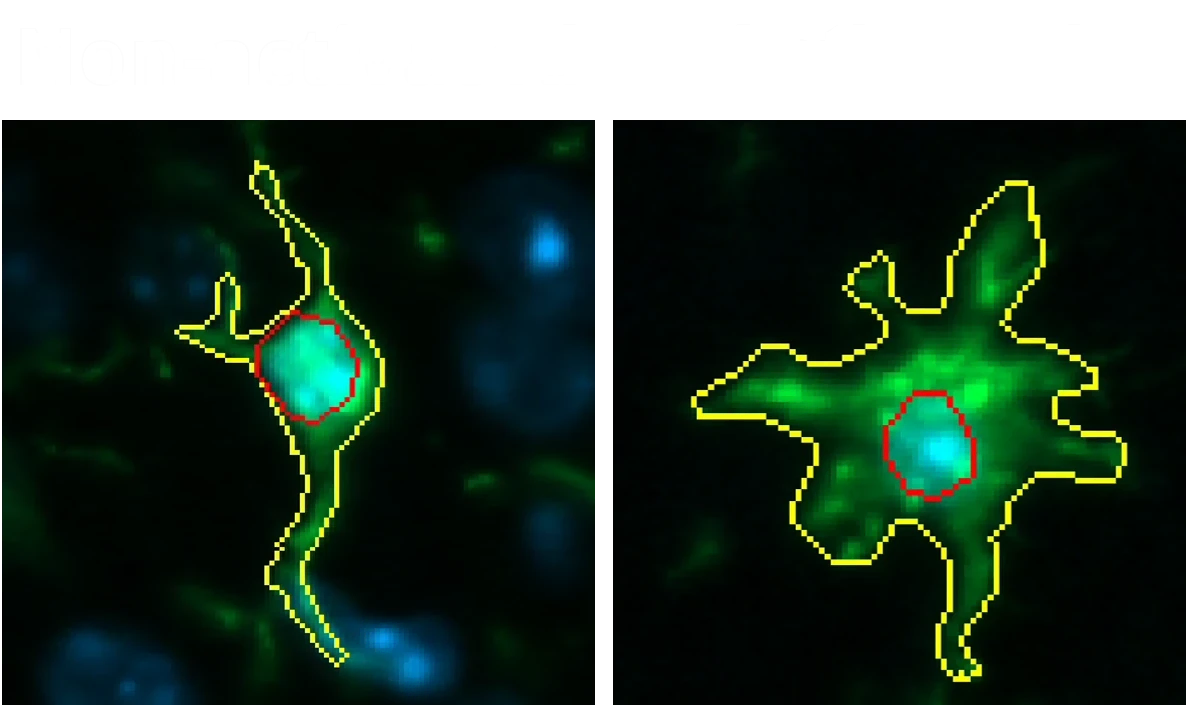
Des microglies activées et des astrocytes réactifs à proximité des inclusions tau intracellulaires.
Perte de neurones dopaminergiques dans la substantia nigra pars compacta.
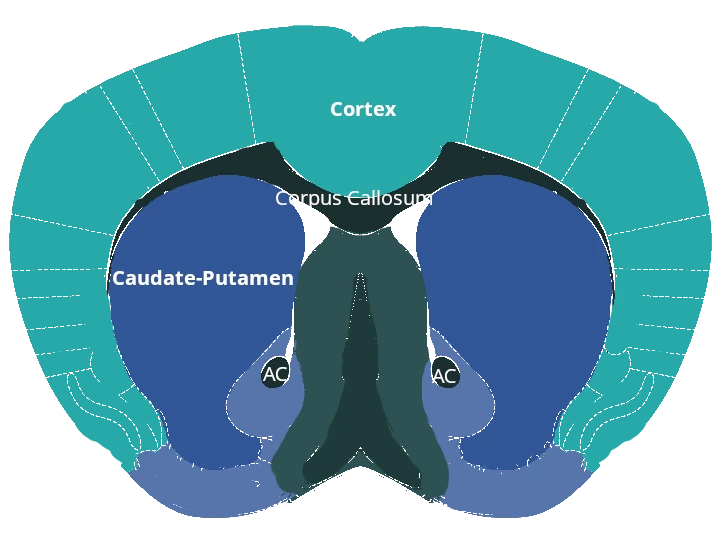
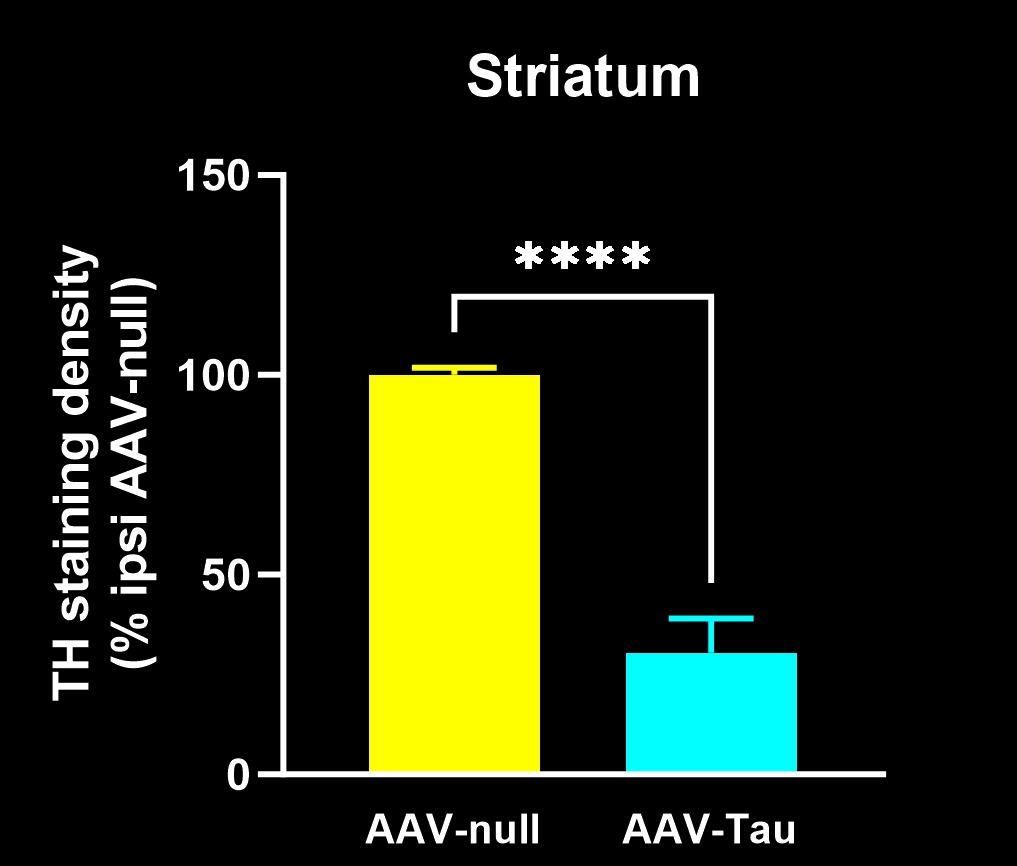
Réduction des terminaux dopaminergiques dans le caudé-putamen.
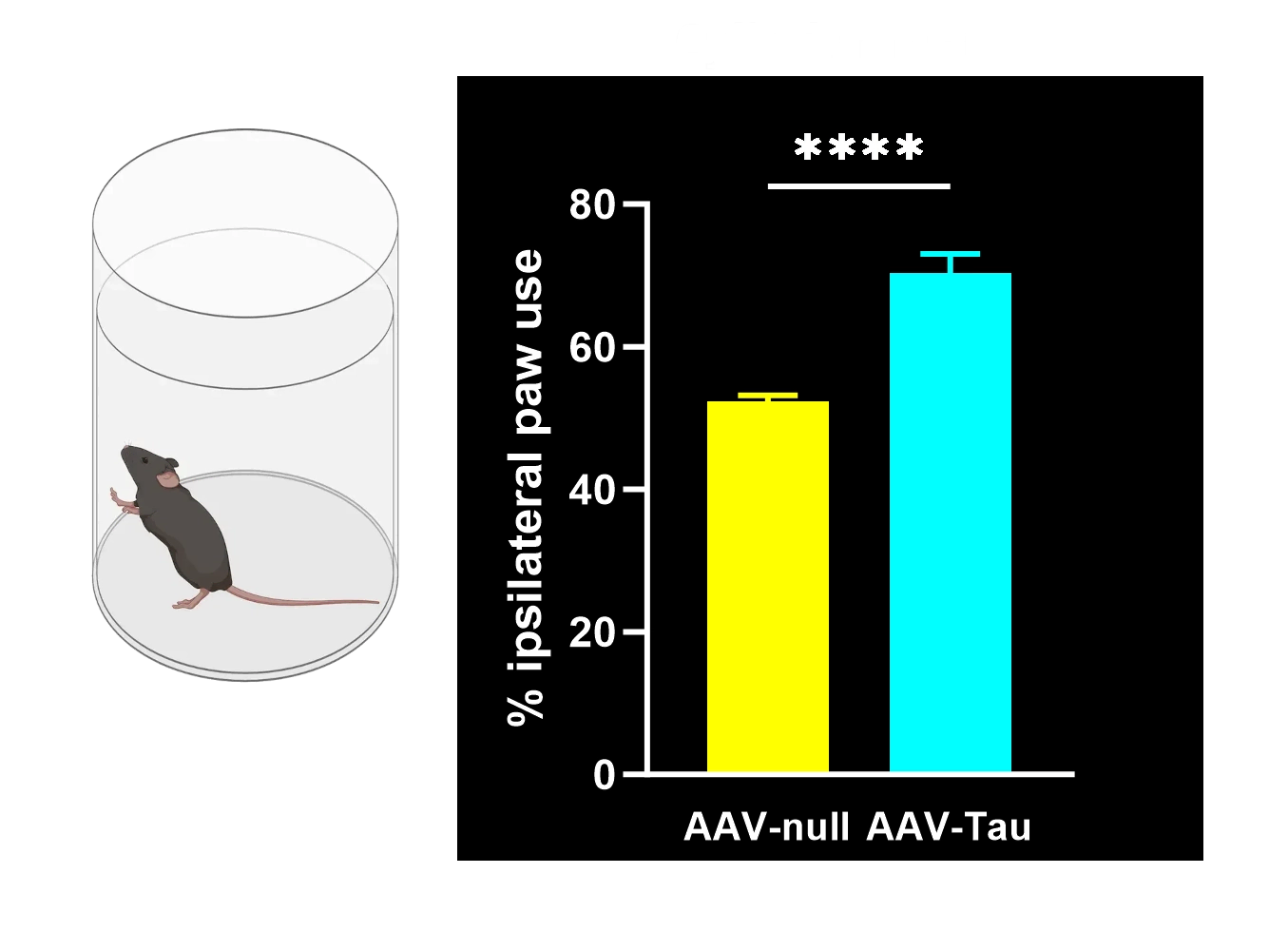
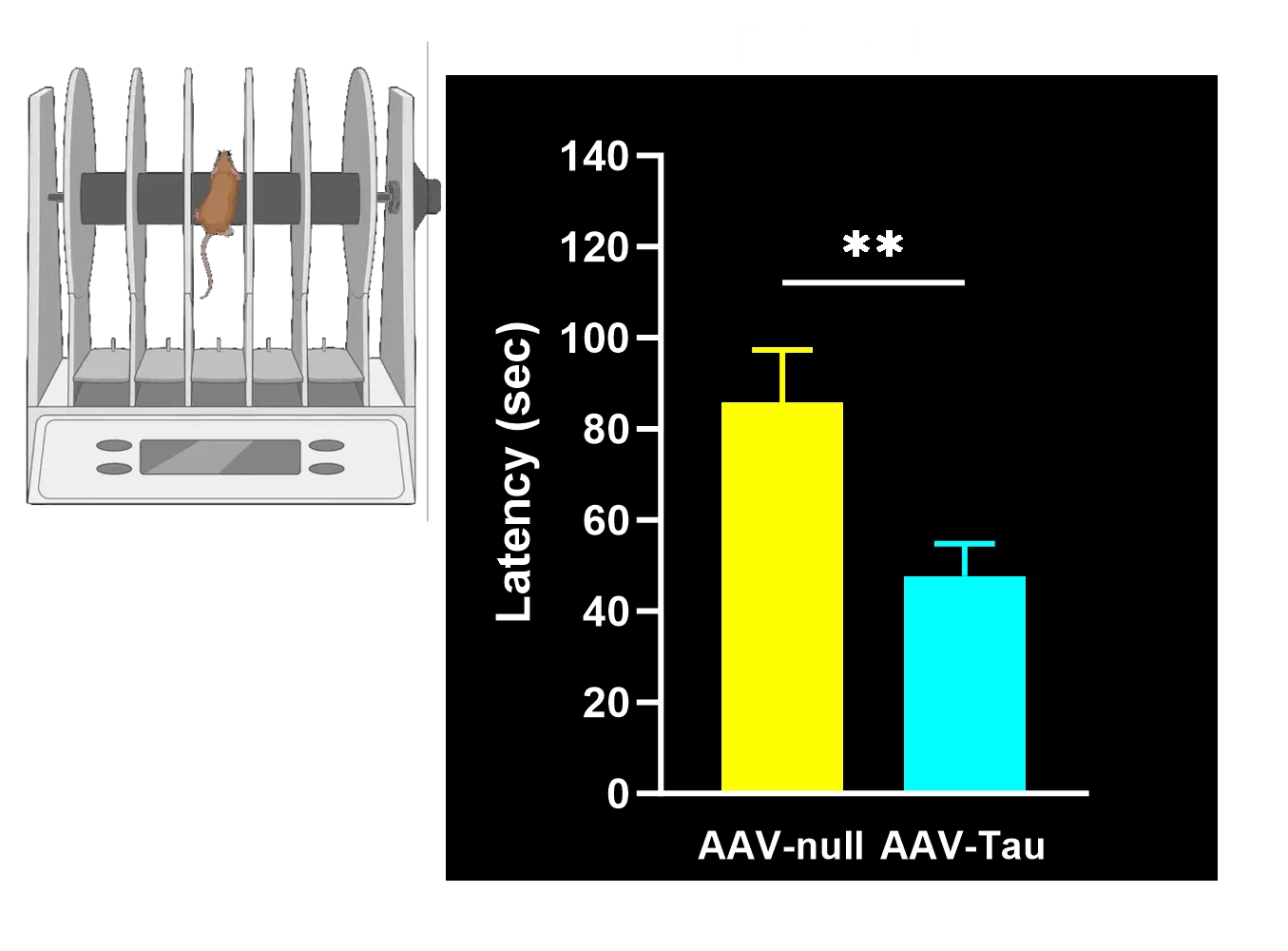
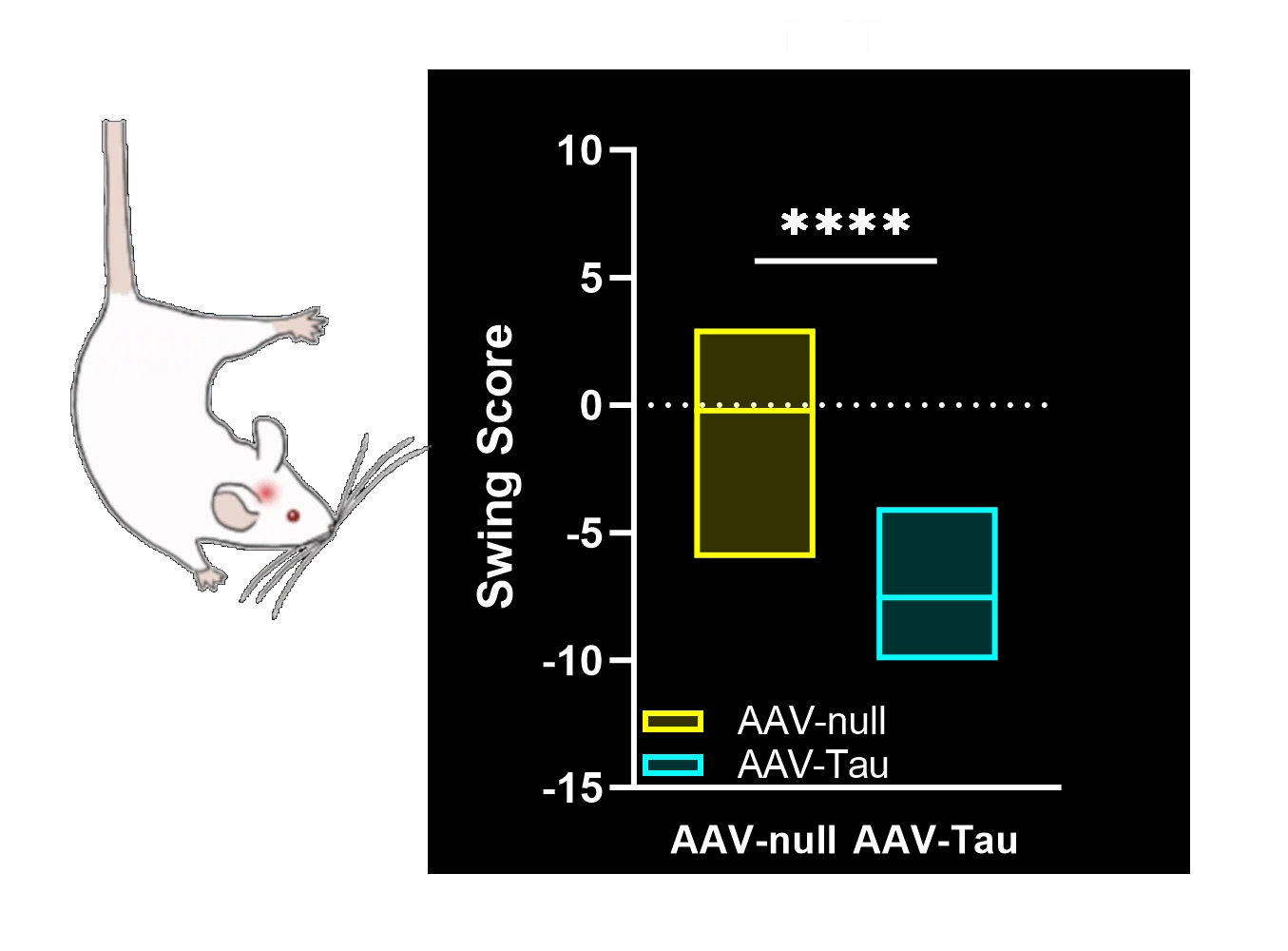
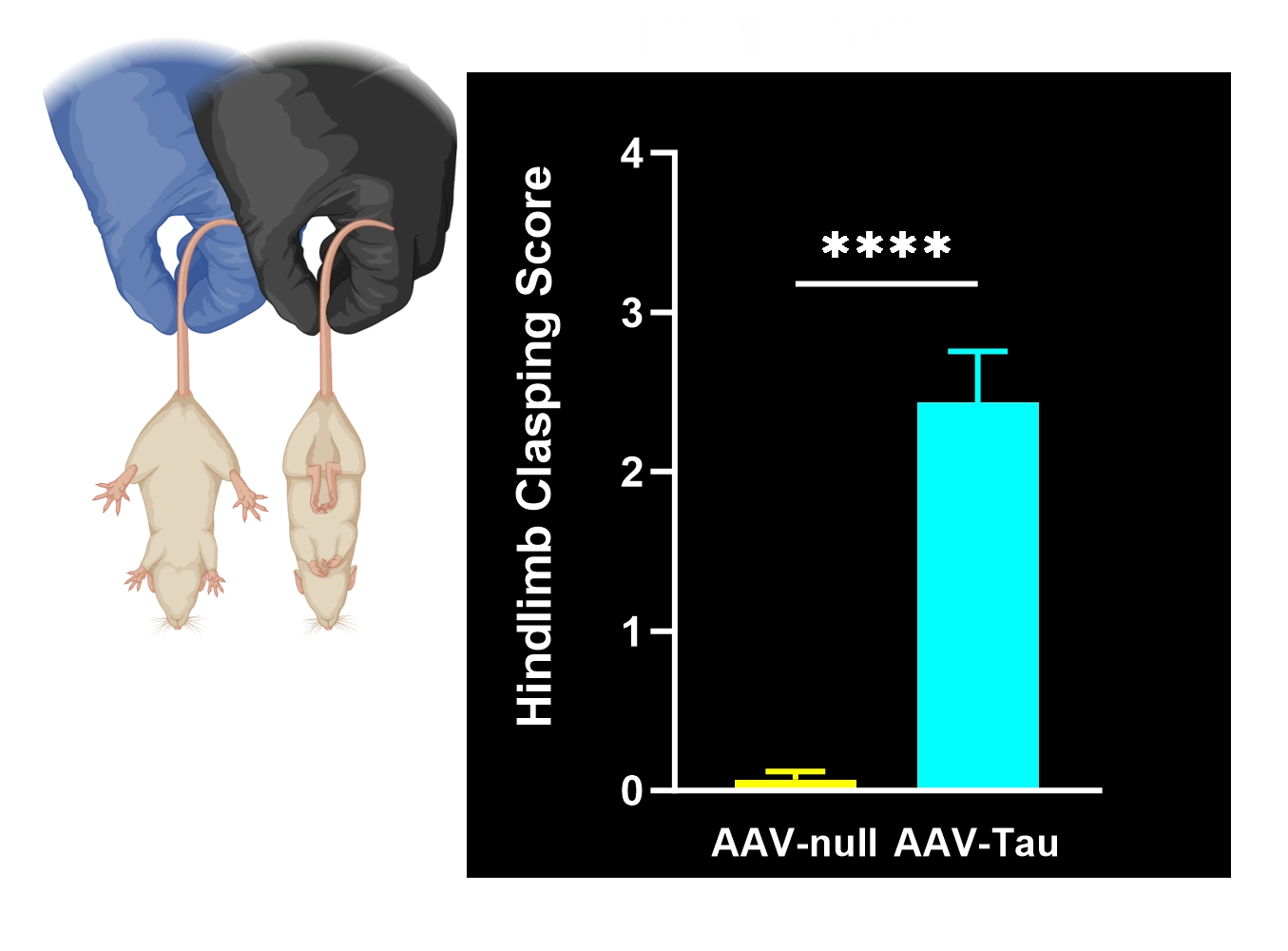
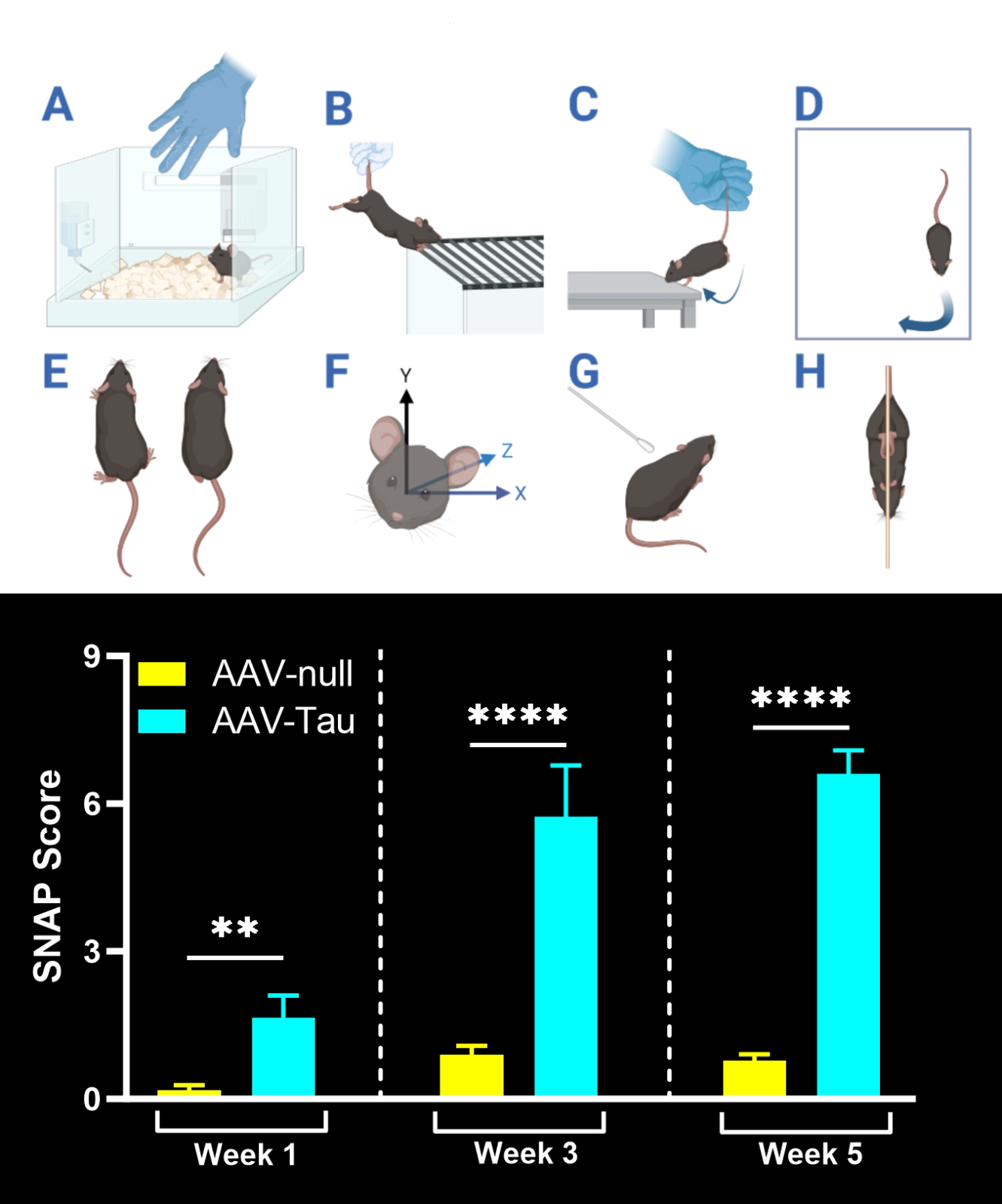
Déficits moteurs mesurés par l'agrippement des membres postérieurs, le test du cylindre, le rotarod, le test de suspension de la queue et les scores SNAP.
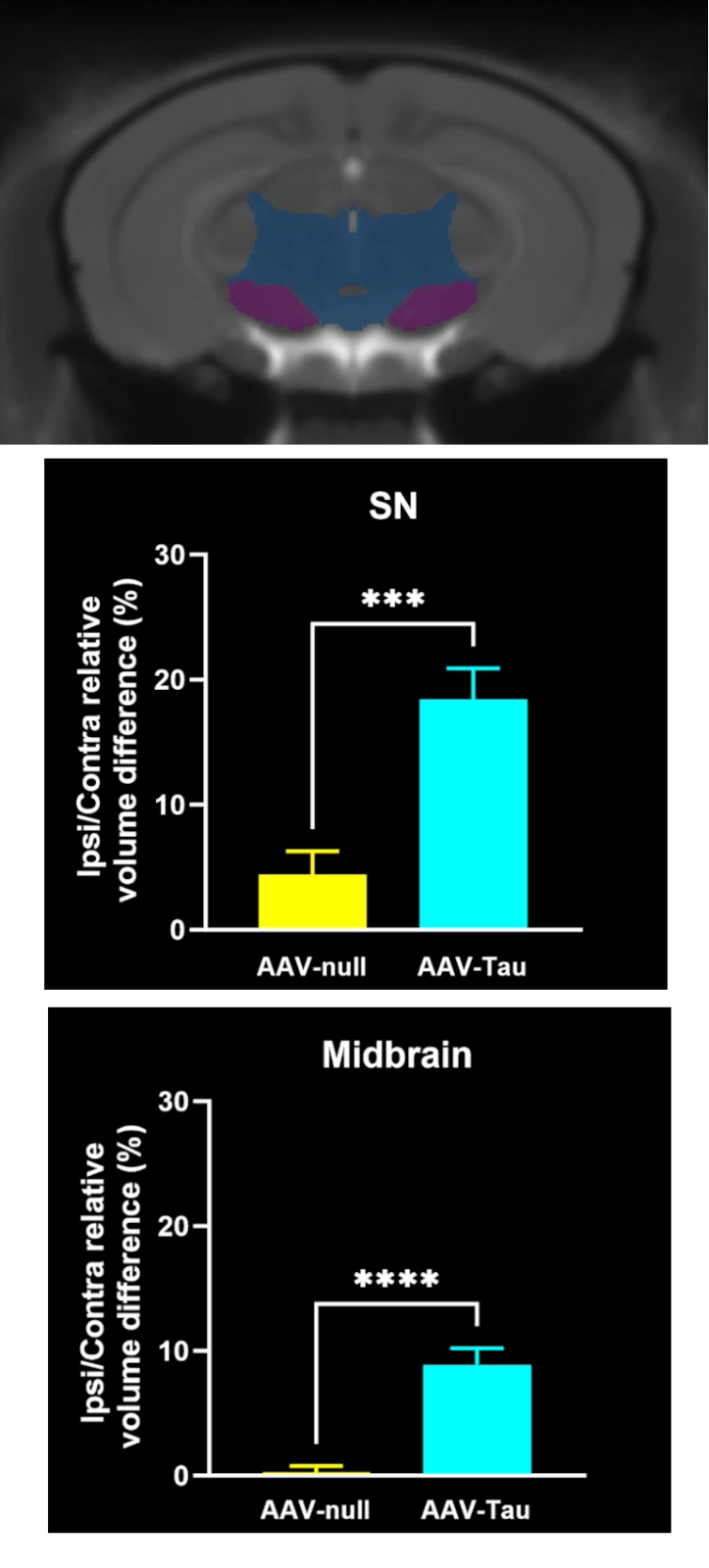
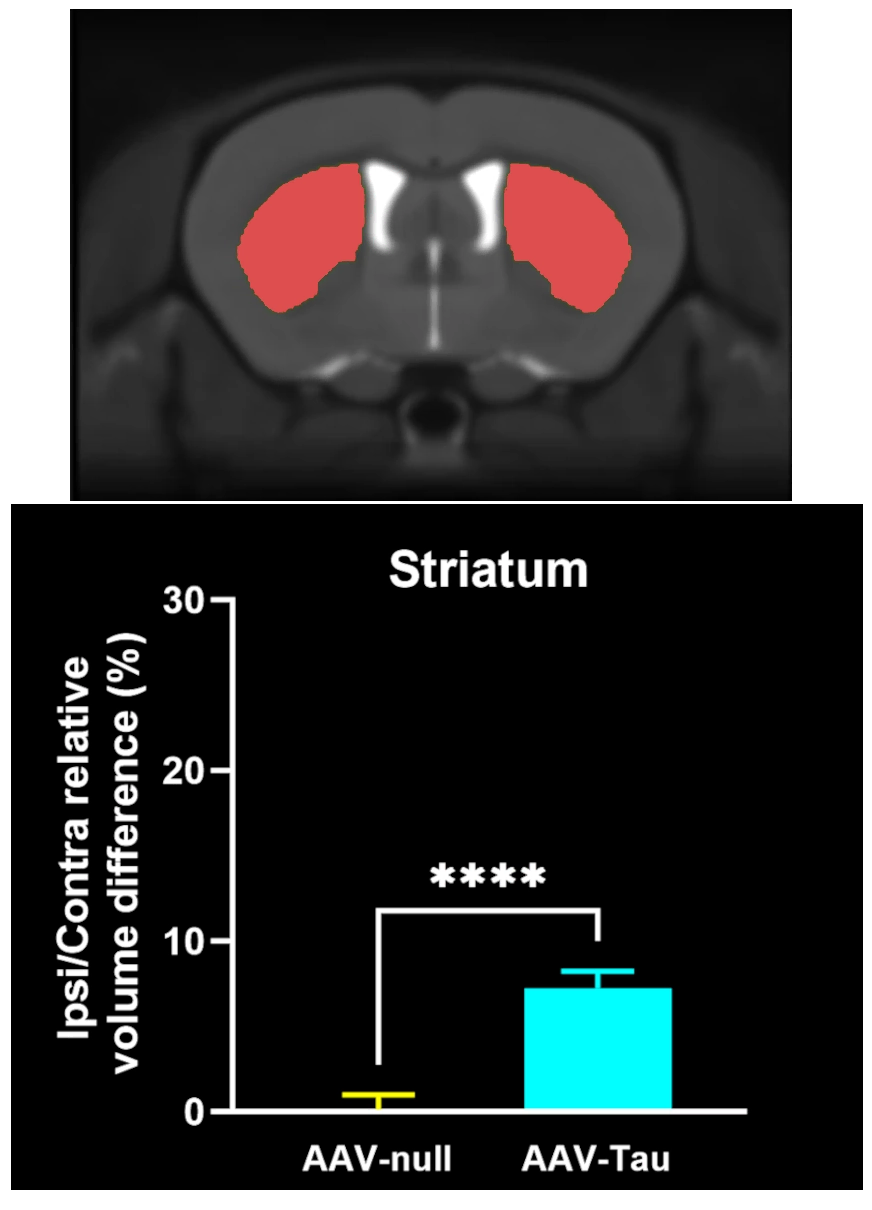
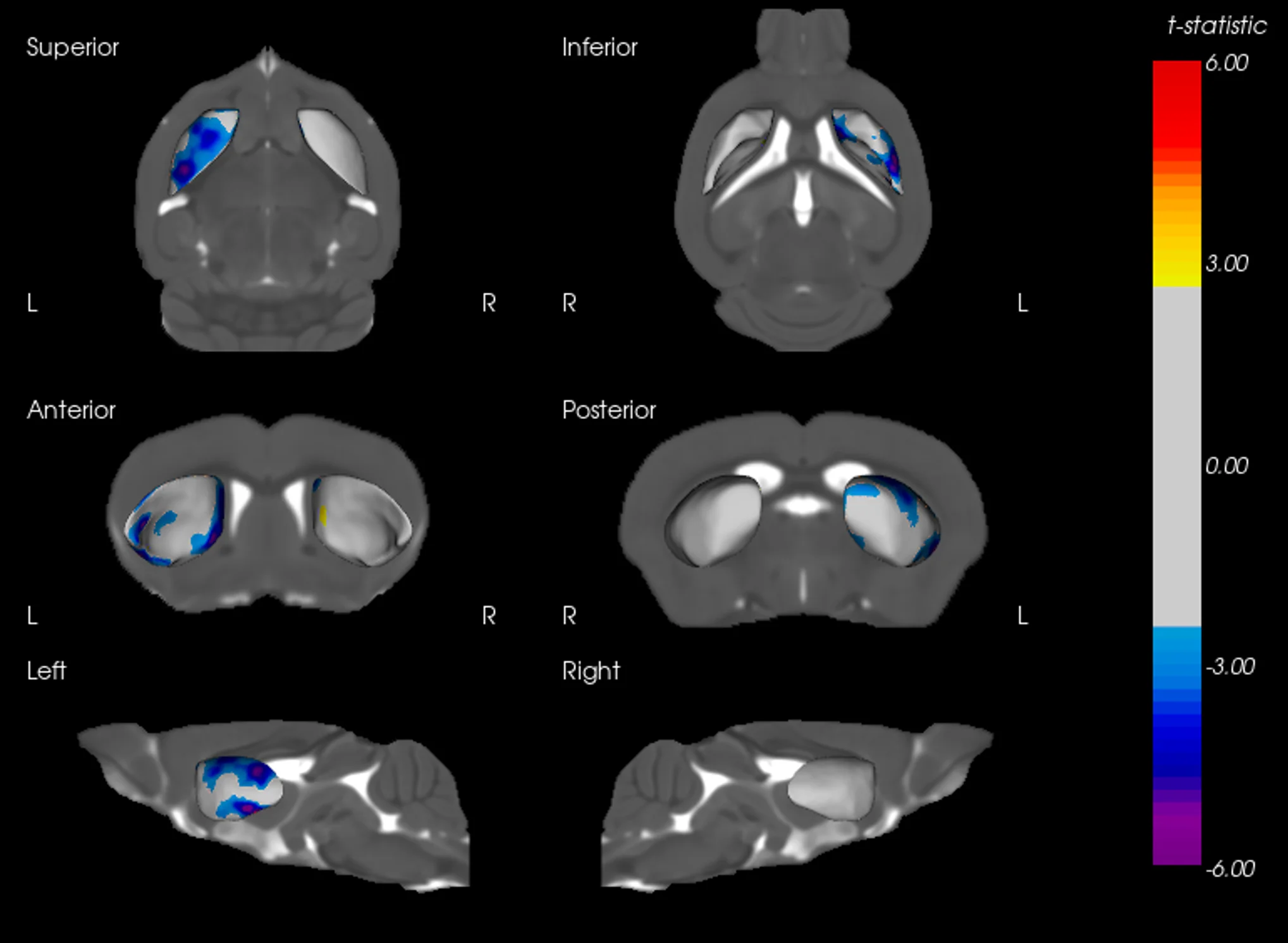
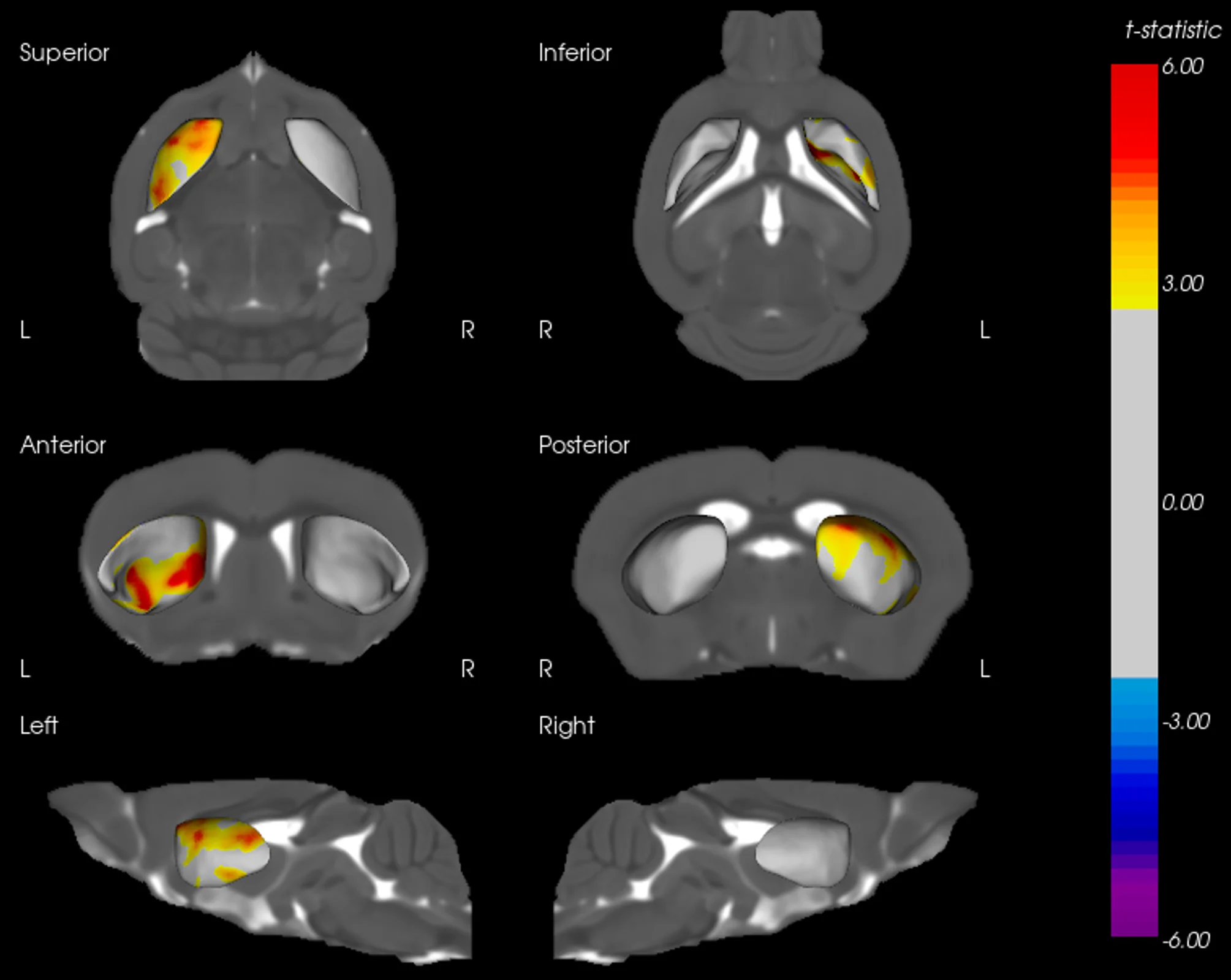
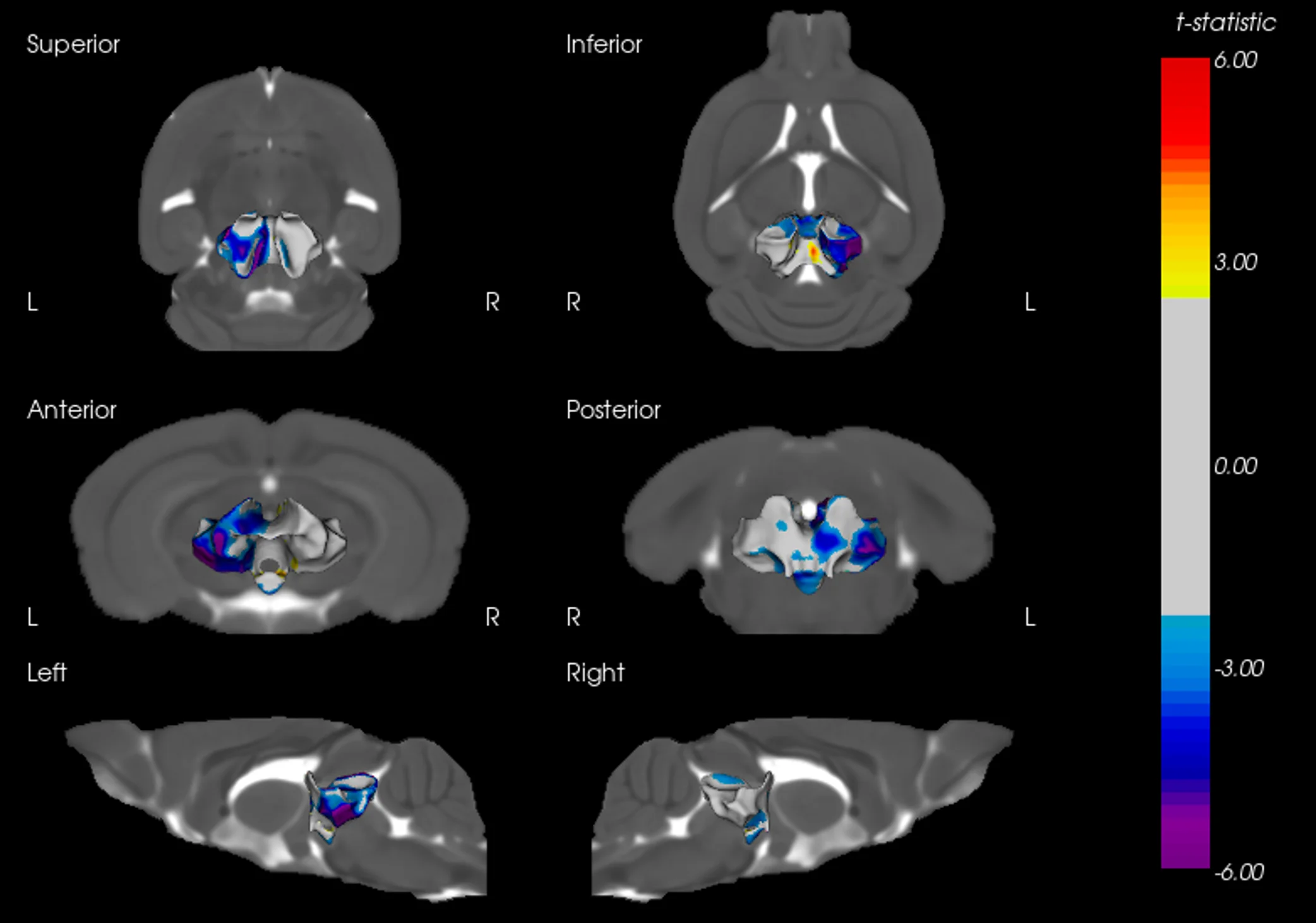
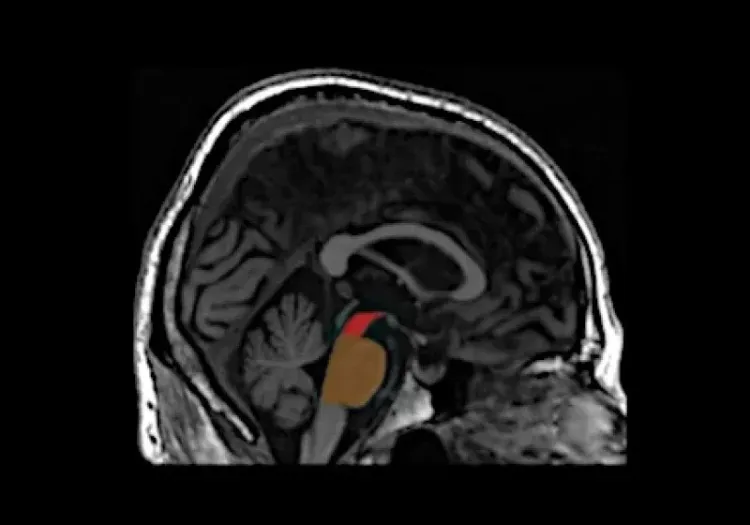
Atrophie cérébrale régionale à l'IRM dans la substantia nigra, le mésencéphale et le striatum.
Concentrations élevées de la chaîne légère des neurofilaments (NfL) dans le plasma.
Présentation interactive de notre étude de recherche
Dans l'"Image Interactive" ci-dessous, vous trouverez les résultats de notre caractérisation complète et multimodale de notre modèle de souris atteinte de tauopathie, y compris des coupes de tissus cérébraux par immunofluorescence multiplex à haute résolution.
Comment utiliser notre visionneuse interactive
Naviguez dans l'"histoire de l'image" à l'aide du panneau de gauche ou des flèches à l'écran. Vous pouvez effectuer un panoramique sur les images de microscopie à haute résolution à l'aide de votre souris et effectuer un zoom avant/arrière en utilisant la molette de défilement ou les commandes +/-. Le panneau de contrôle (en haut à droite) permet de basculer entre les canaux d'images et les superpositions de segmentation. Pour une expérience optimale, nous vous recommandons de passer en mode plein écran. Cette présentation interactive vous permet d'explorer en détail la neuropathologie du modèle et les déficits fonctionnels qui y sont associés, comme si vous regardiez directement au microscope.
Image interactive illustrant la coloration et l'analyse de la protéine tau, y compris des coupes de tissus cérébraux en immunofluorescence multiplex à haute résolution, provenant de notre modèle de souris 4R atteintes de tauopathie et de souris témoins. Cette présentation met en évidence nos capacités de coloration IF de la protéine tau et d'analyse d'images.
Principaux avantages des services de coloration et d'analyse de la protéine tau de Biospective :
Détection de la protéine tau à haute sensibilité
Coloration personnalisée d'anticorps/marqueurs
Imagerie automatisée à haut débit de la lame entière et analyse des régions neuroanatomiques
Caractérisation et quantification de la protéine tau
Analyse de la morphologie et du phénotype des cellules gliales
Mesures avancées de la neuroinflammation et de l'environnement de la plaque Aβ - très sensibles aux petits changements dans la progression de la maladie
Compatibilité inter-espèces (souris, rat)
Services complémentaires (par exemple, biomarqueurs liquides mesurés par immunoessais)
Nous contacter CTA
Pour discuter des exigences de votre étude ou demander un devis pour les services de coloration Tau et d'analyse d'images :
FAQ
FAQ
Mots clés
Contenu connexe
Informations récentes sur les microglies et la neuroinflammation.
Modèle de souris PS19 pour le développement de médicaments ciblant la protéine tau
Présentation générale des souris PS19 (P301S) en tant que modèle transgénique pour l'évaluation préclinique des traitements modificateurs de la maladie ciblant la formation et la propagation des agrégats de protéine tau.
Microglie, astrocytes et protéine tau dans les maladies neurodégénératives
Comment la neuroinflammation induite par les cellules gliales favorise l'agrégation et la propagation de la protéine tau ainsi que la perte neuronale dans la maladie d'Alzheimer et d'autres tauopathies.
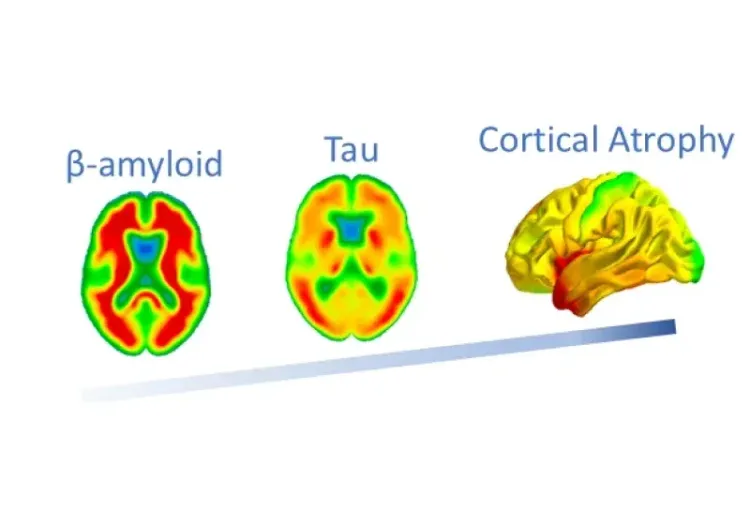
L'atrophie liée à la protéine Tau est indépendante de la β-amyloïde et de l'APOE ε4
En utilisant les biomarqueurs d'imagerie IRM, Tau PET et Amyloid PET de l'étude ADNI, nous montrons que la protéine Tau est plus fortement liée à l'atrophie cérébrale que la β-amyloïde ou l'APOE ε4.
La diminution du métabolisme du glucose cérébral dans la DCL est induite par la protéine Tau
Nous démontrons un rôle plus important de la protéine tau que de la β-amyloïde dans la réduction du métabolisme cérébral du glucose en analysant les images TEP de l'étude ADNI.
Mesures IRM de la progression de la maladie pour les essais cliniques sur la PSP
Biomarqueurs IRM (y compris l'atrophie cérébrale) issus des études 4RTNI et FTLDNI sur l'histoire naturelle de la paralysie supranucléaire progressive (PSP).
IRM et dégénérescence corticobasale (CBD)
Mesures longitudinales de l'atrophie cérébrale par IRM provenant des études 4RTNI et FTLDNI, y compris le calcul de la taille des échantillons pour les essais cliniques sur la dégénérescence corticobasale.
Interactions entre les microglies et les neurones et maladies neurodégénératives
Une revue concise des interactions directes entre les microglies et les neurones, et de la manière dont ces interactions intercellulaires peuvent être affectées dans les maladies neurodégénératives.
Amyloïde-β et microenvironnement inflammatoire chez la souris Alzheimer
Nous avons analysé les relations spatiales complexes entre les plaques β-amyloïdes, la microglie activée et au repos, et les astrocytes dans un modèle transgénique APP/PS1.
Activation microgliale dans un modèle de souris PFF à α-synucléine
Nous avons quantifié l'activation microgliale, sur la base de la morphologie, dans un modèle murin d'ensemencement et d'étalement de fibrilles préformées d'α-synucléine (PFF) de la maladie de Parkinson.
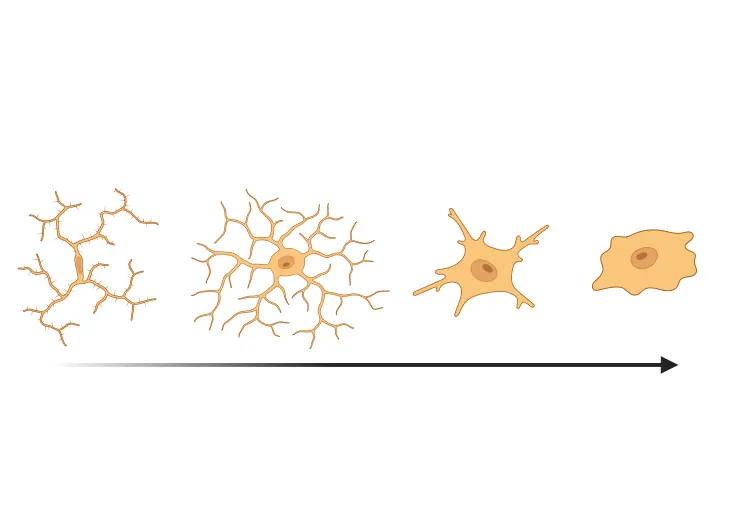
Morphologie de la microglie dans la SLA, la maladie d'Alzheimer et la maladie de Parkinson
Une vue d'ensemble de l'analyse morphologique des microglies et des applications à la recherche sur les maladies neurodégénératives et à la découverte et au développement de médicaments.
Dysfonctionnement mitochondrial dans les microglies et les astrocytes
Le rôle du dysfonctionnement mitochondrial dans les microglies et les astrocytes dans les maladies neurodégénératives, notamment la maladie d'Alzheimer, la maladie de Parkinson et la SLA.
Dysfonctionnement lysosomal dans les microglies et les astrocytes
Un aperçu du dysfonctionnement lysosomal dans la microglie et les astrocytes, et de son rôle dans les maladies neurodégénératives.
Inflammasome NLRP3 et maladies neurodégénératives
Un aperçu de l'inflammasome NLRP3 et de son rôle dans les maladies neurodégénératives, notamment la maladie d'Alzheimer, la maladie de Parkinson et la SLA.
Altération de l'autophagie de la microglia dans les maladies neurodégénératives
Comment l'altération de l'autophagie microgliale contribue à la progression des maladies neurodégénératives.
TNF-α et microglie dans les maladies neurodégénératives
Un aperçu de la fonction du facteur de nécrose tumorale alpha (TNF-α) dans la microglie et de sa contribution à la progression de la neurodégénérescence.