Nos services de coloration et d'analyse par immunofluorescence (IF)
Chez Biospective, les membres de notre équipe sont spécialisés dans les domaines suivants :
- Coloration immunofluorescente multiplexe
- Numérisation fluorescente de lames entières
- Analyse quantitative automatisée de coupes tissulaires
En tant qu'organisme de recherche sous contrat spécialisé dans les neurosciences précliniques, Biospective fournit des services de recherche pour la coloration et l'analyse par immunofluorescence multiplexe aux domaines suivants :
- Industrie biotechnologique
- Les sociétés pharmaceutiques
- Les instituts et laboratoires de recherche
Nous sommes spécialisés dans la coloration et l'analyse des tissus suivants :
- Cerveaux
- Médullaire
- Muscles
- Nerfs périphériques
- Ganglions
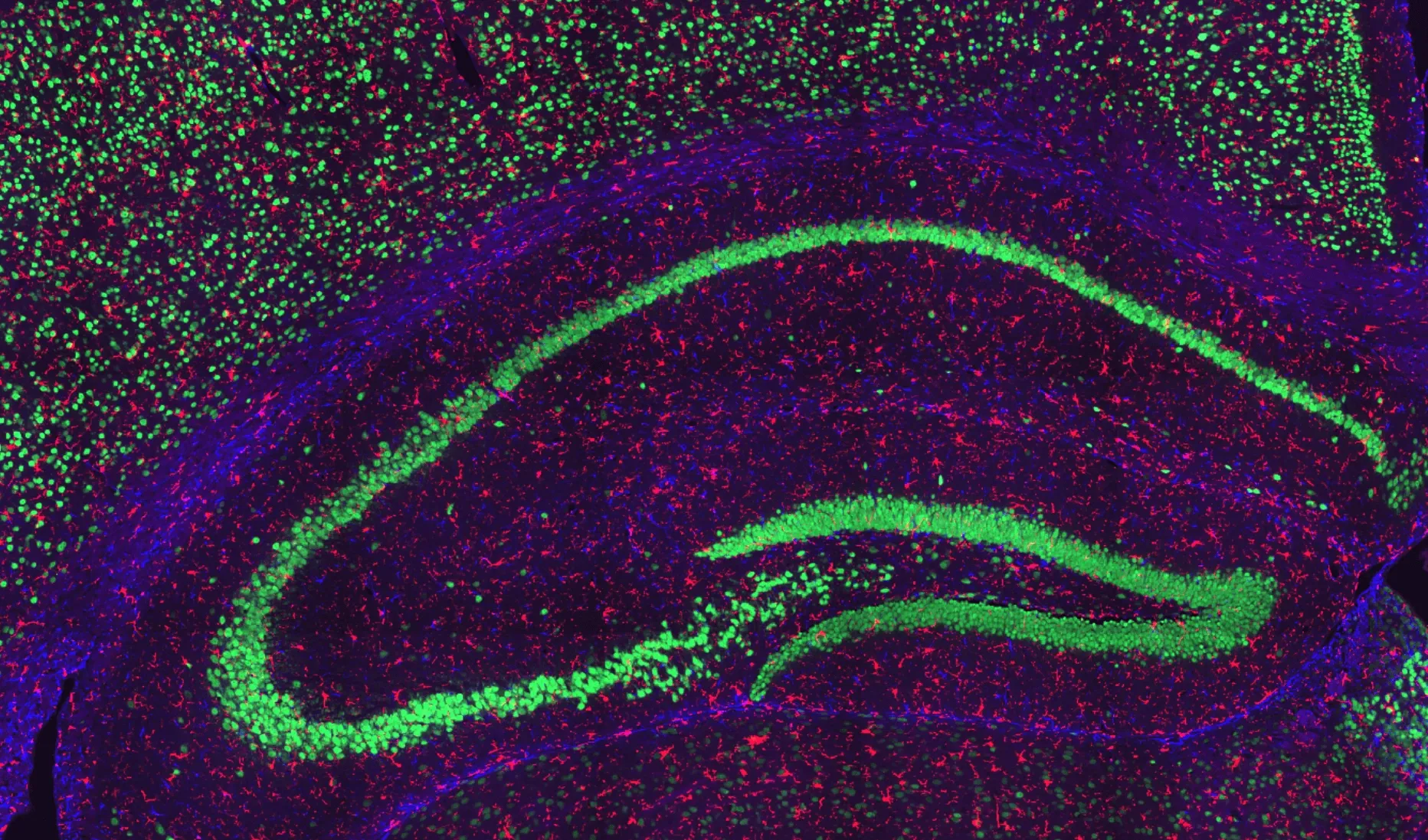
Marquage neuronale et gliale dans l'hippocampe d'une souris de type sauvage.
Région représentative de l'hippocampe d'une coupe coronale provenant d'unesourisde type sauvage .Les neurones NeuN-positifs sont visualisés en vert, les astrocytes GFAP-positifs en bleu etles microglies Iba1-positives en rouge, les noyaux étant contre-colorés à l'aide de DAPI. Cette marquage met en évidence les populations neuronales ainsi que la distribution des astrocytes et des microglies dans l'hippocampe.
Nos laboratoires utilisent des instruments de marquage immunofluorescente automatisés de pointe à haut débit et des scanners de lames entières afin d'optimiser la qualité et de réduire les délais d'exécution.
Si vous prélevez des échantillons de cerveau, de moelle épinière, de muscles, de nerfs périphériques ou de ganglions dans le cadre de vos études internes ou d'études sur des modèles animaux réalisées avec un autre fournisseur, vous pouvez simplement nous les envoyer pour la marquage, la numérisation des lames et l'analyse des images .
Études d'immunofluorescence multiplexe à partir de modèles de maladies neurologiques
Chez Biospective, nous menons régulièrement des études sur des modèles murins de SLA, de maladie d'Alzheimer et de tauopathies, de maladie de Parkinson et de sclérose en plaques (SEP). Nous vous proposons ici des exemples illustratifs de nos marquages par immunofluorescence multiplexe à partir de ces modèles. Vous pouvez également en savoir plus sur nos services d'immunofluorescence multiplexe (mIF) pour ces modèles en utilisant les liens fournis.
Marquage mIF dans des modèles murins de SLA (sclérose latérale amyotrophique)
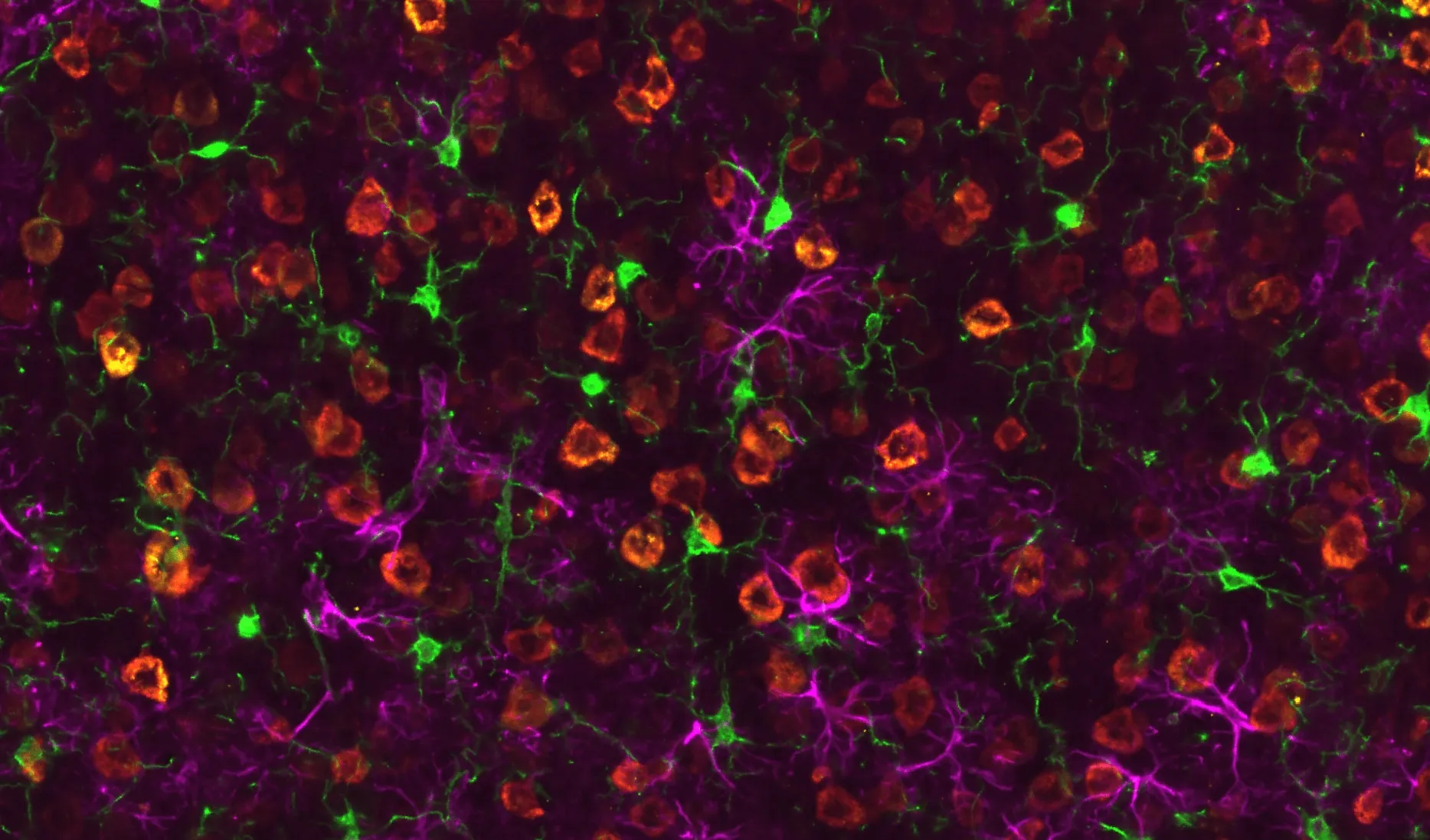
Pathologie TDP-43 et activation gliale dans le cortex moteur de la sourisrNLS8 (TDP-43ΔNLS).
Région représentative du cortex moteur d'une coupe coronale FFPE provenant d'une souris rNLS8. La TDP-43 phosphorylée (pTDP-43) est visualisée en jaune, la TDP-43 humaine (hTDP-43) en rouge, les microglies Iba1-positives en vert etles astrocytes GFAP-positifs d' een violet. Les microglies activées étendent leurs processus qui entrent en contact avec le soma neuronal et les régions d'accumulation de TDP-43, tandis que les astrocytes présentent une régulation à la hausse réactive du GFAP. Cette coloration multiple met en évidence l'agrégation pathogène de TDP-43 ainsi que les réponses microgliales et astrocytaires caractéristiques du modèle rNLS8 de la SLA.
Dans ces modèles de SLA, nous procédons systématiquement à la marquage des cerveaux et des moelles épinières pour détecter :
- TDP-43 humaine
- TDP-43 phosphorylée (pTDP-43)
- GFAP (astrocytes)
- Iba1 (microglies)
- ATP5A (mitochondries)
- Motoneurones spinaux (ChAT)
Nous colorons également les muscles pour les jonctions neuromusculaires (NMJ) à l'aide de :
- α-bungarotoxine
- SV2A
- β-III-tubuline
Notre équipe a développé des analyses d'images robustes pour les modèles de SLA :
- Veuillez consulter notre présentation interactive – Immunofluorescence multiplexe de coupes cérébrales provenant du modèle murin « Low Dox » TDP-43ΔNLS de la SLA.
- Nous vous invitons à consulter notre « Image interactive » – Dénervation de la jonction neuromusculaire (NMJ) dans le modèle murin TDP-43ΔNLS (rNLS8) de la SLA.
Si vous disposez de cerveaux, de moelles épinières, de muscles ou d'autres tissus provenant de modèles TDP-43 et/ou d'autres modèles de SLA (par exemple C9orf72, SOD1, PFN1), nous serions ravis de collaborer avec vous.
Nous pouvons également compléter la marquage IHC par des biomarqueurs liquides provenant du sang et du LCR, tels que :
- Chaîne légère du neurofilament (NF-L)
- TDP-43
- GFAP
- Cytokines (par exemple IL-1β, TNF-α)
- Chimiokines
- PSD-95
Pour en savoir plus sur ces biomarqueurs, veuillez consulter notre page Services de biomarqueurs cellulaires et liquides.
Marquage mIF dans les modèles murins de la maladie d'Alzheimer et des tauopathies
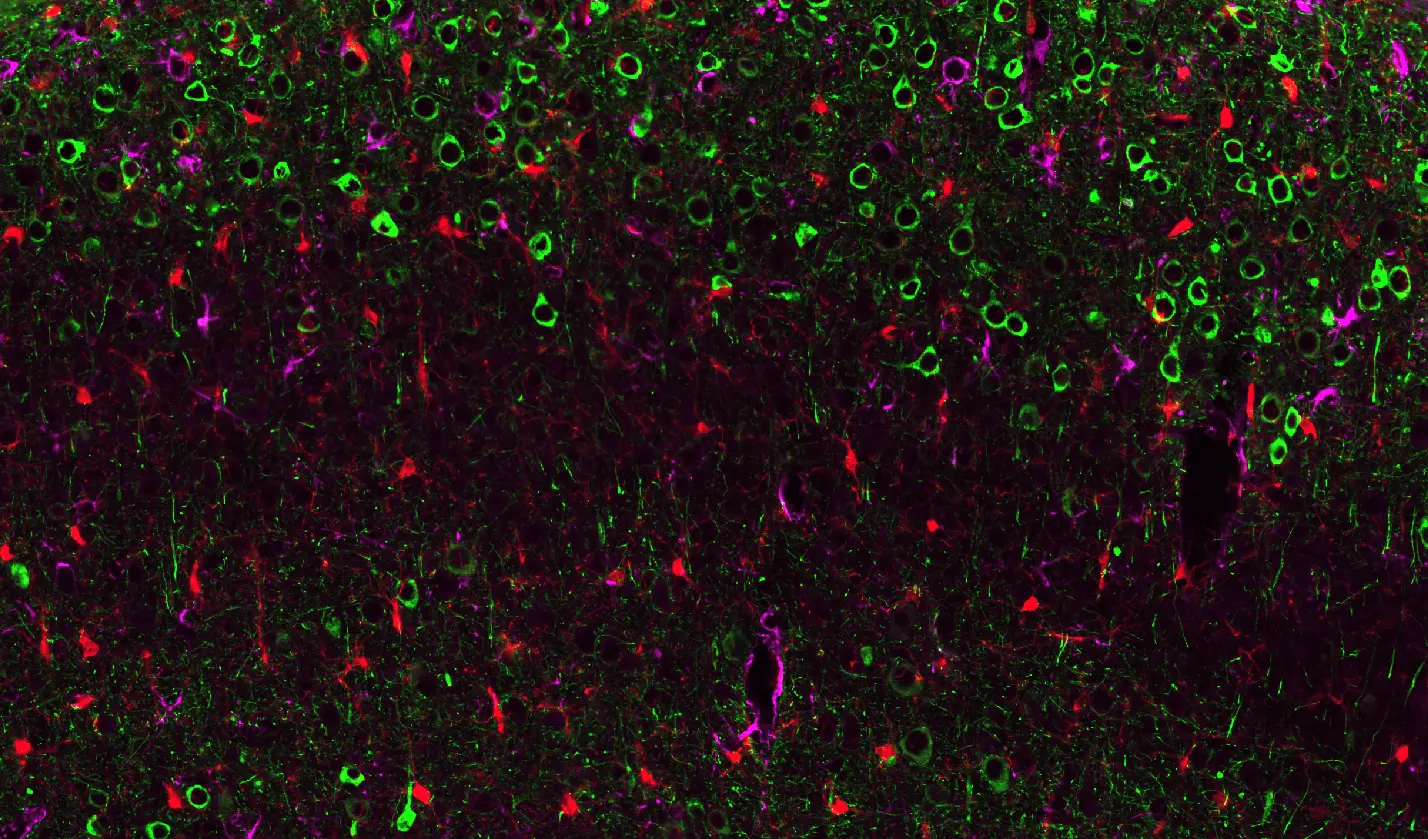
Agrégats pathologiques de protéine Tau chez des souris WT injectées avec AAV-hTau.
Région représentative du cortex piriforme d'une coupe coronale du cerveau d'une souris de type sauvage injectée avec AAV-hTau. La protéine Tau phosphorylée (AT8) est visualisée en vert, les microglies Iba1-positives en rouge et les astrocytes GFAP-positifs en violet, les noyaux étant contre-colorés à l'aide de DAPI. Les microglies activées étendent leurs processus vers les neurones Tau-positifs, tandis que les astrocytes présentent une régulation à la hausse réactive du GFAP.
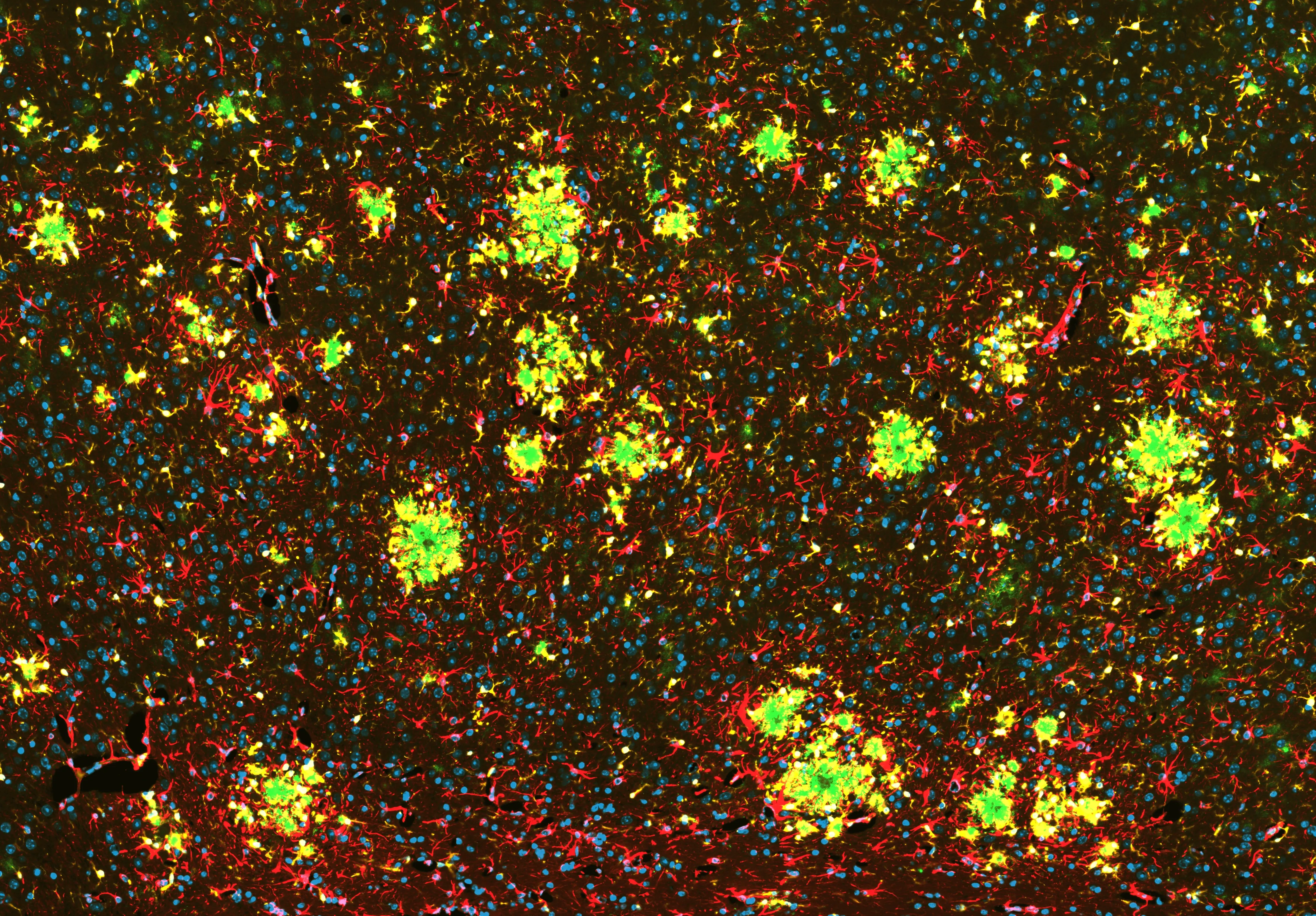
Pathologie amyloïde-β et activation gliale dans le cerveau de souris APP/PS1
Coupe coronale représentative du cerveau d'une souris transgénique APP/PS1. Les fibrillesAβpositives à l'anticorps OC sont visualisées en vert, les astrocytes positifs à la GFAP en rouge et les microglies positives à l'Iba1 en jaune, les noyaux étant contre-colorés à l'aide de DAPI (bleu). Les microglies activées étendent leurs processus vers les dépôts amyloïdes, tandis que les astrocytes présentent une régulation à la hausse réactive du GFAP. Cette coloration multiple met en évidence l'accumulation d'amyloïde-β fibrillaire ainsi que les réponses coordonnées des microglies et des astrocytes dans les régions touchées dans ce modèle APP/PS1 de la maladie d'Alzheimer.
Dans ces modèles de maladie d'Alzheimer et de tauopathie, nous procédons systématiquement à la coloration des cerveaux pour détecter :
- Bêta-amyloïde (divers anticorps Aβ)
- La protéine tau phosphorylée (AT8)
- La protéine tau à conformation modifiée (MC1)
- GFAP (astrocytes)
- Iba1 (microglies)
- NeuN (neurones)
- ASC (inflammasome)
Notre équipe a développé des analyses d'images robustes pour les modèles de la maladie d'Alzheimer, notamment :
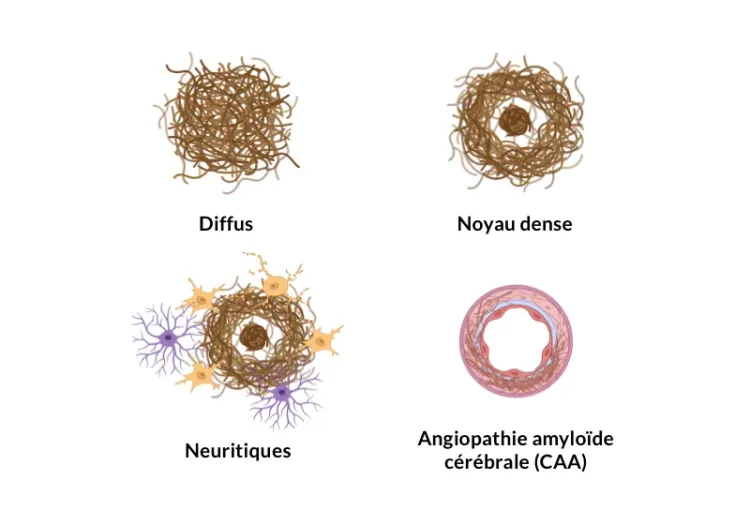
- Caractérisation des plaques amyloïdes (par exemple, taille, type [compactes, diffuses, fibrillaires], nombre) ; veuillez consulter notre ressource : Analyse des plaques amyloïdes-β dans la maladie d'Alzheimer
- Analyse du microenvironnement inflammatoire ; veuillez consulter notre rubrique Innovation : Amyloïde-β et microenvironnement inflammatoire dans un modèle murin APP/PS1 de la maladie d'Alzheimer
- Analyse des astrocytes réactifs ; veuillez consulter notre rubrique Innovation : Astrocytes et modèles murins de la maladie d'Alzheimer avec bêta-amyloïde
Veuillez également consulter notre présentation interactive intitulée « Tau, plutôt que l'amyloïde-β, est responsable de la neurodégénérescence dans la maladie d'Alzheimer (MA) et les modèles murins de la MA ».
Si vous disposez de cerveaux ou d'autres tissus provenant de souris APP/PS1 et/ou d'autres modèles murins ou rats de la maladie d'Alzheimer ou de tauopathies (par exemple, souris PS19, souris 5xFAD, souris ou rats APP KI, souris JNPL3, souris rTg4510), nous serions ravis de collaborer avec vous.
Nous pouvons également compléter la coloration IHC par des biomarqueurs liquides provenant du sang et du LCR ou des surnageants d'homogénats cérébraux, tels que :
- Chaîne légère du neurofilament (NF-L)
- Aβ40 et Aβ42
- Tau totale et tau phosphorylée
- GFAP
- Cytokines (par exemple, IL-1β, TNF-α)
- Chimiokines
- APOE4
- PSD-95
Pour en savoir plus sur ces biomarqueurs, veuillez consulter notre page Services de biomarqueurs cellulaires et liquides.
Coloration mIF dans des modèles murins de la maladie de Parkinson
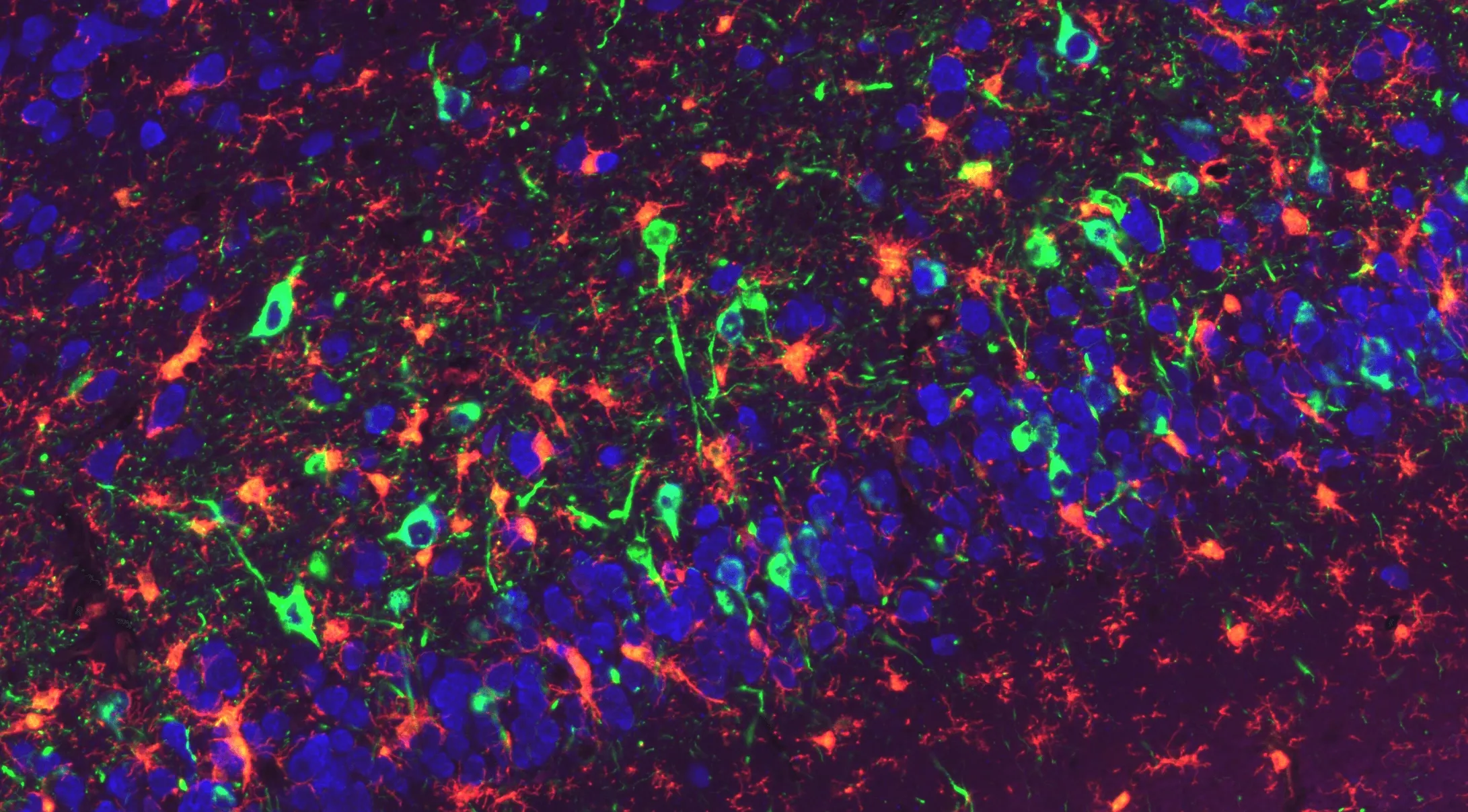
Pathologie de l'α-synucléine phosphorylée et implication des microglies dans le cortex piriforme de souris M83+/-
Région représentative du cortex piriforme d'une coupe coronale FFPE provenantd'unesouris transgénique M83 d' (surexprimant l'α-synucléine humaine A53T) injectée avec des fibrilles préformées d'α-synucléine (PFF). L'a-synucléine phosphorylée (pSyn129) est visualisée en vert, les noyaux neuronaux NeuN-positifs en bleu et les microglies Iba1-positives en rouge. L'accumulation de pSyn met en évidence la pathologie synucléine induite par les PFF au sein des populations neuronales, tandis que les microglies étendent leurs processus vers les somas neuronaux chargés de pSyn et le neuropile environnant. Cette coloration multiple délimite la relation entre l'agrégation induite de l'α-synucléine et l'activation microgliale dans le cortex piriforme des sourisM83 ayant reçu une injection de PFF .
Dans ces modèles de la maladie de Parkinson, nous procédons systématiquement à la coloration des cerveaux pour détecter :
- α-synucléine phosphorylée (pSyn129)
- GFAP (astrocytes)
- Iba1 (microglies)
- NeuN (neurones)
- Tyrosine hydroxylase (neurones dopaminergiques)
Notre équipe a développé des analyses d'images robustes pour les modèles de la maladie de Parkinson, notamment :
- Microglia activée ; veuillez consulter notre innovation : Activation microgliale dans un modèle murin PFF a-synucléine de la maladie de Parkinson
Si vous disposez de cerveaux provenant de modèles murins ou rats transgéniques, knock-in, knock-out, humanisés ou induits par des toxines (par exemple MPTP, 6-OHDA, roténone) de la maladie de Parkinson, nous serions ravis de collaborer avec vous.
Nous pouvons également compléter la coloration IHC par des biomarqueurs liquides provenant du sang et du LCR ou des surnageants d'homogénat cérébral, tels que :
- Chaîne légère du neurofilament (NF-L) [voir également notre ressource - Chaîne légère du neurofilament dans les modèles de la maladie de Parkinson]
- GFAP
- Cytokines (par exemple, IL-1β, TNF-α)
- Chimiokines
- PSD-95
Pour en savoir plus sur ces biomarqueurs, veuillez consulter notre page Services de biomarqueurs cellulaires et fluidiques.
Coloration mIF dans des modèles murins de sclérose en plaques
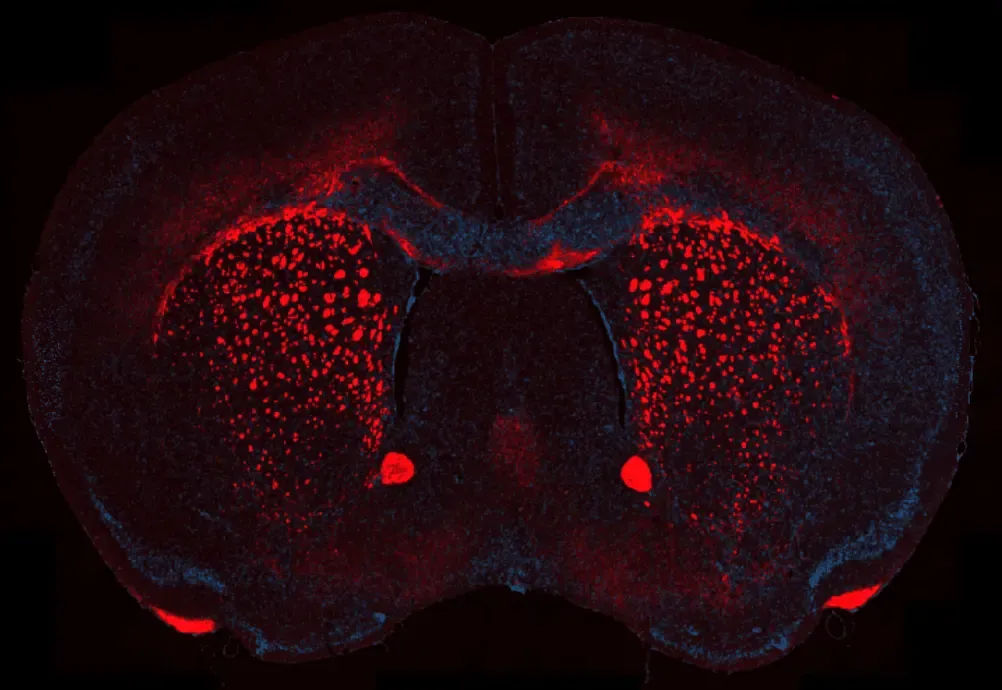
Perte de myéline dans le modèle de démyélinisation à la cuprizone
Région représentative du corps calleux d'une coupe cérébrale coronale FFPE provenant d'une souris présentant une démyélinisationinduite par la cuprizone. La protéine basique de la myéline (MBP) est visualisée en rouge, mettant en évidence les régions de perte et de fragmentation de la myéline, tandis que les noyaux sont contre-colorés avec du DAPI (bleu). Cette coloration permet de mettre en évidence la réduction caractéristique de la myéline compacte associée au traitement au cuprizone et d'évaluer la gravité de la démyélinisation dans les voies de la substance blanche touchées.
Dans ces modèles de sclérose en plaques (SEP), nous procédons systématiquement à la coloration des cerveaux et des moelles épinières pour détecter :
- MBP, MOG ou PLP (myéline)
- GFAP (astrocytes)
- Iba1 (microglies et macrophages)
- CD3 (cellules T)
- Oligodendrocytes matures
- Marqueurs des cellules précurseurs des oligodendrocytes (OPC)
- Marqueurs de lésions axonales
Notre équipe a développé des analyses d'images robustes pour les modèles de SEP, notamment :
- Marqueurs de lésions et dommages axonaux ; veuillez consulter notre ressource : Encéphalomyélite auto-immune expérimentale et lésions axonales
Nous pouvons également compléter la coloration IHC par des biomarqueurs liquides provenant du sang et du LCR ou des surnageants d'homogénat cérébral, tels que :
- La chaîne légère du neurofilament (NF-L) [voir également notre ressource - Encéphalomyélite auto-immune expérimentale et lésion axonale]
- GFAP
- Cytokines (par exemple, IL-1β, TNF-α)
- Chimiokines
- PSD-95
Vous pouvez en savoir plus sur ces biomarqueurs sur notre page Services de biomarqueurs cellulaires et liquides.
Si vous disposez de cerveaux, de moelles épinières ou d'autres tissus provenant d'EAE, de cuprizone et/ou d'autres modèles murins ou rats de sclérose en plaques (par exemple, LPC), nous serions ravis de collaborer avec vous.
Qu'est-ce que l'immunofluorescence multiplexe (mIF) ?
L'immunofluorescence multiplexe (mIF) est une technique puissante qui permet la détection simultanée de plusieurs cibles protéiques dans la même coupe tissulaire à l'aide d'anticorps conjugués à des fluorophores spectralement distincts, tels que ceux de la série Alexa Fluor (AF488, AF555, AF647, AF750). En préservant le contexte spatial, la mIF fournit des cartes détaillées de la coexpression cellulaire, de la localisation subcellulaire, des interactions intercellulaires et de l'organisation du microenvironnement. Cette approche permet de visualiser directement les interactions entre plusieurs marqueurs dans le cerveau, la moelle épinière, les muscles, etc., tels que les agrégats de protéines pathogènes, les cellules gliales activées et les populations neuronales, au sein d'une même région tissulaire. Dans la recherche sur les maladies neurodégénératives, la mIF est essentielle pour disséquer des pathologies complexes, notamment la co-agrégation de protéines pathologiques, les phénotypes gliaux hétérogènes, les contacts/interactions microgliaux-neuronaux et les réponses neuroinflammatoires. Elle permet également une évaluation quantitative fiable de la progression de la maladie, une analyse spatiale des biomarqueurs et des effets thérapeutiques (Hickey, 2021; Park, 2022; Bull, 2024).
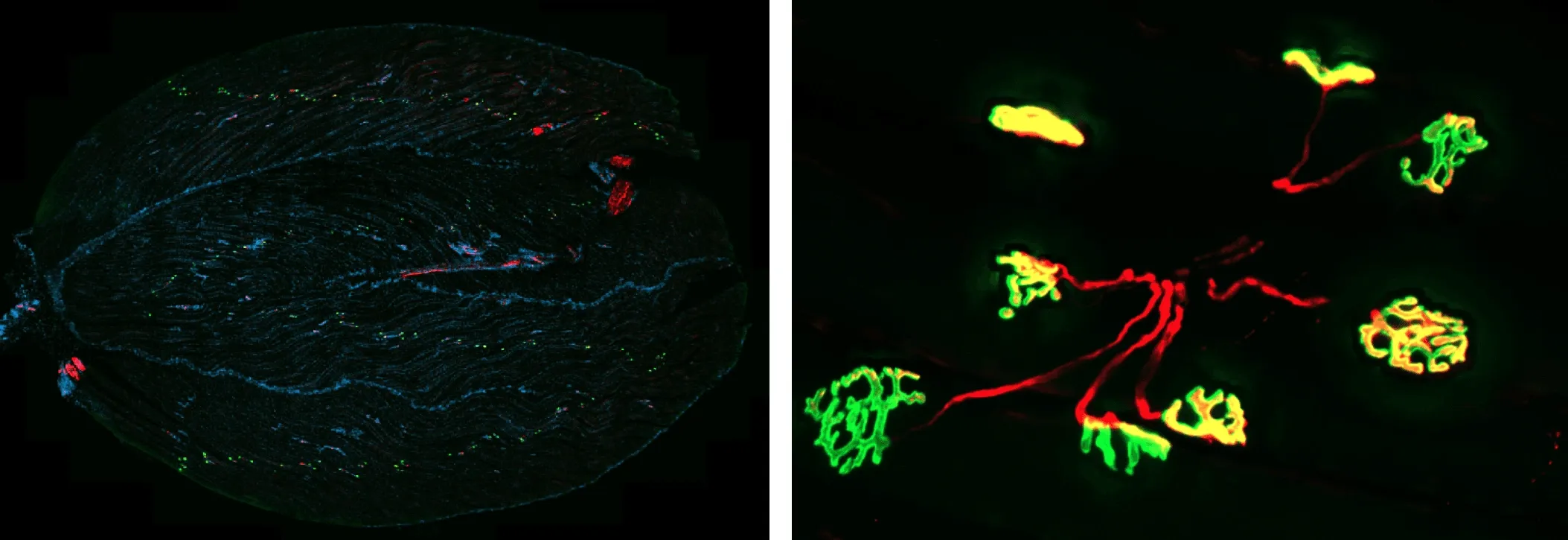
Visualisation dela jonction neuromusculaire (JNM) dans le muscle gastrocnémien de souris.
(À gauche) Coupe représentative dumuscle gastrocnémiende souris . Le marquage à l'α-bungarotoxine (BTX) des récepteurs de l'acétylcholine (ACh) est visualisé en vert, la protéine SV2A des vésicules synaptiques et la tubuline sont visualisées en rouge, et les noyaux sont contre-colorés avec du DAPI (bleu). Cette marquage permet de visualiser l'architecture de la jonction neuromusculaire, y compris les compartiments présynaptiques et postsynaptiques, au sein des fibres musculaires.
(À droite) Imageà plus fortgrossissement de la jonction neuromusculaire montrantdes jonctions neuromusculaires partiellement et entièrement innervées.
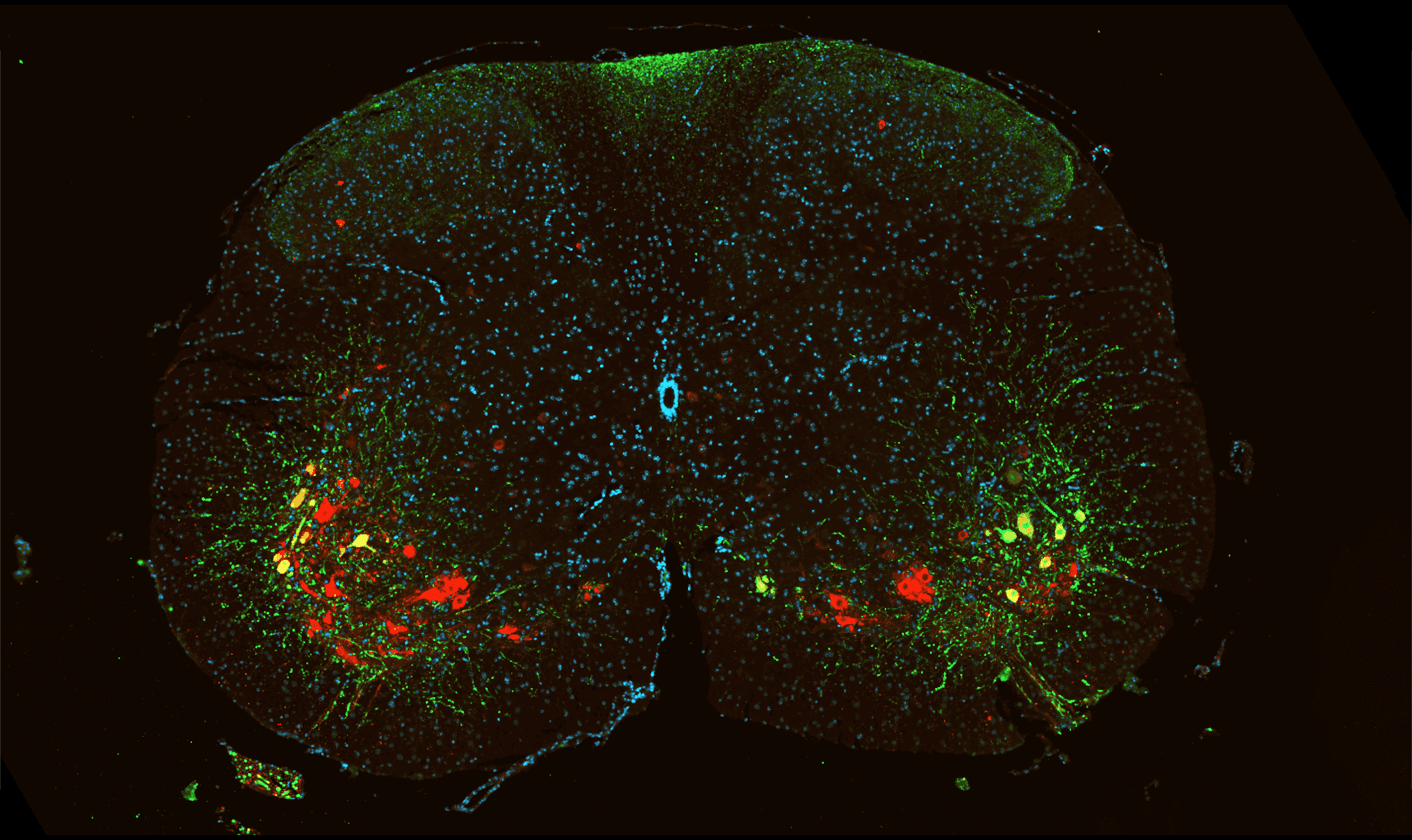
Visualisationdes motoneurones dans la moelle épinière de souris.
Coupe représentative de la moelle épinière de souris. Les neuronesexprimant la GFP sont visualisés en vert et les neurones cholinergiques ChAT-positifs sont visualisés en rouge. Les noyaux sont contre-colorés avec du DAPI (bleu).
Illustration du processus de Biospective consistant à prélever des tissus sur des modèles animaux, à réaliser des coupes tissulaires, à effectuer un marquage immunofluorescent multiplex, à scanner des lames entières et à procéder à une analyse quantitative des images.
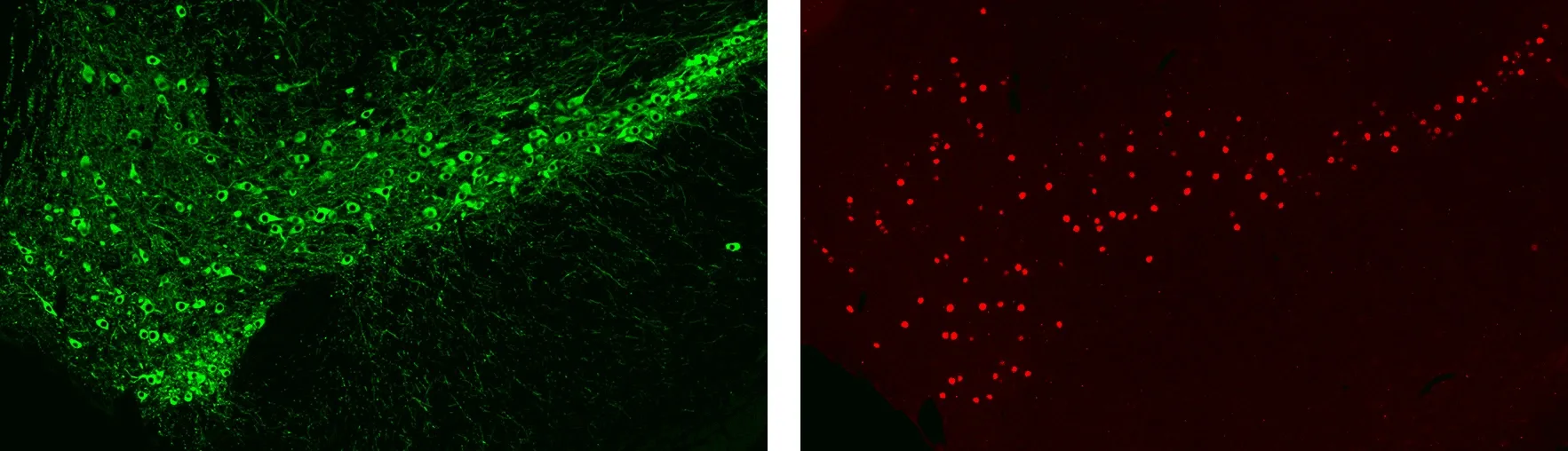
Coloration par immunofluorescence (IF) de la substance noire de souris pour les corps cellulaires et les processus dopaminergiques (à gauche) et les noyaux neuronaux (à droite).
Chez Biospective, nos laboratoires utilisent plusieurs colorateurs IHC/IF automatisés, garantissant :
- Une reproductibilité élevée
- Une faible variabilité
- Un délai d'exécution rapide
- Une cohérence optimale pour les grandes cohortes
Nous disposons de panels IF multiplex validés pour les modèles murins de maladies neurologiques et pouvons développerdes protocoles de marquage personnalisés adaptés à vos besoins de recherche. Notre équipe de R&D dédiée, composée de scientifiques et de techniciens expérimentés, veille à ce que chaque protocole soit optimisé en termes de reproductibilité, de sensibilité et d'analyse quantitative de haute qualité.
Pour en savoir plus sur nos services d'immunofluorescence multiplexe,
Découvrez nos services de marquage par immunofluorescence.
Contenu connexe
Informations actualisées sur nos services d'immunohistochimie (IHC) et les meilleures pratiques liées à l'évaluation des agents thérapeutiques dans les modèles animaux de maladies neurodégénératives.
Analyse des plaques amyloïdes-β dans la maladie d'Alzheimer
Aperçu des méthodes de classification et de quantification des plaques Aβ dans les coupes de tissus cérébraux provenant d'humains et de modèles animaux de la maladie d'Alzheimer (souris et rats transgéniques).
Amyloïde-β et microenvironnement inflammatoire chez la souris Alzheimer
Nous avons analysé les relations spatiales complexes entre les plaques β-amyloïdes, la microglie activée et au repos, et les astrocytes dans un modèle transgénique APP/PS1.
Souris TDP-43 ΔNLS (rNLS8) pour le développement de médicaments contre la SLA
Cette ressource fournit des informations sur l'utilisation du modèle de souris transgénique TDP-43 ΔNLS (deltaNLS, hTDP-43ΔNLS, hTDP-43DeltaNLS, dNLS, TDP43 NLS, rNLS8) de la SLA pour des études thérapeutiques précliniques.