Qu'est-ce que l'APOE ε4?
La maladie d'Alzheimer (MA) est une maladie neurodégénérative progressive caractérisée par un déclin progressif de la mémoire et des fonctions cognitives. La MA est la cause la plus fréquente de démence chez les personnes âgées de plus de 65 ans, et sa prévalence augmente à l'échelle mondiale en raison du vieillissement de la population. La maladie est associée à l'accumulation de deux protéines caractéristiques dans le cerveau: les plaques amyloïdes (Aβ) et les enchevêtrements tau. Ces dépôts perturbent la communication neuronale, entraînant la mort cellulaire et des troubles cognitifs.
La MA se divise en deux formes:
- La maladie d'Alzheimer à début précoce (EOAD), qui est rare et se développe généralement avant l'âge de 65 ans.
- La maladie d'Alzheimer à début tardif (LOAD), qui représente plus de 95% des cas de MA et survient généralement après 65 ans.
Bien que la cause exacte de la MA reste incertaine, on sait qu'une combinaison de facteurs génétiques, environnementaux et liés au mode de vie contribue à la maladie. Parmi ceux-ci, la prédisposition génétique est un facteur de risque important, et l'un des facteurs génétiques les plus connus contribuant à la MA est le gène APOE.
Le gène APOE (apolipoprotéine E) est situé sur le chromosome 19 et code la protéine apolipoprotéine E (ApoE), qui joue un rôle clé dans le métabolisme des lipides, la réparation neuronale et la fonction immunitaire au sein du système nerveux central (SNC). L'ApoE est impliquée dans le transport des lipides, y compris le cholestérol, qui sont essentiels à l'intégrité neuronale et à la fonction synaptique.
Le gène APOE existe sous trois isoformes principales - APOE ε2, APOE ε3 et APOE ε4 - qui diffèrent par une seule substitution d'acide aminé. L'APOE ε3 est la plus courante et est considérée comme « neutre » en ce qui concerne le risque de MA, tandis que l'APOE ε2 est considérée comme protectrice. Cependant, l'APOE ε4 augmente considérablement le risque de développer une MA tardive.
Les mécanismes pathologiques à l'origine de ce risque accru sont complexes et impliquent l'interaction entre l'ApoE4 et divers processus cellulaires dans le cerveau. Plus précisément, on pense que l'ApoE4 altère le métabolisme lipidique, perturbe la fonction microgliale et interfère avec l'élimination de l'Aβ, ce qui contribue à l'accumulation de protéines toxiques et à une inflammation chronique dans le cerveau.
De plus, l'ApoE4 favorise l'agrégation de l'Aβ, facilitant la formation de plaques qui endommagent les neurones. L'ApoE4 module également la pathologie tau, favorisant l'hyperphosphorylation de la protéine tau, ce qui conduit à la formation d'enchevêtrements neurofibrillaires, une caractéristique distinctive de la MA. La combinaison d'une élimination altérée de l'Aβ, de l'agrégation de la protéine tau et de la neuroinflammation entraîne la progression de la maladie, conduisant à une perte neuronale et à un déclin cognitif (Shi, 2017; Najm, 2020).
Comment les interactions entre l'APoE4 et les microglies influencent-elles la progression de la maladie d'Alzheimer?
Les microglies sont les cellules immunitaires résidentes du SNC, représentant environ 10 à 15% des cellules du cerveau. Elles jouent un rôle essentiel dans le maintien de l'homéostasie cérébrale en surveillant constamment l'environnement cérébral à la recherche de lésions, en éliminant les débris et en régulant l'inflammation. Dans des conditions normales, les microglies contribuent à protéger les neurones contre les lésions et à soutenir la fonction synaptique en éliminant les déchets cellulaires, notamment les protéines mal repliées, telles que l'Aβ et la tau. Cependant, dans la MA, en particulier chez les personnes porteuses de l'allèle APOE ε4 , les microglies subissent un dysfonctionnement qui contribue à la progression de la maladie.
En présence d'ApoE4, la fonction microgliale est considérablement altérée de la manière suivante:
Altération de l'élimination de l'Aβ
- L'ApoE4 réduit la capacité des microglies à éliminer efficacement les peptides Aβ, ce qui entraîne une accumulation de plaques (Deane, 2008; Najm, 2020).
- Normalement, les microglies expriment les récepteurs P2RY12, qui sont essentiels pour guider les microglies vers les dépôts de Aβ et permettre leur élimination. Chez les porteurs d'ApoE4, l'expression des récepteurs P2RY12 est régulée à la baisse, ce qui altère la motilité des microglies et leur capacité à éliminer efficacement les plaques Aβ (Sepulveda, 2024).
Pour une analyse des relations spatiales complexes entre les plaques Aβ, les microglies activées et au repos, et les astrocytes dans un modèle transgénique APP/PS1, voir: Amyloïde-β et microenvironnement inflammatoire chez la souris Alzheimer.
Environnement pro-inflammatoire
- L'accumulation d'Aβ déclenche l'activation microgliale, un processus destiné à favoriser l'élimination des débris cellulaires et à déclencher des réponses immunitaires. Cependant, en présence d'ApoE4, les microglies adoptent un phénotype pro-inflammatoire chronique qui exacerbe la neuroinflammation (Rao, 2025).
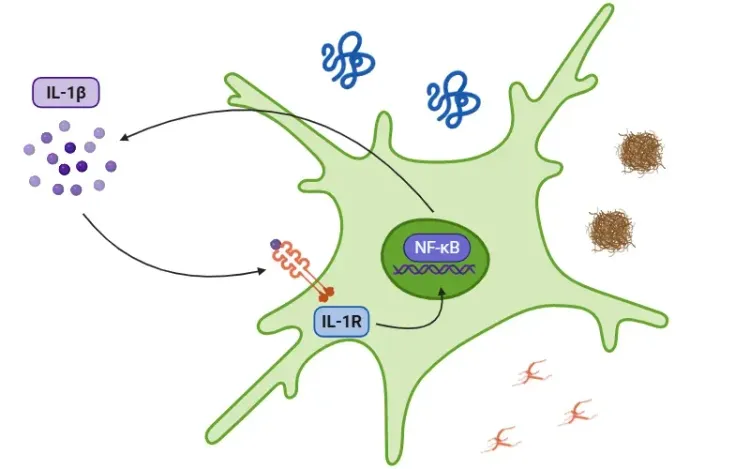
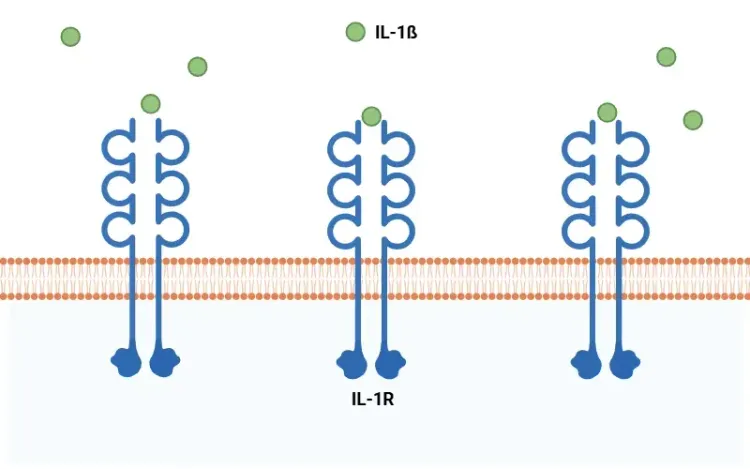
- Les microglies exprimant l'ApoE4 libèrent des niveaux élevés de cytokines pro-inflammatoires, notamment le TNF-α , l'IL-1β et l'IL-6 (Iannucci, 2021). Ces cytokines perpétuent l'inflammation chronique dans le cerveau.
- L'ApoE4 augmente également l'expression du TREM2, un récepteur impliqué dans l'activation des microglies associées à la maladie (DAM). Alors que l'activation des DAM vise à éliminer l'Aβ, elle favorise davantage l'inflammation et la neurodégénérescence (Iannucci, 2021).
Pour plus d'informations sur le rôle de la cytokine pro-inflammatoire IL-1β dans les maladies neurodégénératives, voir: Interleukine-1 bêta (IL-1β) et maladies neurodégénératives
Pathologie Aβ et Tau
- L'ApoE4 favorise la formation d'oligomères Aβ neurotoxiques, aggravant ainsi la pathologie amyloïde (Hashimoto, 2012).
- En plus de l'Aβ, l'ApoE4 augmente également l'hyperphosphorylation de la protéine Tau, ce qui conduit à la formation d'enchevêtrements neurofibrillaires, une caractéristique de la MA (Shi, 2017).
Perturbation du métabolisme lipidique
- L'ApoE4 altère le métabolisme lipidique, entraînant l'accumulation de gouttelettes lipidiques intracellulaires et de cholestérol dans les microglies (Wang, 2022).
- Cette accumulation de lipides compromet la fonction microgliale, altérant davantage la capacité à éliminer l'Aβ et d'autres protéines toxiques.
- De plus, ces déséquilibres lipidiques favorisent la signalisation pro-inflammatoire au sein des microglies, exacerbant encore davantage la neurodégénérescence.
Augmentation du stress oxydatif
- Les microglies exprimant l'ApoE4 produisent des niveaux élevés d'espèces réactives de l'oxygène (ERO), ce qui entraîne un stress oxydatif dans le cerveau (Liu, 2025).
- Les ROS endommagent les composants cellulaires, et le stress oxydatif altère davantage la fonction microgliale, favorisant un cercle vicieux d'inflammation et de neurodégénérescence.
Voir: Dysfonctionnement mitochondrial dans les microglies et les astrocytes
Changements morphologiques dans les microglies
- Normalement, les microglies ont des processus étendus et très ramifiés qui leur permettent de surveiller efficacement le cerveau et de réagir aux dommages.
- L'ApoE4 modifie la morphologie des microglies, ce qui entraîne un raccourcissement et une ramification moindre de leurs prolongements, altérant ainsi leur capacité à surveiller le cerveau à la recherche de dommages et à éliminer l'Aβ et la tau (Sepulveda, 2024).
Pour une analyse approfondie des changements morphologiques des microglies dans les maladies neurodégénératives, voir: Morphologie des microglies dans la SLA, la maladie d'Alzheimer et la maladie de Parkinson
Ensemble, ces interactions dysfonctionnelles entre l'ApoE4 et les microglies créent un cycle auto-entretenu de neuroinflammation, d'accumulation de plaques amyloïdes, de pathologie tau et de stress oxydatif. Ces événements pathologiques exacerbent non seulement les dommages neuronaux, mais accélèrent également la progression de la MA, entraînant un déclin cognitif et une neurodégénérescence.
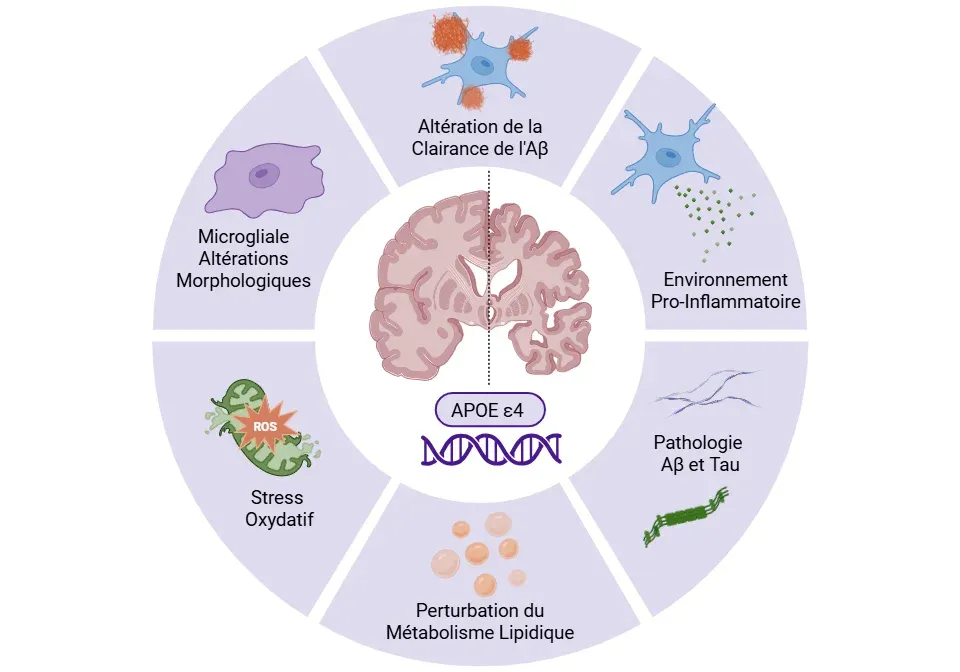
Dysfonctionnement microglial induit par l'ApoE4 dans la maladie d'Alzheimer.
L'ApoE4 modifie la morphologie et la fonction microgliales, altère la clairance de l'Aβ et perturbe le métabolisme lipidique, favorisant ainsi la pathologie Aβ et tau, un environnement pro-inflammatoire et le stress oxydatif, ce qui accélère globalement la neurodégénérescence.
Quelles stratégies thérapeutiques ciblent l'ApoE4 dans les microglies?
Compte tenu du rôle crucial de l'ApoE4 dans la progression de la MA, en particulier par ses effets sur la fonction microgliale et la neuroinflammation, plusieurs stratégies thérapeutiques ont été développées pour cibler directement l'ApoE4 ou moduler ses effets. Ces stratégies visent soit à corriger la structure de l'ApoE4, soit à réduire son expression, soit à contrer ses effets pathologiques en aval.
Petites molécules
- De petites molécules ont été conçues pour modifier spécifiquement la structure et la fonction de l'ApoE4, dans le but de stabiliser la structure de la protéine et d'empêcher ses changements conformationnels pathogènes (Dias, 2025).
- Les essais cliniques de phase III de l'ALZ-801 (valiltramiprosate) chez des homozygotes APOE ε4 présentant une déficience cognitive légère (MCI) ont donné des résultats prometteurs (NCT04770220, NCT06304883).
Oligonucléotides antisens (ASO)
- Les ASO sont des brins synthétiques d'oligodésoxynucléotides conçus pour se lier à l'ARN messager et réduire l'expression d'une protéine spécifique, en l'occurrence l'ApoE4.
- Des études précliniques ont démontré que les ASO ciblant l'ApoE4 peuvent réduire efficacement l'expression de l'ApoE4 et diminuer la pathologie Aβ dans des modèles murins de MA.
- Il est à noter que lorsqu'ils sont administrés avant le dépôt de plaques, les ASO sont capables de réduire la charge en Aβ. Cependant, lorsqu'ils sont administrés pendant la phase d'ensemencement, les ASO entraînent la formation de plaques Aβ plus importantes, mais avec une dystrophie neuritique associée aux plaques réduite, ce qui met en évidence les effets dépendants du moment d'administration des ASO (Huynh, 2017).
- Il a également été démontré que les ASO ciblant l'ApoE4 réduisent la pathologie tau, préservent la densité synaptique et réduisent la neuroinflammation dans les modèles murins de tauopathie (Litvinchuk, 2021).
Modification génétique
- Les technologies d'édition génétique, telles que CRISPR/Cas9, offrent la possibilité de modifier directement l'allèle APOE ε4 au niveau génétique. En corrigeant l'allèle ε4 pour obtenir les isoformes ε3 ou ε2, l'édition génétique pourrait potentiellement inverser le risque génétique sous-jacent de la MA.
- Les modèlesin vitro utilisant CRISPR/Cas9 ont donné des résultats prometteurs dans la réduction de la phosphorylation de la protéine tau, de la cytotoxicité et de la pathologie Aβ en améliorant la clairance de l'Aβ par les cellules gliales (Raulin, 2022).
- Les thérapies géniques basées sur l'AAV, comme le LX1001, qui utilise des vecteurs de virus adéno-associés (AAV) pour délivrer le gène APOE2 dans le cerveau, ont montré des résultats positifs lors des essais cliniques de phase précoce dans les cas de MA modérée et de MCI. Les données intermédiaires de ces essais indiquent une augmentation de l'expression de l'ApoE2, une réduction des biomarqueurs tau et une stabilisation de la pathologie Aβ (NCT03634007, NCT05400330).
Médicaments anti-inflammatoires (AINS)
- Les anti-inflammatoires non stéroïdiens (AINS) sont l'une des classes de médicaments les plus largement utilisées pour réduire l'activation microgliale et la libération de cytokines. Cependant, les résultats cliniques obtenus avec les AINS ont été variables et n'ont pas démontré une efficacité constante dans la MA (McGeer, 2007; Imbimbo, 2010).
Immunothérapies
- Les immunothérapies ciblant l'ApoE4 ou l'activation microgliale représentent une autre stratégie pour réduire la neuroinflammation et atténuer les effets pathologiques de l'ApoE4 dans la MA
- Des études précliniques sur des modèles de MA ont exploré les anticorps anti-ApoE pour cibler et neutraliser directement l'ApoE, réduisant ainsi ses effets pathologiques. Dans ces modèles, il a été démontré que les anticorps anti-ApoE favorisent le recrutement de microglies autour des plaques A&beta et réduisent la charge amyloïde (Kim, 2012; Liao, 2018).
Ces stratégies thérapeutiques en sont encore à différents stades de développement, mais elles représentent des approches prometteuses pour atténuer les effets néfastes de l'ApoE4 dans la MA. Les futurs essais cliniques seront essentiels pour déterminer la sécurité, l'efficacité et l'impact à long terme de ces interventions.
Notre équipe se fera un plaisir de répondre à toutes vos questions concernant l'influence de l'ApoE4 sur l'activité microgliale dans la maladie d'Alzheimer ou de vous fournir des informations spécifiques sur les modèles que nous utilisons pour les études d'efficacité thérapeutique.
En savoir plus sur nos modèles de maladies neurodégénératives
Contenu connexe
Informations actualisées sur la neuroinflammation et les meilleures pratiques liées à l'évaluation des agents thérapeutiques dans les modèles animaux de maladies neurodégénératives.
Interleukine-1 bêta (IL-1β) et maladies neurodégénératives
Le rôle de l'IL-1bêta dans les maladies neurodégénératives, notamment la maladie d'Alzheimer (MA), la maladie de Parkinson (MP) et la sclérose latérale amyotrophique (SLA).
TNF-α et microglie dans les maladies neurodégénératives
Un aperçu de la fonction du facteur de nécrose tumorale alpha (TNF-α) dans la microglie et de sa contribution à la progression de la neurodégénérescence.
Dysfonctionnement mitochondrial dans les microglies et les astrocytes
Le rôle du dysfonctionnement mitochondrial dans les microglies et les astrocytes dans les maladies neurodégénératives, notamment la maladie d'Alzheimer, la maladie de Parkinson et la SLA.
Dysfonctionnement lysosomal dans les microglies et les astrocytes
Un aperçu du dysfonctionnement lysosomal dans la microglie et les astrocytes, et de son rôle dans les maladies neurodégénératives.
Qu'est-ce que l'IL-1β?
Présentation générale de l'IL-1β, de son rôle pro-inflammatoire dans les maladies systémiques et neurologiques, et des stratégies thérapeutiques impliquant l'antagonisme de l'IL-1β.