このリソースでは、以下の内容について説明しています。
ミクログリアの老化とは何でしょうか?
ミクログリアは中枢神経系(CNS)内の多様な細胞集団であり、脳の常在免疫細胞として機能しています。ミクログリアは、恒常性の維持、損傷や感染への対応、細胞残骸の除去において重要な役割を果たしています。ミクログリアは、全脳細胞の約10~15%を占め、神経炎症反応の調整に不可欠であり、ミエリン化のようなプロセスにも寄与しています(Greenwood, 2021;Malvaso, 2023)。さらに、ミクログリアは免疫監視やシナプス再構築にも関与しています(Ng, 2023)。最近の研究では、ミクログリアは加齢に伴い老化し、通常の老化だけでなく、神経変性疾患を含むさまざまな疾患においても機能変化を引き起こすことが示唆されています(Ng, 2023)。
ミクログリアの老化には、老化関連分泌表現型(SASP)の獲得が伴い、不可逆的な細胞周期停止によって特徴づけられます(Greenwood, 2021;Malvaso, 2023)。この状態は、活性酸素種(ROS)や炎症性サイトカインの分泌量の増加、ミトコンドリアの機能不全、鉄やフェリチンの高レベル蓄積など、いくつかの重要な変化によって特徴付けられます。その結果、老化したミクログリアは、突起の分岐の減少、異常な膨潤、細胞裂開、空胞化などの特徴を示す、形態変化が現れます(Malvaso, 2023)。ミクログリアの老化の主な特徴は、貪食活性の低下と運動性の低下であり、これによって老廃物の除去や損傷部位への移動能力が妨げられます。老化ミクログリアの蓄積が一定の閾値を超えると、おそらく老化の傍分泌による拡散によって、老化関連疾患の進行が加速し、老化ミクログリアの数を増やすフィードフォワードループが形成される可能性があります(Chaib, 2022)。
ミクログリアの老化を定義することは、その特徴を定義する上でのコンセンサスが欠如しており、特定のマーカーも存在しないため困難です。さらに、老化ミクログリアの表現型は、ジストロフィー状態などの他の細胞状態と重複しており、これらはしばしば互換的に使用されています(Ng, 2023)。老化ミクログリアは、テロメアの短縮など、疾患関連ミクログリア(DAM)と共通の特徴も有しており、老化ミクログリアはDAMの別個のサブセットであると考えられています(Hu, 2021;Samuel Olajide, 2024)。 こうした課題があるにもかかわらず、老化関連神経変性疾患におけるミクログリア老化の役割は、治療介入の標的となりうる可能性を秘めており、研究の焦点となっています。
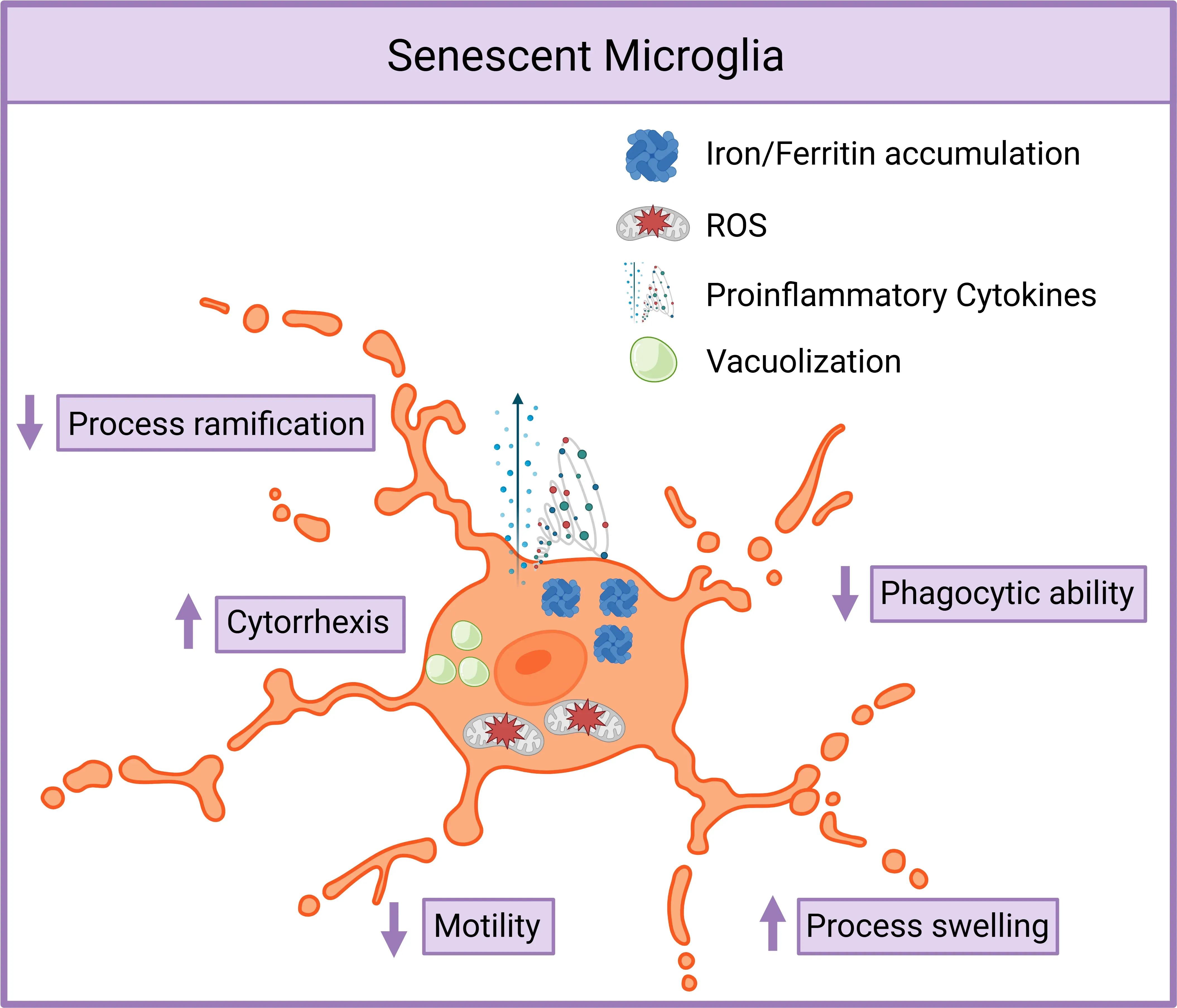
老化したミクログリアは、突起の分岐と運動性の低下、膨潤と細胞破裂の増加、空胞化を伴う細胞質断片化を示します。 また、鉄の蓄積量が増え、フェリチンの発現量が高まり、活性酸素種(ROS)の産生量も増加し、炎症性サイトカインの放出量も増えます。 残骸や有毒タンパク質を除去する食作用能力は著しく損なわれます。 図とキャプションは、クリエイティブ・コモンズ表示ライセンスに基づき 、Malvaso et al. (Malvaso, 2023)より改変しています。
クリックしてリンクをコピー
ADやPDにおいて、ミクログリアの老化はどのような役割を果たしているのでしょうか?
世界的な高齢化に伴い、タンパク質異常症を含む加齢性神経変性疾患の発生率は増加すると予想されています。老化は、アミロイドベータ(Aβ)、タウ、トランス活性化応答DNA結合タンパク質43kDa(TDP-43)、α-シヌクレイン(α-syn)などのミスフォールディングタンパク質の蓄積を特徴とするタンパク質病理学の主なリスク要因となります。そのため、これらの疾患の進行を遅らせたり、予防したりすることを目的とした標的療法への需要が高まっています。
老化したミクログリアは、通常の老化および神経変性疾患の両方において脳や脊髄に蓄積されるため、潜在的な治療介入の主要なターゲットとなっています。老化細胞を選択的に除去するように設計されたセノリック薬は、老化や炎症の影響を軽減または逆転させることを目的としています。これらの薬は前臨床試験で有望な結果を示しており、現在、神経変性疾患を含む加齢関連疾患の治療効果を評価するために、初期段階の臨床試験で試験されています。
アルツハイマー病(AD)
アルツハイマー病は、主に認知機能の低下、記憶障害、行動や気分に変化をもたらす進行性の神経変性疾患です。ベータ・アミロイド斑と過リン酸化タウ神経原繊維の蓄積が、アルツハイマー病の病態の中心となっています。これらの特徴的な症状以外にも、ミクログリアが病気の進行に重要な役割を果たしています。
タンパク質異常症における疾患進行のメカニズムとして提案されているものに、老化、疾患、異常なフォールディングタンパク質、老化したミクログリアの間の正のフィードバックループが関与しています(Lau, 2023)。このループでは、加齢によりミスフォールドタンパク質の蓄積が促進されますが、このプロセスは特にアルツハイマー病のような疾患で加速します。 ミスフォールドタンパク質の蓄積は、さらにミクログリアの老化を誘発し、これがさらにミスフォールドタンパク質の蓄積を悪化させます。 研究により、高レベルのタウにさらされたミクログリアは、細胞周期停止、タウ除去の低下、およびSASP(サイトカイン放出症候群)の形成を特徴とする老化表現型を獲得することが示されています(Karabag, 2023)。これらの老化したミクログリアは、アルツハイマー病の影響を受けた脳領域に蓄積し、そこでは傍分泌シグナル伝達によって周囲のミクログリアの老化が引き起こされます(Lau, 2023)。この連鎖反応により、神経毒性タンパク質の蓄積、神経変性、神経炎症がさらに悪化し、老化したミクログリアの貪食機能が低下することで、病気の進行が加速します(Lau, 2023;Miao, 2023)。
パーキンソン病(PD)
パーキンソン病(PD)は、アルツハイマー病に次いで2番目に多い神経変性疾患であり、主に筋肉の硬直、動作緩慢、安静時振戦などの運動症状が特徴です。見過ごされがちですが、パーキンソン病は、無気力やうつ病などの気分や情動の障害、認知機能障害、行動障害などの非運動症状とも関連しています。黒質緻密部(SNc)におけるドーパミン作動性ニューロンの進行性損失と、α-シヌクレイン凝集体を含むレビー小体の蓄積は、パーキンソン病の決定的な特徴です。ミクログリアがパーキンソン病の進行に寄与していることが知られていますが、パーキンソン病における老化ミクログリアの特定の役割については、アルツハイマー病(AD)と比較するとまだあまり理解が進んでいません(Rim, 2024)。
研究により、老化した脳、特にSNcにミクログリアが蓄積することが示されています(Shaerzadeh, 2020)。また、線条体内にα-シヌクレインを注射したところ、高齢のマウスでは、若いマウスと比較してα-シヌクレインのレベルが高いことが示されました(Hong, 2024)。このα-シヌクレインの増加は、オートファジー・リソソーム系の機能不全が原因と考えられる、加齢による除去の遅延によってさらに悪化します(Hong, 2024)。さらに、鉄の蓄積は、SNcなどのPDの影響を受ける領域で観察されており、過剰な鉄への曝露は、疾患を発症するリスクを高めることが分かっています(Angelova, 2019)。
結論として、アルツハイマー病とパーキンソン病はそれぞれ異なる病理学的特徴を持っていますが、特にミクログリアの機能不全という共通の基礎メカニズムをいくつか共有しています。両疾患において、ミクログリアは炎症を促進し、神経毒性タンパク質の除去を損なうことで、疾患の進行に寄与しています。神経変性疾患におけるミクログリアの老化の役割については、かなりの進展が見られていますが、効果的な治療法の開発には課題が残っています。しかし、現在進行中の老化細胞除去療法の研究は、これらの加齢関連疾患の治療に有望です。
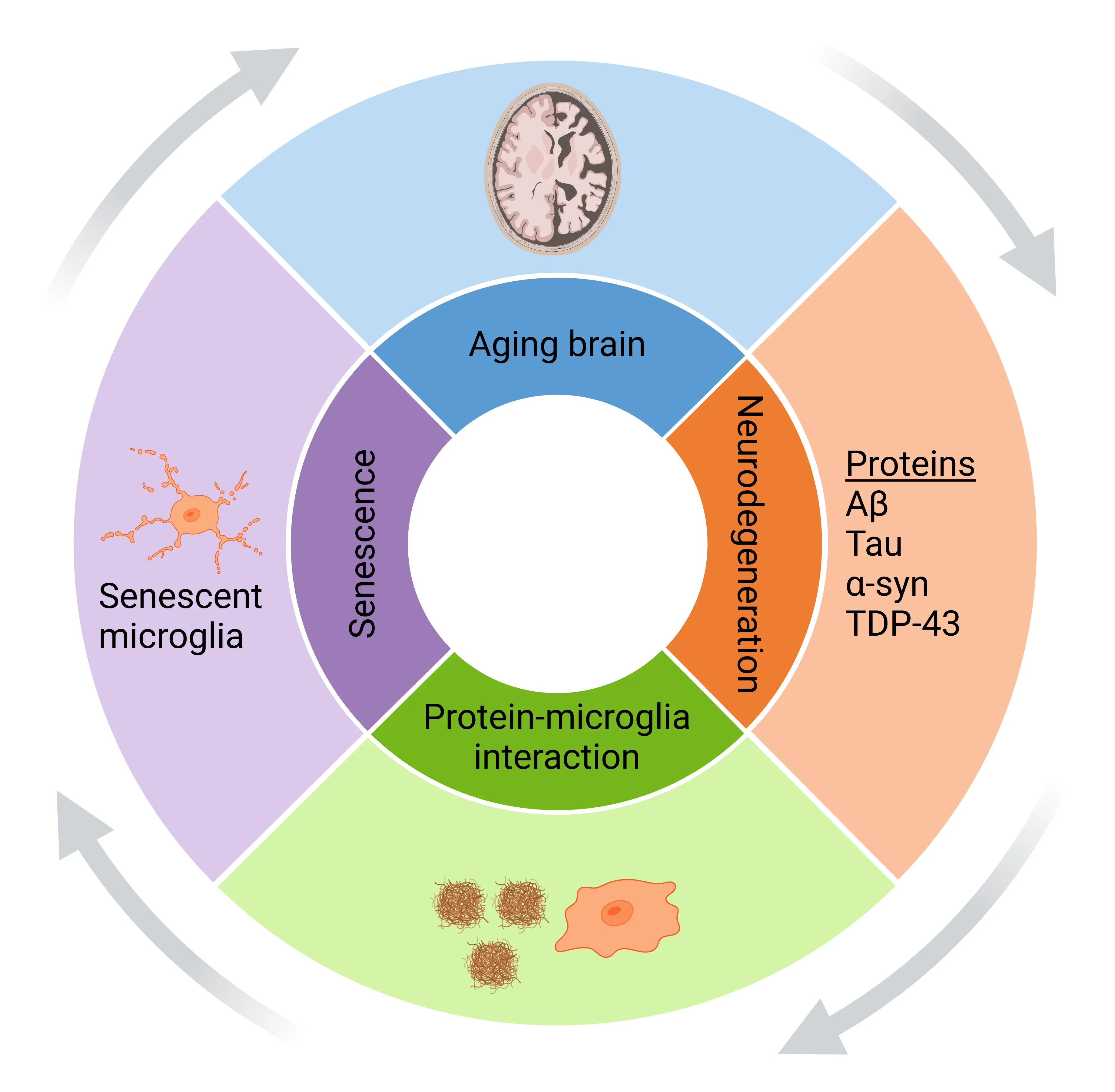
タンパク質異常症における疾患進行のメカニズムの概略図。 誤って折りたたまれたタンパク質の凝集体の蓄積は加齢に伴って起こり、疾患状態ではさらに悪化します。 これらのタンパク質はミクログリアと相互作用し、ミクログリアの老化を誘導します。これにより、神経毒性タンパク質の蓄積がさらに激化し、正のフィードバックループにより神経変性と疾患進行が加速されます。図とキャプションは、クリエイティブ・コモンズ表示ライセンスに基づき、Samuel Olajide et al. (Samuel Olajide, 2024) より改変しています。
ミクログリアの老化を研究するために現在使用されているモデルやマーカーは何ですか?
神経変性疾患におけるミクログリアの老化の役割に関する研究が進むにつれ、的を絞った治療戦略の開発がより急務となっています。しかし、特に生体内における老化ミクログリアを検出するための正確な方法が欠如しているため、これらの治療法の進歩は妨げられています。したがって、老化ミクログリアの信頼性の高いマーカーを特定することは、これらの治療努力を進める上で不可欠です。
ミクログリア老化の最も広く使用されているマーカーのひとつは、老化関連βガラクトシダーゼ(SA-β-gal)活性であり、これは依然として重要な指標となっています。さらに、細胞周期停止との強い関連性から、p21(別名WAF1/CIP1)やp16INK4aなどのサイクリン依存性キナーゼ阻害剤も、マーカーとして頻繁に使用されています。p16luc(ルシフェラーゼレポーターモデル )、p16ノックアウト、ミクログリア特異的p16ノックアウトマウスなどのモデルを含む、ミクログリアの老化の研究には動物モデルが役立っています。これらのモデルは、ミクログリアの老化におけるp16INK4aの役割と、加齢性神経変性疾患への寄与を解明する上で不可欠です。
フェリチンの蓄積もまた、老化したミクログリアで観察されていますが、その役割については他のマーカーほどにはよく理解されていません。リポフスチンの染色剤であるSudan Black Bは、SA-β-galの代替となる可能性のあるものとして注目されています(Ng, 2023)。ミクログリアのような老化細胞に蓄積するリポフスチンは、Sudan Black B を使用することで検出でき、老化ミクログリアを特定する有望な方法となりますが、まだ広く普及しているわけではありません。さらに、TNF-α、IL-6、IL-1βなどのSASPサイトカインの発現も、老化細胞の特徴です。これらの炎症促進性サイトカインは老化ミクログリアから放出され、神経炎症の一因となり、さまざまな神経変性疾患に関与しています。 これらのマーカーとミクログリアの老化との関連を示す証拠は増えつつありますが、決定的な単一のマーカーは確立されていません。 そのため、現在では、これらの指標のいくつかを組み合わせたマルチマーカーアプローチが、老化ミクログリアを特定する最も信頼性の高い方法と考えられています。
研究により、p16INK4aのようなマーカーの重要性が強調されており、特にミクログリアの老化に関する研究において重要な意味を持っています。例えば、マウスを対象とした研究では、ミクログリア、特に白質におけるミクログリアは、加齢に伴い中枢神経系で最初に老化する細胞であることが示されています(Matsudaira, 2023)。これらの研究により、ミクログリアの老化は脳と脊髄の両方で起こり、特にDAMで顕著であることが確認されています(Matsudaira, 2023 )。MAPT P301S(PS19)マウスなどのタウオパチーのモデルでは、p16INK4aを発現する老化ミクログリアが時間とともに蓄積することが明らかになっています(Bussian, 2018)。これらの老化細胞を標的とすることで、治療効果が期待されています。老化したミクログリアの除去は、タウ凝集および神経原線維変化の沈着を防止し、神経変性を軽減し、認知機能を維持するのに役立つことが分かっています。さらに、老化細胞除去剤の使用は、タウ凝集を調節することが示されています。これらの知見は、タウオパチーの治療法としての老化ミクログリアを標的とするアプローチの可能性を強調し、ミクログリアの老化と神経変性疾患の進行との関連性を強調しています(Bussian, 2018)。
老化ミクログリアを特定し標的とする能力の向上により、研究者たちは神経変性疾患に対する新たな治療介入の道筋を作っています。ミクログリアの老化とその加齢に伴う神経疾患の治療への影響についての理解を深めるには、これらのマーカーとモデルの継続的な使用が不可欠です。
ミクログリア老化と神経変性疾患に関するご質問や、治療効果研究に使用しているADおよびPDモデルに関する具体的な情報については、お気軽にお問い合わせください。
神経変性疾患モデルについてさらに詳しく知る
関連コンテンツ
ミクログリアの老化と神経変性疾患に関する最新情報と、神経変性疾患の動物モデルにおける治療薬の評価に関するベストプラクティス。
パーキンソン病におけるミクログリア、アストロサイト、およびα-シヌクレイン
α-シヌクレインがパーキンソン病およびその他のシヌクレイン病においてミクログリアおよびアストロサイトに及ぼす影響。
神経変性疾患におけるTNF-αとミクログリア
ミクログリアにおける腫瘍壊死因子-α(TNF-α)の機能と、神経変性進行への寄与についての概要。
NLRP3インフラマソームと神経変性疾患
NLRP3インフラマソームの概要と、アルツハイマー病、パーキンソン病、ALSなどの神経変性疾患におけるその役割について。
ALS, アルツハイマー病, パーキンソン病におけるミクログリアの形態
ミクログリアの形態解析の概要と, 神経変性疾患の研究および創薬・薬剤開発への応用。
ミクログリアとアストロサイトのライソゾーム機能不全
ミクログリアとアストロサイトのライソゾーム機能不全の概要と、神経変性疾患におけるその役割。