Modèles de fibrilles préformées d'α-synucléine (PFF) pour la maladie de Parkinson
La propagation pathologique de l'alpha-synucléine mal repliée, caractéristique de la maladie de Parkinson chez l'homme, peut être modélisée dans le cerveau des animaux par l'injection de fibrilles préformées d'α-synucléine (PFF). Ce "modèle d'ensemencement et de propagation des PFF" peut être induit chez des souris transgéniques surexprimant l'α-synucléine humaine ou chez des souris ou des rats de type sauvage.
Ce modèle animal hautement reproductible de synucléinopathie reproduit plusieurs caractéristiques clés de la MP humaine, notamment les agrégats d'α-synucléine dans le corps cellulaire et les neurites, la neurodégénérescence (mesurable par la chaîne légère des neurofilaments dans le sang et le LCR, ainsi que par des mesures in vivo de l'atrophie cérébrale basées sur l'IRM), la microgliose, l'astrogliose et la dénervation dopaminergique. Les déficits moteurs et les altérations de l'architecture du sommeil peuvent également être mesurés quantitativement dans ce modèle.
Modèle de souris AAV A53T Alpha-Synucléine de la maladie de Parkinson
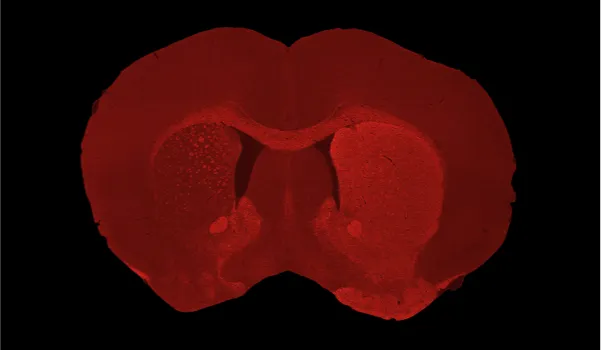
L'injection de vecteurs du virus adéno-associé (AAV) permet de générer la pathologie de l'alpha-synucléine dans le cerveau de rongeurs adultes. Dans ce modèle murin de la maladie de Parkinson, des souris de type sauvage (C57BL/6) subissent une injection stéréotaxique de vecteurs AAV surexprimant l'alpha-synucléine humaine mutante A53T dans la substantia nigra pars compacta.
Ce modèle robuste de synucléine présente pathologiquement des agrégats d'α-synucléine dans le soma des neurones et les neurites, une neuroinflammation (y compris une microglie activée et des astrocytes réactifs), une neurodégénérescence et une dénervation dopaminergique. Des déficits moteurs significatifs sont observés dans ce modèle suite à la perte unilatérale de neurones dopaminergiques, y compris des altérations dans le test d'agrippement des membres postérieurs, le test du rotarod, le test de suspension de la queue et le test du cylindre.
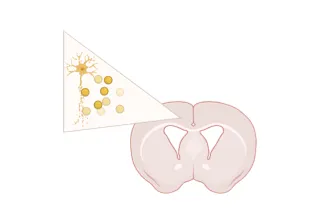
L'injection stéréotaxique unilatérale de vecteurs AAV-Syn induit une perte progressive de neurones dopaminergiques dans la substantia nigra pars compacta et des déficits moteurs associés (par exemple, basculement vers le côté controlatéral). Remarque : les neurones pigmentés sont représentés à des fins d'illustration (les souris n'ont pas de neurones pigmentés dans la substantia nigra).
En savoir plus sur la caractérisation de ces modèles murins de la maladie de Parkinson, sur nos mesures validées et sur nos services de CRO en neurosciences précliniques.
Contenu connexe
Informations actualisées sur la maladie de Parkinson et les meilleures pratiques liées à l'évaluation des agents thérapeutiques dans les modèles animaux de la maladie de Parkinson.
Modèles AAV d'α-synucléine pour le développement de médicaments contre la maladie de Parkinson
Vue d'ensemble des modèles de souris et de rats à α-synucléine induite par un vecteur du virus adéno-associé (AAV), à utiliser dans les études précliniques de thérapeutiques modificatrices de la maladie.
Le neurofilament à chaîne légère dans les modèles de la maladie de Parkinson
Comment les niveaux de neurofilament à chaîne légère (NfL ; NF-L) peuvent être utilisés comme biomarqueurs dans le sang et le LCR dans les modèles de souris et de rats atteints de la maladie de Parkinson.
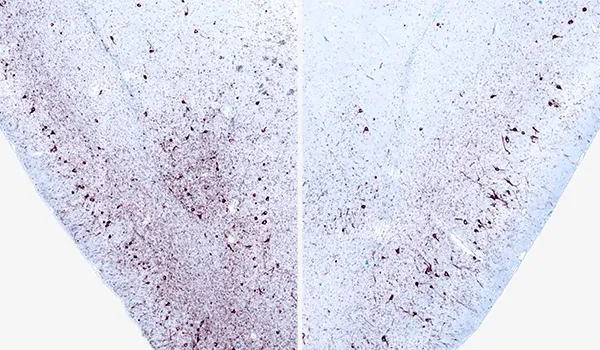
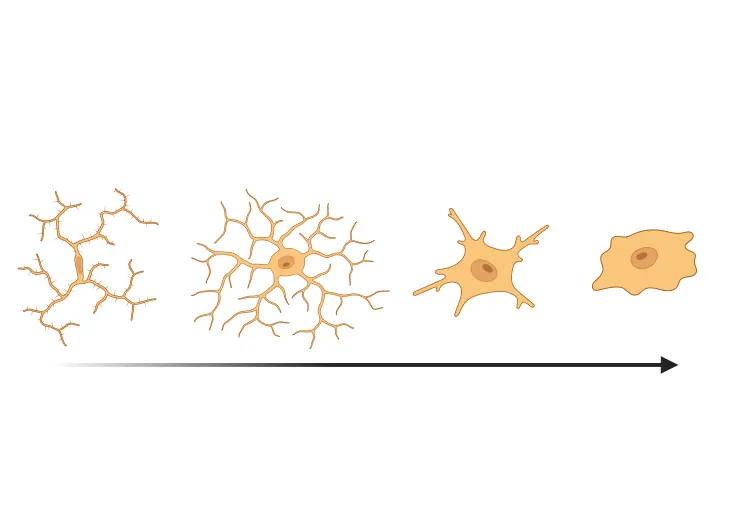
Activation microgliale dans un modèle de souris PFF à α-synucléine
Nous avons quantifié l'activation microgliale, sur la base de la morphologie, dans un modèle murin d'ensemencement et d'étalement de fibrilles préformées d'α-synucléine (PFF) de la maladie de Parkinson.